Abstract
目的
评估同种异体骨 Cage 在经椎间孔腰椎椎间融合术(transforaminal lumbar interbody fusion,TLIF)术后的融合效果。
方法
回顾分析 2015 年 1 月—2017 年 1 月使用同种异体骨 Cage 行 TLIF 的 30 例患者(38 个节段)临床资料。男 25 例,女 5 例;年龄 44~72 岁,平均 56.9 岁。腰椎间盘突出症 20 例,腰椎滑脱 7 例,腰椎管狭窄 3 例。手术节段:单节段 22 例,L3、4 4 例,L4、5 13 例,L5、S1 5 例;双节段 8 例,L4、5~L5、S1 6 例,L3、4~L4、5 2 例。病程 6~36 个月,平均 12 个月。术前,术后 3、6 个月及末次随访时采用疼痛视觉模拟评分(VAS)、Oswestry 功能障碍指数(ODI)和日本骨科协会(JOA)评分评估临床疗效;术后 3、6 个月摄正侧位 X 线片及行 CT 三维重建评估融合率;术前及术后 3 d、3 个月、6 个月分别摄腰椎正侧位 X 线片测量椎间隙高度。
结果
手术时间 2.1~4.3 h,平均 3.1 h;术中出血量 150~820 mL,平均 407.5 mL。30 例均获随访,随访时间 8~25 个月,平均 16.4 个月。1 例术后 6 个月出现 Cage 下缘碎裂,不伴 Cage 移动,无神经症状;其余患者均无 Cage 脱出、位移、碎裂等情况发生。所有患者均无局部或全身变态反应或感染征象,随访期间无神经压迫、受损症状。30 例患者术后各时间点 VAS 评分、ODI 评分及 JOA 评分均较术前显著改善(P<0.05);术后 6 个月及末次随访时显著优于术后 3 个月(P<0.05);术后 6 个月和末次随访间比较差异无统计学意义(P>0.05)。X 线片及 CT 三维重建示,术后 3、6 个月及末次随访时的融合率分别为 55.3%(21/38)、92.1%(35/38)、100%(38/38)。术后 3 d、3 个月、6 个月及末次随访时椎间隙高度均较术前显著改善(P<0.05);末次随访时与术后 3 d 比较椎间隙高度有所丢失,差异有统计学意义(P<0.05)。
结论
同种异体骨 Cage 在腰椎 TLIF 术后可提供早期稳定性和较高融合率。
Keywords: 同种异体骨, Cage, 经椎间孔腰椎椎间融合, 融合率, 椎间隙高度
Abstract
Objective
To explore the fusion effect of allograft Cages on transforaminal lumbar interbody fusion (TLIF).
Methods
The clinical data of 30 patients (38 vertebral segments) who underwent TLIF with allograft interbody fusion Cages between January 2015 and January 2017 were retrospectively analysed. There were 25 males and 5 females with an average age of 56.9 years (range, 44-72 years). The lesions included 20 cases of lumbar disc herniation, 7 cases of lumbar spondylolisthesis, and 3 cases of lumbar spinal stenosis. The operation section included 4 cases of L3, 4, 13 cases of L4, 5, 5 cases of L5, S1, 6 cases of L4, 5-L5, S1, and 2 cases of L3, 4-L4, 5. The disease duration was 6-36 months (mean, 12 months). The clinical effectiveness was evaluated by visual analogue scale (VAS) score, Oswestry disability index (ODI), and Japanese Orthopaedic Association (JOA) score at preoperation, 3 months and 6 months after operation, and last follow-up. The fusion rate was evaluated by anteroposterior and lateral X-ray films and CT three-dimensional reconstruction at 3 and 6 months after operation. The intervertebral space height was measured on anteroposterior and lateral X-ray films at preoperation, 3 days, 3 months, and 6 months after operation.
Results
The operation time was 2.1-4.3 hours (mean, 3.1 hours), and the intraoperative blood loss was 150-820 mL (mean, 407.5 mL). The follow-up time was 8-25 months (mean, 16.4 months). One Cage split at 6 months after operation without Cage movement and neurologic symptoms; none of the other patients had Cage prolapse, displacement, and fragmentation. No local or systemic allergy or infection signs was found in all patients. No nerve compression or symptoms was observed during the follow-up. The postoperative VAS score, ODI score, and JOA score improved significantly when compared with preoperative scores (P<0.05); and the scores at 6 months and at last follow-up were significantly improved when compared with those at 3 months after operation (P<0.05); but no significant difference was found between at 6 months and at last follow-up (P>0.05). The fusion rate was 55.3% (21/38), 92.1% (35/38), and 100% (38/38) at 3 months, 6 months, and last follow-up postoperatively. The intervertebral space height was increased significantly at 3 days, 3 months, 6 months, and last follow-up postoperatively when compared with preoperative ones (P<0.05); and the loss of intervertebral space height was significant at last follow-up when compared with postoperative at 3 days (P<0.05).
Conclusion
The allograft interbody fusion Cage contributes to the spine interbody fusion by providing an earlier stability and higher fusion rate.
Keywords: Allograft, Cage, transforaminal lumbar interbody fusion, fusion rate, intervertebral space height
脊柱退行性疾病是常见病、多发病,严重者多采用手术治疗,其中脊柱融合术相对安全可靠。但脊柱融合术也有着不低的失败率,有报道为 10%~40%[1-2],这些患者部分还需二次手术。传统的椎间融合术主要以自体骨块移植为主,其并发症众多,术后患者卧床时间长,术后稳定性差,同时患者椎间隙高度有所丢失。Cage 的主要作用有恢复椎间孔的高度,解除受压神经的压迫,恢复脊柱对应节段的正常生理曲度等[3-4]。Cage 的发明和使用显著提高了椎间融合术的融合率,同时在减少并发症方面也有突出改善[5]。传统的 Cage 多为金属或聚醚醚酮材料制成,弹性模量大,容易切割终板,造成椎间隙塌陷。同种异体骨的结构和理化性质与正常骨组织相似,其三维网状结构可被爬行替代,是一种理想的骨科手术移植物。目前关于同种异体骨制成的 Cage 用于临床的报道有很多,主要为同种异体股骨环(femoral cortical allograft,FCA)[6]和一种用于后路腰椎椎间融合术(posterior lumbar interbody fusion,PLIF)的 PLIF 垫片[7]。其中 FCA 主要应用于腰椎前路融合术或颈椎前路术,其融合率非常理想,1 年时达到了 98%[8];另一种为解剖型同种异体骨 Cage,其融合效果同样很好,有报道为 95.2%[9],并不低于使用聚醚醚酮 Cage 的融合率。目前尚罕见关于同种异体骨 Cage 在经椎间孔腰椎椎间融合术(transforaminal lumbar interbody fusion,TLIF)中应用的报道。
本研究回顾分析了 2015 年 1 月—2017 年 1 月采用同种异体骨 Cage 行 TLIF 手术并获成功随访的 30 例患者临床资料,评估其临床疗效及同种异体骨 Cage 的实用性和安全性。报告如下。
1. 临床资料
1.1. 患者选择标准
纳入标准:① 术前经至少 3 个月保守治疗无效或效果不明显的腰椎间盘突出或腰椎滑脱;② 既往无脊柱手术病史;③ 有腰椎融合术的手术指征。排除标准:① 严重骨质疏松;② 椎间隙高度狭窄;③ 3 个以上需融合节段;④ 局部或全身感染及其他严重全身疾病;⑤ 终板硬化;⑥ 使用免疫抑制剂或强过敏体质者。2015 年 1 月—2017 年 1 月共 30 例患者符合选择标准纳入研究。
1.2. 一般资料
本组男 25 例,女 5 例;年龄 44~72 岁,平均 56.9 岁。腰椎间盘突出症 20 例,腰椎滑脱 7 例,腰椎管狭窄 3 例。症状有间歇性跛行,腰腿痛、下肢无力等。手术节段:单节段 22 例,L3、4 4 例,L4、5 13 例,L5、S1 5 例;双节段 8 例,L4、5~L5、S1 6 例,L3、4~L4、5 2 例。病程 6~36 个月,平均 12 个月。无高血压、糖尿病等内科合并症。
1.3. 手术方法
本组采用的同种异体骨 Cage 采用 2 片皮质骨压制而成,上下缘有齿,中间填充自体骨,由北京大清生物技术股份有限公司提供。见图 1。
图 1.
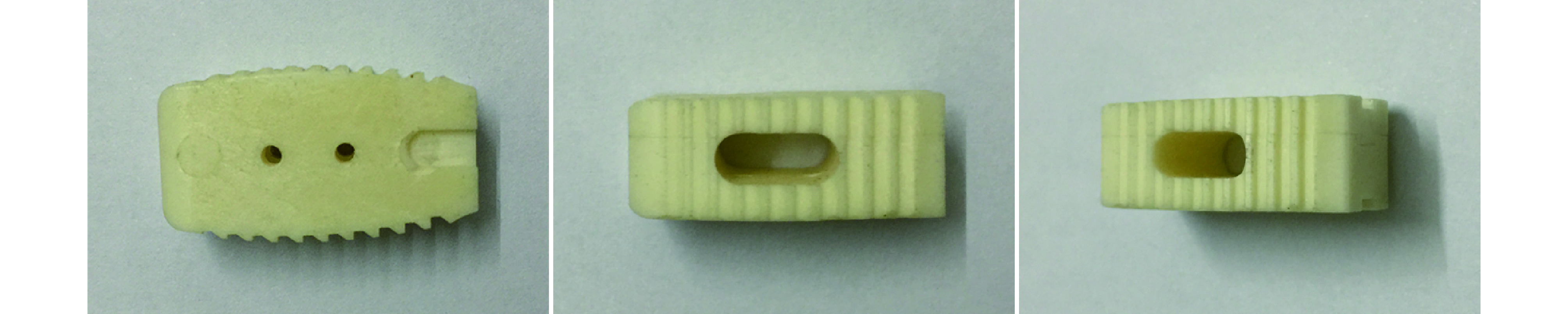
Appearance of allograft bone Cage
同种异体骨 Cage 外观
患者于全麻后取俯卧位,C 臂 X 线机透视下定位病变节段,并于体表标记。取腰部正中切口,切开皮肤后逐层切开皮下组织,重点向两旁剥离。于筋膜层两侧正中旁 2 cm 作切口,小心钝性分离肌肉,经椎旁肌入路(即 Wiltse 入路[10])暴露脊柱,主要是双侧关节突关节。于常规植钉点(横突 1/3 与上关节突外侧交点)两侧植钉,透视可见螺钉位置良好;切除双侧下关节突及部分椎板开窗减压,切除双侧黄韧带,游离神经根后将神经根牵开切除椎间盘,用不同型号的铰刀及刮匙清除残余椎间盘组织。撑开椎间隙后使用合适大小的试模测量椎间隙高度。将自体松质骨填入同型号的同种异体骨 Cage 中,单枚斜行植入椎间隙,适当打压。再次透视可见内固定物及 Cage 位置良好,探查可见双侧神经根游离彻底,硬膜搏动良好,上钛棒及尾帽加压固定。彻底止血冲洗,双侧各放入 1 根负压引流管,逐层关闭切口。
1.4. 术后处理及疗效评价指标
术后常规使用广谱抗生素 3~5 d、小剂量甲泼尼龙及甘露醇 3 d,引流管 2 d 后拔除。所有患者术后逐渐行腰背肌功能锻炼,术后下地活动时佩戴腰围,持续 3 个月,同时要求患者 3 个月内避免腰部负重。
术前,术后 3、6 个月及末次随访时采用疼痛视觉模拟评分(VAS)、Oswestry 功能障碍指数(ODI)[11]和日本骨科协会(JOA)评分评估临床疗效。术后 3、6 个月摄正侧位 X 线片及行 CT 三维重建评估融合率。X 线片标准:① 上下终板间有连续的骨小梁通过;② 过伸过屈位 X 线片上下椎体间位移<3 mm,上下终板夹角变化<5°。CT 三维重建标准:观察 Cage 周围及植入自体骨部位有无连续的骨小梁通过。术前及术后 3 d、3 个月、6 个月分别摄腰椎正侧位 X 线片测量椎间隙高度,即上位椎体下端前后缘连线的中点和下位椎体上缘前后缘连线的中点之间的距离。
1.5. 统计学方法
采用 SPSS21.0 统计软件进行分析。数据以均数±标准差表示,手术前后各时间点间比较采用单因素方差分析,两两比较采用 SNK 检验;检验水准取双侧 α=0.05。
2. 结果
本组患者手术时间 2.1~4.3 h,平均 3.1 h;术中出血量 150~820 mL,平均 407.5 mL。30 例均获随访,随访时间 8~25 个月,平均 16.4 个月。1 例术后 6 个月出现 Cage 下缘碎裂,不伴 Cage 移动,无神经症状;其余患者均无 Cage 脱出、位移、碎裂等情况发生。所有患者均无局部或全身变态反应或感染征象,随访期间无神经压迫、受损症状。30 例患者术后各时间点 VAS 评分、ODI 评分及 JOA 评分均较术前显著改善,差异有统计学意义(P<0.05);术后 6 个月及末次随访时显著优于术后 3 个月(P<0.05);术后 6 个月和末次随访间比较差异无统计学意义(P>0.05)。见表 1。X 线片及 CT 三维重建示,术后 3、6 个月及末次随访时的融合率分别为 55.3%(21/38)、92.1%(35/38)、100%(38/38)。本组患者术前及术后 3 d、3 个月、6 个月、末次随访时的椎间隙高度分别为(9.45±2.54)、(14.15±0.75)、(13.60±1.23)、(12.40±1.57)、(11.40±1.78)mm,术后各时间点椎间隙高度均较术前显著,差异有统计学意义(P<0.05);末次随访时与术后 3 d 比较差异亦有统计学意义(P<0.05),术后其余各时间点间比较差异均无统计学意义(P>0.05)。见图 2。
表 1.
Comparison of effectiveness scores before and after operation (n=30,
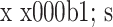 )
)
患者手术前后各时间点各疗效评分比较(n=30,
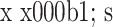 )
)
| 时间
Time |
VAS 评分
VAS score |
ODI 评分
ODI score |
JOA 评分
JOA score |
|
*与术前比较 P<0.05,#与术后 3 个月比较 P<0.05,△与术后 6 个月比较 P<0.05
*Compared with preoperative value, P<0.05;#compared with postoperative value at 3 months, P<0.05;△compared with postoperative value at 6 months, P<0.05 | |||
| 术前
Preoperative |
5.1±1.5#△ | 51.5±10.4#△ | 12.1±5.2#△ |
| 术后 3 个月
Postoperative at 3 months |
2.3±1.1*△ | 25.9± 5.3*△ | 20.6±3.2*△ |
| 术后 6 个月
Postoperative at 6 months |
1.8±0.7*# | 19.3± 5.1*# | 23.7±2.2*# |
| 末次随访
Last follow-up |
1.3±0.8*# | 13.3± 3.0*# | 25.9±2.0*# |
| 统计值
Statistic |
F=14.741
P= 0.001 |
F=5.836
P=0.017 |
F=8.679
P=0.003 |
图 2.
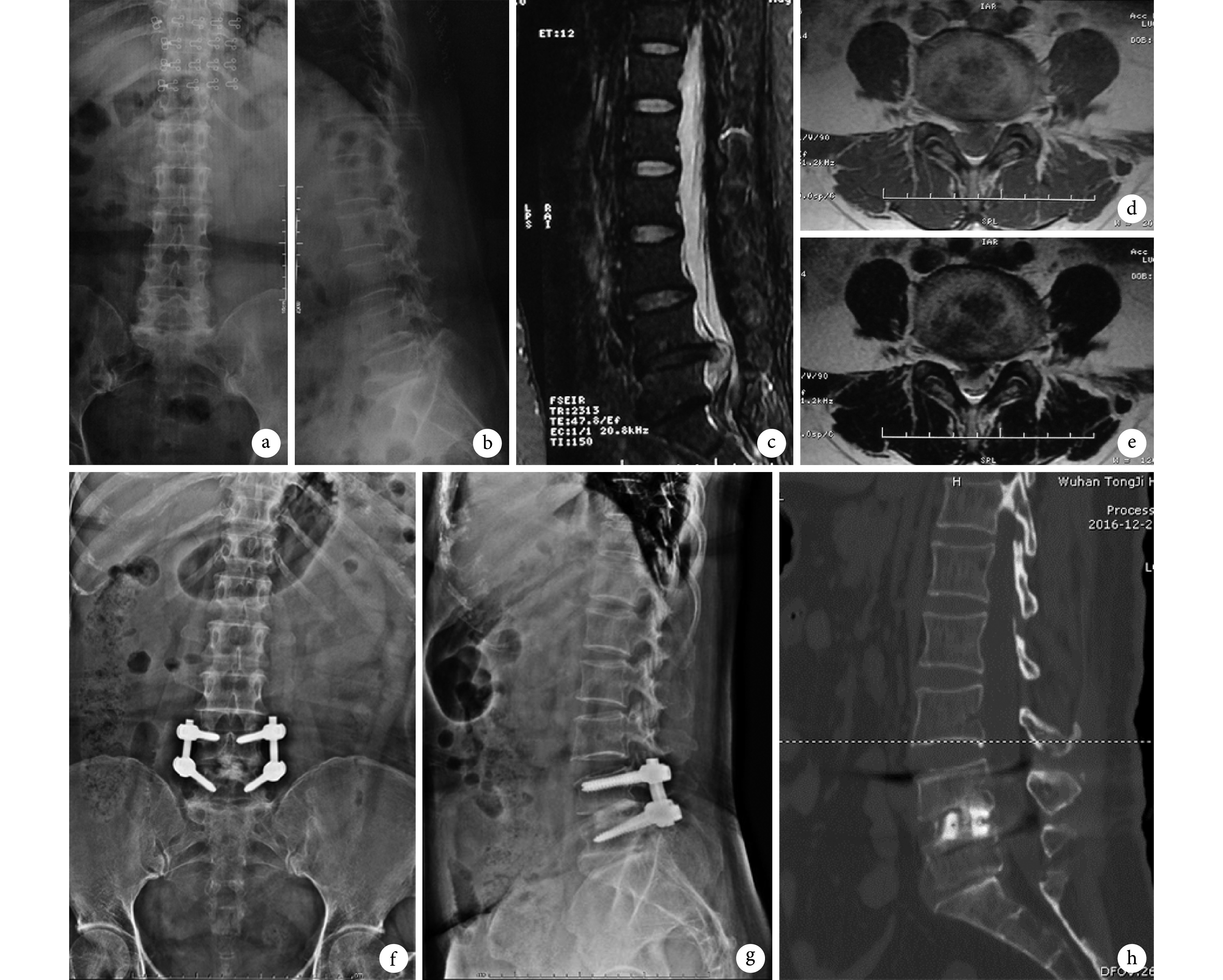
A 53-year-old female patient with lumbar disc herniation at L4, 5 level
患者,女,53 岁,L4、5 腰椎间盘突出症
a、b. 术前正侧位 X 线片;c~e. 术前 MRI 示 L4、5 椎间盘突出;f、g. 术后 6 个月正侧位 X 线片;h. 术后 6 个月 CT 三维重建示连续骨小梁形成
a, b. Anteroposterior and lateral X-ray films before operation; c-e. MRI before operation, showing lumbar disc herniation at L4, 5 level; f, g. Anteroposterior and lateral X-ray films at 6 months after operation; h. CT three-dimensional reconstruction at 6 months after operation, showing continuous trabecular formation
3. 讨论
3.1. 同种异体骨 Cage 的融合效果
本研究对常见的腰椎间盘突出症、腰椎管狭窄症以及腰椎滑脱症患者使用同种异体骨 Cage 行 TLIF 手术,术后 3 个月即有 55.3% 患者骨性融合,6 个月时融合率达 92.1%;患者术后椎间隙显著增高,末次随访时椎间隙高度和术前相比仍有明显增高。Liljenqvist 等[6]进行了一项包含 41 例患者的研究,所有患者均采用 FCA 行 PLIF 融合,术后随访至少 24 个月,平均 30.6 个月,结果显示融合率为 95.2%,影像学显示的平均融合时间为 8.7 个月。Janssen 等[7]对 150 例患者使用了两种不同 Cage,一种是同种异体股骨环移植,用于腰椎前路手术;另一种是用于后路 PLIF 手术的 PLIF 垫片。平均随访 18 个月后结果显示,融合率为 94%,与本研究结果相似,不过这种融合器对椎间隙高度的提高有限,远期椎间隙高度无明显变化。Arnold 等[8]使用一种解剖型 Cage 对 89 例患者(113 个节段)行 PLIF 并用楔形同种异体骨融合。术后 2 年随访显示,融合率达 98%,椎间隙高度相比于术前明显提高,与本研究结果相似。因此,同种异体骨 Cage 能够提供良好的早期融合率,缩短融合时间,同时有助于术后椎间隙高度的提高。
3.2. 同种异体骨 Cage 的安全性
本研究结果显示,30 例患者术后均无神经压迫、受损症状,无局部或全身变态反应或感染征象,随访期间无 Cage 脱出、位移等情况发生。1 例患者术后出现 Cage 下缘碎裂,不伴 Cage 移动,无神经症状。有学者认为该现象是异体骨被爬行替代时旧骨吸收的结果[11]。有研究表明[12],使用同种异体股骨和腓骨环制成的 Cage 有时会发生不同程度的变形(骨折或碎裂),股骨环的概率为 10.8%,腓骨环达 53.2%。股骨 Cage 碎裂较少可能是股骨皮质更厚,且相同密度下强度指数较大的缘故。该研究患者术后同样未再次出现神经压迫或受损症状。
3.3. 同种异体骨 Cage 的优点与不足
优点:① 弹性模量低:钛合金、聚醚醚酮材料、自体髂骨、松质骨的弹性模量分别为 110 Pa、3 600 MPa、1 500 MPa 和 100 MPa[13]。根据应力遮挡理论,过大的弹性模量常会引起周围骨质应力不足,引起应力性骨吸收,使成骨部分骨质疏松。相对于金属 Cage 和聚醚醚酮 Cage,同种异体骨 Cage 弹性模量更接近于正常骨质。② 早期融合率高:同种异体骨 Cage 和金属及聚醚醚酮 Cage 相比,早期融合率更高。金属 Cage 通常需要 12 个月左右达到融合[14-15]。Lied 等[16]进行了一项自体骨及聚醚醚酮 Cage 应用于颈椎前路椎间盘切除融合术(anterior cervical discectomy and fusion,ACDF)手术的对比,两者远期融合率相似。Chiang 等[17]将聚醚醚酮 Cage 用于 ACDF 的研究也得出了相似结果,远期融合率满意。但聚醚醚酮材料在融合速度方面同样慢于同种异体骨,Lee 等[18]报道了使用聚醚醚酮 Cage 用于 PLIF 手术的情况,术后 6 个月融合率为 73.2%,12 个月融合率为 84.5%,均小于同种异体骨 Cage 的早期融合率。③ 增大椎间隙高度:同种异体骨 Cage 可以显著增大术后椎间隙高度,本研究平均随访时间超过 1 年,椎间隙高度相比于术前仍明显提高,无明显 Cage 下沉发生。金属 Cage 下沉率较高,Wang 等[15]的研究中 9 例患者出现 Cage 明显下沉,且下沉超过 3 mm,同时伴颈部疼痛,2 例再次手术。聚醚醚酮材料同样有椎间隙下沉的情况发生,Yang 等[19]关于单枚聚醚醚酮 Cage 在 ACDF 中应用的研究中发现,38 例患者(47 个节段)在随访 5 年后,椎间隙高度均有不同程度下沉,下沉≥2 mm 的有 12 个节段(25.5%),≥3 mm 的有 7 个节段(14.9%)。Kim 等[20]进行的一项关于聚醚醚酮 Cage 下沉的研究显示,104 例患者下沉率为 14.8%(>2 mm),发生于术后(7.2±8.5)个月。
不足:① 刚性较低:本研究中出现 1 例同种异体骨 Cage 下缘碎裂,患者无神经症状,而聚醚醚酮 Cage 很少发生碎裂情况。② 同种异体骨 Cage 材料获得较难,价格较贵。
综上述,同种异体骨 Cage 可以为腰椎 TLIF 手术提供较早期且较高的融合率,能够改善患者的脊柱功能,临床效果良好。但本研究存在样本量少及随访时间不够长等问题,其长期疗效还需要更大样本和更长时间随访来进一步研究。
References
- 1.Costi JJ, Freeman BJ, Elliott DM Intervertebral disc properties: challenges for biodevices. Expert Rev Med Devices. 2011;8(3):357–376. doi: 10.1586/erd.11.1. [DOI] [PubMed] [Google Scholar]
- 2.Snell BE, Maiman DJ Decompression, arthrodesis, and arthroplasty: decision making in the surgical treatment of lumbar disc disease. Clin Neurosurg. 2005;52:271–278. [PubMed] [Google Scholar]
- 3.Humphreys SC, Hodges SD, Patwardhan AG, et al Comparison of posterior and transforaminal approaches to lumbar interbody fusion. Spine (Phila Pa 1976) 2001;26(5):567–571. doi: 10.1097/00007632-200103010-00023. [DOI] [PubMed] [Google Scholar]
- 4.Groth AT, Kuklo TR, Klemme WR, et al Comparison of sagittal contour and posterior disc height following interbody fusion: threaded cylindrical cages versus structural allograft versus vertical cages. J Spinal Disord Tech. 2005;18(4):332–336. doi: 10.1097/01.bsd.0000163037.17634.89. [DOI] [PubMed] [Google Scholar]
- 5.DiPaola CP, Molinari RW Posterior lumbar interbody fusion. J Am Acad Orthop Surg. 2008;16(3):130–139. doi: 10.5435/00124635-200803000-00004. [DOI] [PubMed] [Google Scholar]
- 6.Liljenqvist U, O’Brien JP, Renton P Simultaneous combined anterior and posterior lumbar fusion with femoral cortical allograft. Eur Spine J. 1998;7(2):125–131. doi: 10.1007/s005860050042. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 7.Janssen ME, Lam C, Beckham R Outcomes of allogenic cages in anterior and posterior lumbar interbody fusion. Eur Spine J. 2001;10 Suppl 2:S158–168. doi: 10.1007/s005860100292. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 8.Arnold PM, Robbins S, Paullus W, et al Clinical outcomes of lumbar degenerative disc disease treated with posterior lumbar interbody fusion allograft spacer: a prospective, multicenter trial with 2-year follow-up. Am J Orthop (Belle Mead NJ) 2009;38(7):E115–122. [PubMed] [Google Scholar]
- 9.Sievänen H, Koskue V, Rauhio A, et al Peripheral quantitative computed tomography in human long bones: evaluation of in vitro and in vivo precision . J Bone Miner Res. 1998;13(5):871–882. doi: 10.1359/jbmr.1998.13.5.871. [DOI] [PubMed] [Google Scholar]
- 10.Oh HS, Shim CS, Kim JS, et al Clinical and radiological comparison of femur and fibular allografts for the treatment of cervical degenerative disc diseases. J Korean Neurosurg Soc. 2013;53(1):6–12. doi: 10.3340/jkns.2013.53.1.6. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 11.Fairbank JC, Couper J, Davies JB, et al The oswestry low back pain disability questionnaire. Physiotherapy. 1980;66(8):271–273. [PubMed] [Google Scholar]
- 12.Kayanja M, Orr RD Incidence and outcome of graft resorption in anterior lumbar interbody fusion: using femoral ring allograft s and recombinant human bone morphogenetic protein-2. Spine (Phila Pa 1976) 2014;39(5):374–380. doi: 10.1097/BRS.0000000000000145. [DOI] [PubMed] [Google Scholar]
- 13.Xiao Z, Wang L, Gong H, et al Biomechanical evaluation of three surgical scenarios of posterior lumbar interbody fusion by finite element analysis. Biomed Eng Online. 2012;11:31. doi: 10.1186/1475-925X-11-31. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 14.Kolstad F, Nygaard ØP, Andresen H, et al Anterior cervical arthrodesis using a standalone cylindrical titanium cage. Spine (Phila Pa 1976) 2010;35(16):1545–1550. doi: 10.1097/BRS.0b013e3181d259c1. [DOI] [PubMed] [Google Scholar]
- 15.Wang X, Chen Y, Chen D, et al Anterior decompression and interbody fusion with BAK/C for cervical disc degenerative disorders. J Spinal Disord Tech. 2009;22(4):240–245. doi: 10.1097/BSD.0b013e31816d5f7e. [DOI] [PubMed] [Google Scholar]
- 16.Lied B, Roenning PA, Sundseth J, et al Anterior cervical discectomy with fusion in patients with cervical disc degeneration: a prospective outcome study of 258 patients (181 fused with autologous bone graft and 77 fused with a PEEK cage) BMC Surg. 2010;10:10. doi: 10.1186/1471-2482-10-10. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 17.Chiang CJ, Kuo YJ, Chiang YF, et al Anterior cervical fusion using a polyetheretherketone cage containing bovine xenograftpthree to five-year follow-up. Spine (Phila Pa 1976) 2028;33(23):2524–2428. doi: 10.1097/BRS.0b013e318185289c. [DOI] [PubMed] [Google Scholar]
- 18.Lee JH, Lee JH, Park JW, et al Fusion rates of a morselized local bone graft in polyetheretherketone cages in posterior lumbar interbody fusion by quantitative analysis using consecutive three-dimensional computed tomography scans. Spine J. 2011;11(7):647–653. doi: 10.1016/j.spinee.2011.04.029. [DOI] [PubMed] [Google Scholar]
- 19.Yang JJ, Yu CH, Chang BS, et al Subsidence and nonunion after anterior cervical interbody fusion using a stand-alone polyetheretherketone (PEEK) cage. Clin Orthop Surg. 2011;3(1):16–23. doi: 10.4055/cios.2011.3.1.16. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 20.Kim MC, Chuang HT, Cho JL, et al Subsidence of polyetheretherketone cage after minimally invasive transforaminal lumbar interbody fusion. J Spinal Disord Tech. 2013;26(2):87–92. doi: 10.1097/BSD.0b013e318237b9b1. [DOI] [PubMed] [Google Scholar]


