Abstract
Antivirale Medikamente hemmen die Virusvermehrung durch Interaktion mit spezifischen Angriffspunkten im viralen Replikationszyklus. Direkt antivirale Wirkstoffe haben die therapeutischen Möglichkeiten bei chronischen Infektionen mit dem humanen Immundefizienz- (HIV), Hepatitis-B- (HBV) und Hepatitis-C-Virus (HCV) revolutioniert. Fortlaufende pharmakologische Entwicklungen sorgen auch bei Erkrankungen durch Herpesviren für verbesserte therapeutische und prophylaktische Möglichkeiten, was insbesondere immunsupprimierten Patienten zugutekommt. Während Infektionen mit persistierenden Viren wie HIV, HBV oder Herpesviren vom Grundsatz her bislang nicht heilbar sind, können Erreger von akuten Virusinfektionen vollständig eliminiert werden. Akute Infektionen, wie Influenza oder „coronavirus disease 2019“ (COVID-19) weisen durch ihre pathophysiologische Dynamik jedoch schmale therapeutische Zeitfenster für antivirale Therapieansätze auf. Der ideale Therapiezeitpunkt liegt hier unmittelbar nach der Virusexposition, was die Anwendung in der Praxis häufig limitiert. Eine effektive antivirale Prä- oder Postexpositionsprophylaxe hat sich bei Infektionen mit HIV und Influenza A/B etabliert und gewinnt aktuell auch bei Infektionen mit dem „severe acute respiratory syndrome coronavirus 2“ (SARS-CoV‑2) an Bedeutung.
Schlüsselwörter: Virusinfektionen, Virustatika, Virusreplikation, Postexpositionsprophylaxe, COVID-19
Abstract
Antiviral drugs inhibit viral replication by interaction with specific elements of the viral replication cycle. Directly acting antiviral agents have revolutionized the therapeutic options for chronic infections with human immunodeficiency virus (HIV), hepatitis B virus (HBV) and hepatitis C virus (HCV). Pharmacological developments constantly improve therapeutic and prophylactic options for diseases caused by herpes viruses, which is of particular relevance for immunocompromised patients. While infections with persistent viruses, such as HIV, HBV or herpes viruses principally so far cannot be cured, complete elimination of viruses that cause acute infections is possible; however, acute infections, such as influenza or coronavirus disease 2019 (COVID-19) offer only a small therapeutic window for antiviral strategies due to their pathophysiological dynamics. The optimal time point for antiviral agents is immediately after exposure to the virus, which frequently limits its application in practice. An effective pre-exposure or postexposure prophylaxis has been established for infections with HIV and influenza A/B and also gains relevance for infections with severe acute respiratory syndrome coronavirus 2 (SARS-CoV-2).
Keywords: Viral infections, Virustatics, Virus replication, Post-exposure prophylaxis, COVID-19
Antiviral wirksame Medikamente werden zu Behandlung, Therapie und Prophylaxe von Viruserkrankungen eingesetzt. Direkt antiviral wirksame Medikamente („directly acting antivirals“, DAA) greifen virale Zielstrukturen an und damit in den viralen Vermehrungszyklus ein, wodurch die Bildung neuer Viruspartikel gehemmt wird. Da Viren über keinen eigenen Stoffwechsel verfügen, sondern darauf angewiesen sind, von Zellen „vermehrt zu werden“, kommen alternativ indirekt antiviral wirksame Substanzen zum Einsatz, die z. B. die Virusabwehr stärken oder zelluläre, für das Virus essenzielle Enzyme inhibieren.
Antivirale Angriffspunkte
Die Mehrheit der antiviralen Wirkstoffe setzt an Schlüsselproteinen des viralen Replikationszyklus an, wobei neben der Pharmakokinetik die Selektivität der Substanz bezogen auf spezifische Erreger eine entscheidende Rolle für die Wirksamkeit und die therapeutische Breite spielt. Da sich der Replikationszyklus in Abhängigkeit von der Genomstruktur (RNA- oder DNA-Genom) und der Hülle der Viren deutlich unterscheidet, kommen unterschiedliche antivirale Substanzklassen zum Einsatz. In Deutschland zugelassene antivirale Wirkstoffe, aufgegliedert nach ihrem Ansatzpunkt im viralen Replikationszyklus, und ihre klinischen Indikationen, sind in Tab. 1 aufgeführt.
| Angriffspunkt im viralen Replikationszyklus | Wirkmechanismus/Target | Wirkstoffe (Verabreichungsform) | Indikationena |
|---|---|---|---|
|
Zelleintritt (Bindung und Fusion) |
Verhinderung der Adhäsion von CCR5-tropen HI-Viren | Maraviroc (p.o.) | HIV-1-Infektionen mit CCR5-Tropismus bei bereits vorbehandelten Patienten in Kombination mit anderen Wirkstoffen |
| HBsAg-Derivat | Bulevirtid (s.c.) | Chronische HDV-Infektion | |
| Monoklonale neutralisierende Antikörper gegen die rezeptorbindende Domäne (RBD) des SARS-CoV‑2 Spike-Proteins | Casirivimab/Imdevimab (i.v./s.c.) | Therapie und Prophylaxe von COVID-19 bei Patienten ab 12 Jahren, die keine Sauerstofftherapie benötigen | |
| Intrazelluläre Verarbeitung | Störung des viralen „uncoating“ durch Blockierung des M2-Ionenkanals | Amantadin (p.o./i.v.) | Therapie und Prophylaxe von Infektionen mit Influenza A Viren (aufgrund von Resistenzbildung nicht mehr empfohlen) |
| Inhibition der HCV-NS3/4A-Protease | Grazoprevir (p.o.) | Chronische HCV-Infektion (in Kombination mit anderen Wirkstoffen) | |
| Paritaprevir (p.o.) | |||
| Boceprevir (p.o.) | |||
| Telaprevir (p.o.) | |||
| Asunaprevir (p.o.) | |||
| Simeprevir (p.o.) | |||
| Voxilaprevir (p.o.) | |||
| Inhibition des HCV-NS5A-Replikationskomplexes | Daclatasvir (p.o.) | ||
| Elbasvir (p.o.) | |||
| Ledipasvir (p.o.) | |||
| Ombitasvir (p.o.) | |||
| Velpatasvir (p.o.) | |||
| Pibrentasvir (p.o.) | |||
|
Genomreplikation: RNA-abhängige RNA-Polymerase (RNA-Viren) |
Nukleosidanalogon mit Spezifizität für HCV-NS5B | Ribavirin (p.o.) | |
| Nukleotidanalogon mit Spezifizität für HCV-NS5B | Sofosbuvir (p.o.) | ||
| Nichtnukleosidische Inhibition von HCV-NS5B | Dasabuvir (p.o.) | ||
| Nukleosidanalogon mit Spezifizität für RNA-abhängige RNA-Polymerase NSP12 | Remdesivir (i.v.) | COVID-19-Pneumonie mit Sauerstoffbedarf (bedingte Marktzulassung) | |
| Inhibition der Endonukleaseaktivität des Influenza-Polymerase-Komplexes | Baloxavir marboxil (p.o.) | Therapie und Postexpositionsprophylaxe von Infektionen mit Influenza-A/B-Viren | |
|
Genomreplikation: DNA-Polymerase (DNA-Viren) |
Nukleos(t)idanaloga mit Spezifizität für DNA-Polymerasen | Aciclovir (p.o./i.v.) | HSV-Infektionen, Herpes-Zoster-Virus (VZV), Prophylaxe von rezidivierendem Herpes genitalis (HSV) bei Immunsuppression |
| Valaciclovir (p.o.) | HSV-Infektionen; Herpes Zoster-Virus (VZV); Prophylaxe von rezidivierendem Herpes genitalis (HSV); Prophylaxe von CMV-Reaktivierung bei Immunsuppression | ||
| Famciclovir (p.o.) | Herpes-Zoster-Virus (VZV); Herpes genitalis (HSV) | ||
| Brivudin (p.o.) | Herpes-Zoster-Virus (VZV, frühes Stadium) bei immunkompetenten Personen | ||
| Ganciclovir (i.v.) | CMV-Erkrankung bei Immunsuppression | ||
| Valganciclovir (p.o.) | CMV-Retinitis bei Immunsuppression; Prophylaxe einer CMV-Erkrankung bei Organtransplantation | ||
| Cidofovir (i.v.) | Therapie der CMV-Retinitis bei Aids, wenn andere Arzneimittel als ungeeignet erachtet werden | ||
| Pyrophosphatanaloga (Wirksamkeit nicht auf DNA-Polymerasen beschränkt) | Foscarnet (i.v.) | Therapie von CMV-Infektionen bei Patienten mit Aids; Therapie von mukokutanen HSV-Infektionen bei immungeschwächten Patienten, die klinisch nicht auf Aciclovir ansprechen | |
|
Genomreplikation: reverse Transkriptase (Retroviren) |
Nukleosid‑/Nukleotidanaloga mit Spezifizität für retrovirale reverse Transkriptase (N(t)RTI) | Entecavir (p.o.) | Chronische HBV-Infektion |
| Tenofovir (‑disoproxil/-alafenamid; p.o.) | HIV (in Kombination); chronische HBV-Infektion | ||
| Lamivudin (p.o.) | |||
| Emtricitabin (p.o.) | HIV-Infektion (in Kombination mit Virostatika aus anderen Klassen) | ||
| Abacavir (p.o.) | |||
| Nichtnukleosidische Inhibition der HIV-Reverse-Transkriptase (NNRTI) | Rilpivirin (p.o./i.m.) | ||
| Doravirin (p.o.) | |||
| Integration der viralen DNA (Retroviren) | Inhibition der HIV-Integrase (INI) | Dolutegravir (p.o.) | |
| Raltegravir (p.o.) | |||
| Bictegravir (p.o.) | |||
| Cabotegravir (p.o./i.m.) | |||
|
Zusammenbau („assembly “) und Reifung |
Inhibition des CMV-Terminase-Komplexes | Letermovir (p.o./i.v.) | Prophylaxe von CMV-Reaktivierung bei CMV-seropositiven Empfängern einer allogenen hämatopoetischen Stammzelltransplantation |
| Inhibition von HIV-Proteasen (PI) | Darunavir + Ritonavir oder Cobicistat (p.o.) | HIV-Infektion (in Kombination mit Virostatika aus anderen Klassen) | |
| Atazanavir + Ritonavir oder Cobicistat (p.o.) | |||
| Lopinavir (p.o.) | |||
| Freisetzung neuer Viria („release“) | Inhibition der viralen Neuraminidase | Oseltamivir (p.o.) | Therapie bei influenzatypischen Symptomen und Infektionsvorkommen in der Bevölkerung; Prophylaxe und Postexpositionsprophylaxe |
| Zanamivir (p.o./i.v.) | Therapie und Prophylaxe von Infektionen mit Influenza A/B |
CCR5 C-C-Motiv-Chemokin-Rezeptor 5, CMV Zytomegalievirus, COVID-19 „coronavirus disease 2019“, HBsAg „hepatitis B surface antigen“, HBV Hepatitis-B-Virus, HCV Hepatitis-C-Virus, HIV humanes Immundefizienzvirus, HSV Herpes-simplex-Virus, M2 Matrixprotein 2, NS „nonstructural protein“, NSP „nonstructural polymerase“, VZV Varizella-Zoster-Virus
a Kein Anspruch auf Vollständigkeit der Angaben, bitte jeweilige Fachinformation beachten
Therapiekonzepte
Suppressive Therapie
Chronische Infektionen mit persistierenden Viren wie dem humanen Immundefizienzvirus (HIV), dem Hepatitis-B-Virus (HBV) oder Herpesviren sind mit verfügbaren antiviralen Medikamenten nicht restlos heilbar. Sie etablieren Persistenzformen im Kern infizierter Zellen und persistieren auch, ohne sich zu vermehren. Das HIV integriert sich in das Wirtsgenom; Herpesviren und HBV etablieren ein stabiles Episom im Zellkern. Das Immunsystem ist unter normalen Umständen in der Lage, Infektionen mit Herpesviren zu kontrollieren. Eine sequenzielle Suppressionstherapie ist nur dann notwendig, wenn die Immunkontrolle therapiebedingt oder situativ nicht mehr ausreicht. Eine HIV-Infektion und eine chronische HBV-Infektion erfordern hingegen eine kontinuierliche Therapie.
Einige Viren etablieren Persistenzformen im Kern infizierter Zellen, die nur sehr schwer angreifbar sind
Eine adäquate antivirale Therapie hat positiven Einfluss auf den Krankheitsverlauf und die Infektiosität. Eine permanente Suppression wird auch als funktionelle Heilung bezeichnet. Eine langfristige oder wiederholte Wirkstoffexposition birgt jedoch aufgrund des Selektionsdrucks das Risiko einer Resistenzbildung. Die Wahrscheinlichkeit, dass resistente Virusvarianten sich durchsetzen, ist jedoch für verschiedene Viren und Substanzklassen unterschiedlich und kann nicht pauschal beziffert werden.
Eradizierende, kurative Therapie
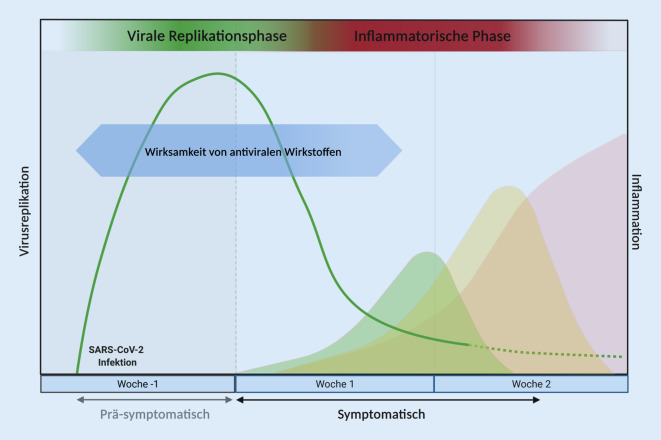
Eine vollständige Viruselimination ist grundsätzlich bei Viren möglich, die keine Persistenzform ausbilden, wie Erreger viraler Atemwegsinfektionen oder dem Hepatitis C‑Virus (HCV). Diese Viren müssen replizieren, um im Wirt persistieren zu können, sodass eine effiziente Hemmung der Replikation über einen gewissen Zeitraum mit einer vollständigen Heilung einhergehen kann. Akute Infektionen, z. B. durch das „severe acute respiratory syndrome coronavirus 2“ (SARS-CoV‑2), sind durch eine Phase der exponentiell ansteigenden Virusvermehrung geprägt, die mit dem Einsetzen der Immunantwort jedoch rasch zurückgeht (Abb. 1). Da der Höhepunkt der Virusproduktion typischerweise bei Symptombeginn bereits überschritten ist, ist das vielversprechendste therapeutische Zeitfenster auf die prodromale oder frühe symptomatische Phase beschränkt. Die höchste Wirksamkeit ist vor dem Auftreten von ersten Symptomen und damit der Diagnosestellung zu erwarten, wodurch der Einsatz in der Praxis häufig limitiert ist.
Primär- oder Sekundärprophylaxe
Ein frühzeitiger Einsatz von antiviralen Medikamenten oder neutralisierenden Antikörpern vor oder unmittelbar nach einer Virusexposition kann manifeste Infektionen und akute Infektionsverläufe verhindern, da die Virusvermehrung bereits im Keim erstickt wird. Die hocheffektive antivirale Prä- oder Postexpositionsprophylaxe hat sich z. B. für Infektionen mit HBV, HIV oder Influenza etabliert. Neutralisierende Antikörper werden bereits zur Prä- und Postexpositionsprophylaxe bei der „coronavirus disease 2019“ (COVID-19) verwendet.
Therapeutische Optionen bei bestimmten Virusinfektionen
Humanes-Immundefizienzvirus-Infektion
Eine adäquate antiretrovirale Therapie (ART) geht inzwischen mit einer annähernd normalen Lebenserwartung bei HIV-Infektionen einher. In Studien geprüfte Wirkstoffkombinationen von mindestens 2 Einzelsubstanzen erreichen bei kontinuierlicher Einnahme eine dauerhafte virale Suppression. Negative Folgen der Infektion auf das Immunsystem, insbesondere die sukzessive Zerstörung von CD4-positiven T‑Lymphozyten und damit einhergehende opportunistische Infektionen, können dadurch verhindert werden. Gleichzeitig wird die Übertragung auf andere Personen verhindert, sodass die ART eine wichtige Komponente zur Eindämmung der Epidemie darstellt. Eine Ansteckung mit HIV kann ebenfalls durch eine Prä- oder Postexpositionsprophylaxe verhindert werden, wenn die zeitlichen Rahmenbedingungen dafür eingehalten werden [2, 3]. Voraussetzungen für ein weitgehend unbeeinträchtigtes Leben mit HIV-Infektion sind eine frühzeitige Diagnosestellung und konsequente Dauertherapie [29]. Hierzu stehen verschiedene Wirkstoffklassen zur Verfügung (Tab. 1).
Frühzeitige Diagnose und konsequente Dauertherapie sichern ein fast normales Leben HIV-Infizierter
Die aktuell empfohlene Erstlinientherapie für nichtvorbehandelte Patienten besteht aus der Kombination von 2 nukleos(t)idischen Reverse-Transkriptase-Inhibitoren (N(t)RTI), Tenofoviralafenamid + Emtricitabin, dem generisch verfügbaren Tenofovirdisoproxil + Emtricitabin oder Abacavir plus Lamivudin, mit einem Integraseinhibitor wie Dolutegravir, Bictegravir oder Raltegravir [11, 15]. Vor der Anwendung von Abacavir muss aufgrund des Risikos für lebensgefährliche Hypersensitivitätsreaktionen das Vorliegen einer HLA-B*5701-Konstellation ausgeschlossen werden. Klinisch bedeutsam ist die Wirksamkeit von Tenofovir und Lamivudin gegen Hepatitis B, die bei HIV/HBV-Koinfektionen relevant ist. Die N(t)RTI sind Nukleotid‑/Nukleosidanaloga (NA), die aufgrund der strukturellen Ähnlichkeit mit dem natürlichen Substrat während der Transkription von einzelsträngiger viraler RNA kompetitiv in eine doppelsträngige DNA eingebaut werden und eine Hemmung der HIV-Reverse-Transkriptase bewirken. Integraseinhibitoren verhindern die Integration proviraler DNA in das humane Genom. Sie gehören zu den antiretroviralen Substanzen mit der höchsten Wirksamkeit und zeichnen sich durch eine hohe Resistenzbarriere aus [8, 10, 15, 31]. Für nichtvorbehandelte Patienten mit niedriger Viruslast wird mit der Kombination aus Lamivudin und Dolutegravir nun erstmalig eine Therapie bestehend aus nur 2 Wirkstoffen zur Erstlinientherapie empfohlen [15].
Alternativ können Kombinationen aus 2 N(t)RTI mit einem nichtnukleosidischen Reverse-Transkriptase-Inhibitor (NNRTI) wie Doravirin oder einem Proteaseinhibitor (PI) wie Darunavir eingesetzt werden [11, 15]. Der Wirkmechanismus von NNRTI ähnelt grundsätzlich dem der NRTI. Sie hemmen die HIV-Reverse-Transkriptase, binden jedoch nichtkompetitiv an das Enzym in der Nähe der Substratbindungsstelle für Nukleoside. Die PI hemmen die Translation viraler DNA, wodurch die Bildung viraler Proteine verhindert wird, die für die Entstehung neuer HIV-Viria erforderlich sind. Sie weisen eine ähnliche Wirksamkeit und Resistenzbarriere auf wie Integraseinhibitoren, haben jedoch den Nachteil, dass die simultane Einnahme eines Zytochrom-P3A(CYP3A)-Inhibitors als pharmakologischer Booster erforderlich ist. Die Interaktion der als Booster verwendeten Wirkstoffe Ritonavir und Cobicistat mit CYP3A sowie weiteren CYP-Isoenzymen macht die Therapie anfällig für Wechselwirkungen mit anderen Medikamenten und kann die Verträglichkeit beeinträchtigen. Für die meisten empfohlenen Therapieregime sind heute Fixkombinationen zur einmal täglichen Einnahme verfügbar.
Hepatitis-B- und Hepatitis-D-Virus-Infektion
Der Ausgang einer Infektion mit HBV ist stark altersabhängig. Infektionen bei Jugendlichen oder Erwachsenen gehen bei etwa 30 % mit einer akuten Virushepatitis einher, die nur selten fulminant ist. In diesem Alter kontrolliert das Immunsystem die Infektion; sie „heilt aus“, obwohl noch Spuren viraler DNA verbleiben, die bei Immunsuppression zur Reaktivierung der Infektion führen können [30]. Bei Immunsupprimierten und Kindern kann eine Viruspersistenz eintreten, die ausgehend von viralen DNA-Anteilen im Zellkern der Hepatozyten durch eine anhaltende Sekretion des „hepatitis B surface antigen“ (HBsAg) gekennzeichnet ist und eine chronische Hepatitis zur Folge haben kann. Bei Neugeborenen oder kleinen Kindern kommt es in den meisten Fällen zur Ausbildung einer typischerweise asymptomatischen chronischen Infektion und konsekutiver Leberschädigung, die langfristig das Risiko eines hepatozellulären Karzinoms birgt [37]. Zur Prävention einer HBV-Infektion und einer Superinfektion mit dem Hepatitis-Delta-Virus (HDV) steht eine wirksame prophylaktische Impfung zur Verfügung.
Zur antiviralen Therapie stehen die NA Entecavir und Tenofovir zur Verfügung sowie das unspezifisch antiviral wirkende pegylierte Interferon‑α (pegIFNα). Akute HBV-Infektionen bedürfen regelhaft keiner antiviralen Therapie. Im Fall der fulminanten Hepatitis mit Lebersynthesestörung muss schnellstmöglich eine Therapie mit NA und eine engmaschige Überwachung erfolgen, um ein Leberversagen zu verhindern [21].
Die Therapieindikation bei chronischer HBV-Infektion ist abhängig vom Virustiter und dem Ausmaß der Leberschädigung. Bei Patienten mit Leberzirrhose und nachweisbarer HBV-DNA wird eine Therapie generell empfohlen. Dies gilt ebenso für Patienten mit einer Viruslast > 2000 IU/ml und einer erhöhten Alanin-Aminotransferase(ALT)-Konzentration und/oder nachgewiesener Leberfibrose [6]. Die bevorzugte Behandlung besteht aus einer Monotherapie mit Tenofovir oder Entecavir. Lamivudin wird aufgrund seiner vergleichsweise niedrigen Resistenzbarriere kaum mehr eingesetzt. Die antivirale Therapie führt bei einem Großteil der Patienten zu einer anhaltenden Suppression der Virusreplikation, kann die Infektion aber nicht restlos heilen. Je nach Status des HBe-Antigens (HBeAg) und Therapieverlauf (Dauer der viralen Suppression, Entwicklung von zu Anti-HBe-Antikörpern, Verlust des HBsAg) ist eine Beendigung der Suppressionstherapie möglich. Insbesondere bei der chronischen HBeAg-negativen HBV-Infektion besteht jedoch ein hohes Risiko für ein Relapse mit einem Schub der Hepatitis und muss deshalb unter strenger Kontrolle durchgeführt werden. Ein kontrolliertes Wiederaufflammen der Entzündung nach NA-Therapie kann zur Verschlechterung der Leberfunktion, aber auch zu einer anhaltenden Kontrolle der Infektion führen [42]. Dies zeigt, dass eine Immunstimulation nach längerer Suppressionstherapie eine Möglichkeit bietet, die Infektion doch noch auszuheilen. Aktuell sind deshalb zahlreiche potenziell kurative Therapieansätze in der Entwicklung, wobei das Immunsystem unspezifisch (z. B. durch die Aktivierung von Mustererkennungsrezeptoren) oder HBV-spezifisch, z. B. durch eine therapeutische Impfung, stimuliert wird [17].
Auch bei günstigem Verlauf der Infektion besteht lebenslang ein gewisses Risiko einer HBV-Reaktivierung, insbesondere im Fall einer Immunsuppression. Einer Reaktivierung während immunsuppressiven Therapien kann durch eine prophylaktische Einnahme von NA vorgebeugt werden [36].
Therapien mit dem nebenwirkungsreichen pegIFNα werden heute nur noch selten angewendet, wie z. B. bei einer Koinfektion mit HDV. Die Replikation des HDV ist nicht durch NA beeinflussbar, sodass im Falle einer HBV/HDV-Koinfektion zusätzlich zur Therapie der HBV-Infektion eine 48-wöchige Therapie mit pegIFNα empfohlen wird [6]. Die Herstellung von pegIFNα wird aufgrund eines Marktrückzugs voraussichtlich bis Ende 2022 eingestellt. Damit entfällt die Möglichkeit einer immunstimulatorischen Therapie. Im Jahr 2020 wurde mit dem Entry-Inhibitor Bulevirtid jedoch ein neues Virostatikum zur Therapie der chronischen HDV-Infektion zugelassen. Bulevirtid ist ein Peptid aus der Bindedomäne des Hüllproteins, das HBV und HDV teilen, und verhindert die Bindung neuer HBV- und HDV-Virionen an den Eintritts-Rezeptor, das Natriumtaurocholat-kotransportierendes Polypeptid (NTCP).
Chronische Hepatitis C
Infektionen mit dem Hepatitis-C-Virus (HCV) können persistieren und mit einer chronischen Virushepatitis einhergehen. Im Gegensatz zur Vermehrung von HBV findet die virale Replikation ausschließlich im Zytoplasma statt, ohne dass sich eine virale Persistenzform etabliert. Eine Viruspersistenz setzt daher eine kontinuierliche Replikation voraus [33], wodurch eine vollständige Ausheilung der Infektion („sustained viral response“, SVR) durch antivirale Therapien, die die Virus-Replikation effizient unterdrücken, ermöglicht wird. Seit der Zulassung HCV-spezifischer antiviraler Wirkstoffe, der „directly acting antivirals“ (DAA), können mit zeitlich begrenzten und gut verträglichen Therapien Heilungsraten bis zu 100 % erreicht werden. Die ersten antiviralen Medikamente dieser Art waren Boceprevir und Telaprevir, Hemmer der Protease „nonstructural protein 3/4A“ (NS3/4A) und etwas später Sofosbuvir, ein spezifischer und hochwirksamer, nukleotidischer Hemmer der RNA-abhängigen RNA-Polymerase NS5B, d. h. des Enzyms, was für die Virusvermehrung essentiell ist. Es kamen weitere NS3/4A-Inhibitoren, der nichtnukleosidische NS5B-Polymerase-Inhibitor Dasabuvir sowie Inhibitoren der NS5A-Polymerase hinzu. Eine vollständige Auflistung verfügbarer Wirkstoffe findet sich in Tab. 1.
Die Therapie erfolgt durch Kombinationspräparate mit zwei oder drei Wirkstoffen unterschiedlicher Klassen über einen Zeitraum von 6 bis 12 Wochen. Die geeignetste Therapie wird in Abhängigkeit von Komorbiditäten, Komedikation, dem Ausmaß der Leberschädigung und dem HCV-Genotyp gewählt. Durch die Verfügbarkeit von pangenomisch, breit wirksamen Regimen wie Sofosbuvir/Velpatasvir oder Glecaprevir/Pibrentasvir ist eine Bestimmung des HCV-Genotyps vor der Therapieeinleitung bei therapienaiven Patienten heute prinzipiell verzichtbar [4, 46].
Herpesvirusinfektionen
Infektionen mit den humanpathogenen Herpesviren verursachen eine Vielzahl von Erkrankungen. Allen Herpesviren gemeinsam sind eine hohe Durchseuchungsrate in der Bevölkerung und die Fähigkeit zur lebenslangen, latenten Persistenz nach der Erstinfektion [23]. Eine eradizierende Therapie für Infektionen mit Herpesviren ist bislang nicht bekannt, sodass sequenzielle und/oder prophylaktische antivirale Suppressionstherapien oder eine Impfung im Vordergrund stehen.
Herpes-simplex-Virus 1 und 2
Erstinfektionen mit Herpes-simplex-Virus(HSV) 1 und 2 verlaufen häufig asymptomatisch. Die meisten Erwachsenen sind latent mit HSV infiziert; bei etwa einem Drittel kommt es zu rezidivierenden, symptomatischen Reaktivierungen mit Bläschenbildung auf Haut oder Schleimhäuten. Schwere Komplikationen, wie eine HSV-Pneumonie, können v. a. bei immunsupprimierten Patienten auftreten. Besonders gefürchtet ist die HSV-Enzephalitis, die eine hohe Letalität aufweist. Als antivirales Medikament ist Aciclovir seit seiner Entdeckung in den 1970er-Jahren weiterhin die erste Wahl bei therapiebedürftigen HSV-Infektionen [14]. Aciclovir ist ein NA mit relativ hoher selektiver Wirkung auf infizierte Zellen, da es erst durch virale Kinasen aktiviert und in virale DNA eingebaut wird. Aufgrund seiner schlechten oralen Bioverfügbarkeit werden schwere Krankheitsbilder ausschließlich i.v. behandelt. Bei einer oralen Verabreichung im Rahmen leichter Infektionen müssen hohe Dosen über den Tag verteilt eingenommen werden.
Valaciclovir ist ein orales Pro-Drug mit verbesserter oraler Bioverfügbarkeit. Ein frühzeitiger Therapiebeginn mit (Val‑)Aciclovir kann den Verlauf von symptomatischen Erstinfektionen oder Reaktivierungen abmildern. Insbesondere bei hohen i.v.-Dosen können allerdings Nephro- und Neurotoxizitäten auftreten. Famciclovir ist ein orales Pro-Drug des chemisch mit Aciclovir verwandten Penciclovir und ist in Deutschland ausschließlich zur Therapie des Herpes genitalis und Herpes zoster (s. unten) zugelassen. Als Reservemedikament zur Behandlung von mukokutanen HSV-Infektionen bei immungeschwächten Patienten kann Foscarnet eingesetzt werden, ein Pyrophosphatanalogon, das sowohl virale DNA-Polymerasen als auch reverse Transkriptasen hemmt.
Varizella-Zoster-Virus
Erstinfektion mit dem Varizella-Zoster-Virus (VZV) im Kindesalter verursachen Windpocken (Varizellen), Reaktivierungen bei erwachsenen Personen Herpes zoster, der sich je nach beteiligten Nervenganglien segmental oder auch ausgedehnter manifestieren und sogar zu schweren Enzephalitiden führen kann. Das Risiko einer Reaktivierung steigt mit zunehmendem Alter und betrifft in Deutschland bis zu 25 % der Bevölkerung über 60 Jahre [8, 20]. Da VZV zuvor meist erfolgreich durch das Immunsystem kontrolliert wird, wird eine Impfung ab einem Alter von 60 Jahren empfohlen, um die Immunkontrolle zu reaktivieren. In seltenen Fällen, insbesondere bei immunsupprimierten Patienten, können schwerwiegende Komplikationen wie eine Varizellenpneumonie, ein disseminierter Herpes zoster und/oder Manifestationen im Zentralnervensystem (ZNS) auftreten.
Die Therapie der Windpocken bei immunkompetenten Patienten erfolgt symptomatisch. Zur antiviralen Therapie des Herpes zoster oder komplizierter Infektionen stehen i.v. oder oral zu verabreichendes Aciclovir sowie oral zu verabreichendes Valaciclovir, Famciclovir oder Brivudin zur Verfügung. Brivudin ist ebenfalls ein orales NA-Pro-Drug und ist ausschließlich für die Therapie des Herpes zoster im Anfangsstadium bei immunkompetenten Erwachsenen zugelassen. Eine frühzeitige antivirale Therapie des Herpes zoster innerhalb der ersten 2 bis 3 Tage nach Symptombeginn kann den weiteren Verlauf der Erkrankung günstig beeinflussen. Die Therapie von VZV-Reaktivierungen bei immunsupprimierten Patienten sollte i.v. mit Aciclovir erfolgen.
Zytomegalievirus
Akute Zytomegalievirus(CMV)-Infektionen verlaufen meistens asymptomatisch, können jedoch ein mononukleose-ähnliches Krankheitsbild verursachen. Klinisch relevant sind Reaktivierungen und Infektionen während der Schwangerschaft, die zu fetalen Missbildungen führen können. Schwere Verlaufsformen treten bei immunsupprimierten Patienten auf und können neben allgemeinen Krankheitserscheinungen Organmanifestationen wie Retinitis, interstitielle Pneumonien, Enzephalitiden, Hepatitiden oder gastrointestinale Ulzerationen bedingen. Eine besonders gefährdete Gruppe sind seronegative Empfänger von Organtransplantaten eines CMV-seropositiven Spenders, die in dieser Konstellation durch eine antivirale Dauerprophylaxe vor einer Reaktivierung geschützt werden müssen.
Zytomegalievirusinfektionen bei immunkompetenten Patienten werden symptomatisch behandelt. Für Reaktivierungen bei immunsupprimierten Patienten wird eine i.v.-Therapie mit Ganciclovir empfohlen [5]. Ganciclovir ist ein NA mit guter Wirksamkeit gegen CMV, aber einem vergleichsweise ungünstigen Nebenwirkungsprofil mit insbesondere nephro- und myelotoxischen Effekten. Es sollten daher regelmäßig Blutbild und Nierenfunktion kontrolliert werden. Weiterhin sind eine Mutagenität, Teratogenität und Karzinogenität nicht auszuschließen, sodass der Einsatz bei jüngeren Patienten zurückhaltend erfolgen sollte und sichere Methoden zur Empfängnisverhütung angewendet werden müssen. Foscarnet kann zur Therapie von CMV-Infektionen bei Patienten mit erworbenem Immundefektsyndrom (AIDS) eingesetzt werden, ist aber nephrotoxisch. Als Reservemedikament zur Behandlung der CMV-Retinitis bei Patienten mit dem „acquired immune deficiency syndrome“ (Aids) kann das NA Cidofovir eingesetzt werden.
Zur oralen Anwendung eignet sich Valganciclovir, das eine deutlich verbesserte orale Bioverfügbarkeit aufweist. Valganciclovir ist zur Therapie der CMV-Retinitis sowie zur Prophylaxe nach Organtransplantation zugelassen. Für diese Indikation kann alternativ Valaciclovir verwendet werden. Zur Prophylaxe einer CMV-Erkrankung nach allogener Stammzelltransplantationen ist seit 2018 auch Letermovir zugelassen, ein in Deutschland entwickelter CMV-spezifischer Terminaseinhibitor [32]. Therapeutisch kommen bei diesen Patienten zusätzlich CMV-Immunglobuline zur Anwendung, deren Bedeutung mit den neu verfügbaren Medikamenten allerdings abgenommen hat. Da das CMV eine vergleichsweise niedrige Replikationsrate besitzt, kann das Ansprechen auf eine antivirale Therapie mehrere Tage dauern. Dies sollte bei der Therapiekontrolle berücksichtigt werden.
Akute Atemwegsinfektionen
Influenza
Die endemische Grippe wird durch saisonal auftretende Infektionen primär mit Influenzavirus A oder B verursacht; diese können anhand der Oberflächenantigene H (Hämagglutinin) und N (Neuraminidase) in unterschiedliche Subtypen unterteilt werden. Zur antiviralen Therapie stehen Neuraminidaseinhibitoren wie Oseltamivir und Zanamivir zur Verfügung, die durch Bindung an das virale Enzym die Freisetzung neuer Viruspartikel am Ende des viralen Replikationszyklus verhindern. Der frühzeitige Einsatz, z. B. innerhalb der ersten 48 h nach Symptombeginn, kann eine Symptomlinderung und Verkürzung der Krankheitsdauer bewirken [12]. Neuraminidaseinhibitoren eignen sich ebenfalls zu Prophylaxe und Postexpositionsprophylaxe, z. B. bei Ausbrüchen in Gesundheitseinrichtungen [13]. Bei hospitalisierten Patienten mit Influenza handelt es sich meist um schwere Verläufe mit länger bestehenden Symptomdauern, bei denen der Nutzen einer antiviralen Therapie meist auf eine Reduktion der Infektiosität beschränkt ist [16, 25].
Das in Deutschland zugelassene Amantadin blockiert den M2-Ionenkanal und damit die Virusaufnahme. Es ist ausschließlich gegen das Influenza A Virus wirksam und wird wegen der raschen Resistenzentwicklung nicht mehr empfohlen.
Baloxavir marboxil hemmt die CAP-abhängige Endonuklease von Influenza-A- und Influenza-B-Viren
Ein neuer antiviraler Wirkstoff ist Baloxavir marboxil. Seine Wirkung beruht auf der Hemmung der „Cap“-abhängigen Endonuklease von Influenza-A- und Influenza-B-Viren, wodurch die mRNA-Synthese gestört wird. Baloxavir kann als Einmalgabe bis zu 48 h nach Symptombeginn bei akuter Influenza oder unmittelbar nach Exposition als Postexpositionsprophylaxe eingesetzt werden. Die Wirksamkeit von Baloxavir ist der von Neuraminidaseinhibitoren wahrscheinlich überlegen, der größte Vorteil liegt jedoch in der einmaligen oralen Verabreichung [40, 45].
„Coronavirus disease 2019“
Infektionen mit dem „severe acute respiratory syndrome coronavirus 2“ (SARS-CoV-2) verursachen primär Atemwegserkrankungen, die mit milden Erkältungssymptomen bis hin zu schwersten Verläufen mit hypoxämischem Lungenversagen einhergehen können und zusammenfassend als „coronavirus disease 2019“ (COVID-19) bezeichnet werden. Bekannte antivirale Substanzen, die eine In-vitro-Aktivität gegenüber SARS-CoV‑2 zeigten, wurden in kürzester Zeit in klinischen Studien geprüft [38] und teilweise in Abwesenheit ausreichender klinischer Evidenz eingesetzt. Ein klinischer Nutzen konnte in den allermeisten Fällen jedoch nicht nachgewiesen werden.
Das Nukleosidanalogon-Pro-Drug Remdesivir stammt aus einem Entwicklungsprogramm für antivirale Medikamente, die bei Infektionen mit humanpathogenen RNA-Viren, wie Flaviviren, Filoviren, aber auch Coronaviren eingesetzt werden können. Die intrazellulär aktivierte Triphosphatform wird kompetitiv in die replizierende RNA eingebaut und hemmt bei SARS-CoV‑2 die RNA-abhängige RNA-Polymerase NSP12, was einen vorzeitigen Kettenabbruch zur Folge hat [31]. Einen ähnlichen Wirkmechanismus hat das in Zulassung befindliche Molnupiravir (s. unten). Remdesivir besitzt eine In-vitro-Aktivität gegen SARS-CoV‑2 [38] und wurde in mehreren randomisierten, kontrollierten Studien geprüft, die z. T. zu unterschiedlichen Ergebnissen für die Gesamtgruppen kamen [1, 7, 35, 39, 44]. Ein klinischer Nutzen wird insbesondere bei Anwendung in der Frühphase der Erkrankung vermutet, da in Subgruppenanalysen sauerstoffpflichtige Patienten zu profitieren scheinen, intensivpflichtige beatmete Patienten hingegen nicht. Im Rahmen der PINETREE Studie (NCT 04501952) zeigten sich nach Angaben des Herstellers positive Effekte auf den Krankheitsverlauf bei ambulanten Patienten, die frühzeitig behandelt wurden [18]. In der Europäischen Union erhielt Remdesivir für die Behandlung von hospitalisierten Patienten mit COVID-19-assoziierter Pneumonie und Sauerstoffbedarf eine konditionelle Marktzulassung. Eine finale Bewertung über den klinischen Nutzen und klare Empfehlungen zum rationalen Einsatz von Remdesivir bei COVID-19 stehen noch aus [27].
Ein weiterer antiviraler Ansatz stellt die passive Immunisierung mit SARS-CoV-2 neutralisierenden monoklonalen Antikörpern (nMAB) dar. Diese binden an spezifische Epitope an der rezeptorbindenden Domäne (RBD) des SARS-CoV‑2 Spikeproteins und sind dadurch in der Lage, den Eintritt von Viren in die Zellen zu verhindern. Im November 2021 wurde erstmals ein nMAB-Präparat zur Therapie und Prophylaxe von COVID‑19 bei Patienten, die (noch) keine Sauerstofftherapie benötigen, zugelassen [26]. Die Kombination aus Casirivimab und Imdevimab (Ronapreve) zeigte in klinischen Studien einen günstigen Einfluss auf den Krankheitsverlauf von ungeimpften Patienten mit Risikofaktoren, die frühzeitig behandelt wurden [43]. Ein Mortalitäsvorteil ist zudem für hospitalisierten Patienten belegt, die noch keine humorale Immunantwort mit Immunglobulin G entwickelt haben [28]. Darüber hinaus sind nMAB wirksam in der Prä- und Postexpositionsprophylaxe [10, 22, 34]. Derzeit befindet sich eine Vielzahl nMAB gegen SARS-CoV‑2 in der präklinischen und klinischen Entwicklung. Durch das Targeting von viralen Strukturen ist die Verträglichkeit dieser Substanzen i. Allg. sehr gut. Gleichzeitig sind diese Strategien jedoch durch Selektionsmechanismen anfällig für Resistenzbildung. Nach ersten Erkenntnissen ist die Omikron-Variante in der Lage sich den meisten zugelassenen nMAB zu entziehen [9].
Ausblick: Entwicklung neuer antiviraler Medikamente
Als wirksamste Angriffspunkte für antivirale Medikamente haben sich virale Polymerasen erwiesen, die durch Nukleos(t)idanaloga oder sterisch inhibiert werden können, gefolgt von viralen Proteasen. Weiterhin stellen virale Terminasen und Nukleasen eine vielversprechende Grundlage für die Entwicklung neuer antiviraler Therapien dar. Bedingt durch ihre hohe Spezifizität für das jeweilige Virus bieten direkt antivirale Therapieansätze meist ein günstiges Nebenwirkungsprofil. Breit antiviral wirksame Substanzen haben meist zelluläre Angriffspunkte, die für die Virusvermehrung essenziell sind, und gehen mit einem vergleichsweise ungünstigeren Nebenwirkungsprofil einher.
Im Fokus Entwicklung antiviraler Wirkstoffe gegen COVID-19. Das betrifft nMAB aber auch direkt antiviral wirksame Substanzen. Die Kombination der nMAB Tixagevimab und Cilgavimab besitzt laut Herstellerangaben eine deutlich verlängerte Halbwertszeit, was insbesondere Vorteile für den prophylaktischen Einsatz bieten könnte. Der nMAB Sotrovimab soll ebenfalls verbesserte pharmakokinetische Eigenschaften besitzen und scheint nach ersten Erkenntnissen seine antivirale Aktivität auch gegenüber der Omikron-Variante zu behalten [19]. Beide Präparate befinden sich bereits im Rolling Review-Verfahren der Europäischen Arzneimittel-Agentur (EMA). Ein Nachteil von nMAB in der klinischen Anwendung besteht in der Notwendigkeit einer i.v. oder s.c.-Applikation. Aktuell befinden sich zwei oral verfügbare antivirale Substanzen in Zulassungsverfahren und könnten die therapeutischen Möglichkeiten insbesondere für ambulanten Patienten verbessern. Molnupiravir (MK-4482) ist ein oral verfügbares Pro-Drug eines synthetischen NA und zeigte in der plazebo-kontrollierten MOVe OUT-Studie eine etwa 30 % relative Risikoreduktion für Hospitalisierung oder Mortalität bis zum Tag 29. Davon profitierten ungeimpfte Patienten mit mindestens einem Risikofaktor, die innerhalb von 5 Tagen nach Symptombeginn zweimal täglich Molnupiravir für einen Zeitraum von 5 Tagen erhielten [24]. Ein weiteres oral verfügbares Medikament ist Nirmatrelvir, ein spezifischer Inhibitor der viralen 3CL-Protease von SARS-CoV‑2. Zum erreichen adäquater Wirkstoffspiegel wird Nirmatrelvir in Kombination mit dem CYP 3A4 Inhibitor Ritonavir verabreicht. Im Rahmen der EPIC-HR-Studie (NCT04960202) reduzierte eine fünftägige Therapie mit Nirmatrelvir/Ritonavir laut Pressemeldungen die Hospitalisierungs- und/oder Sterberate relativ um 88 % bei ambulanten Patienten mit mindestens einem Risikofaktor für einen schweren Verlauf bei frühzeitigem Therapiebeginn innerhalb 5 Tage nach Symptombeginn. Durch die erforderliche Kombination mit Ritonavir kann es bei jedoch zu Arzneimittelinteraktionen kommen, die berücksichtigt werden müssen. Sowohl Molnupiravir als auch Nirmatrelvir/Ritonavir erhielten kürzlich von der EMA die Genehmigung zur Anwendung vor Marktzulassung nach Artikel 5(3) der Verordnung (EG) Nr. 726/2004 des Europäischen Parlaments.
Fazit für die Praxis
Moderne antivirale Medikamente haben die therapeutischen Möglichkeiten für chronische Infektionen mit Hepatitis-B- (HBV) und Hepatitis-C-Virus (HCV) sowie „human immunodeficiency virus“ (HIV) revolutioniert. Sie ermöglichen eine Heilung der Hepatitis C und zumindest eine anhaltende Kontrolle der HBV- und HIV-Vermehrung.
Eine frühzeitige, gezielte antivirale Therapie kann Erkrankungen durch ein Aufflammen der Herpes-simplex- (HSV), Varizella-Zoster- (VZV) oder Zytomegalieviren (CMV) abmildern und die Krankheitsdauer verkürzen. Evidenzbasierte antivirale Therapien gegen Infektionen mit EBV oder die Typen 6–8 der Herpesviridae (HHV) sind aktuell nicht vorhanden.
Bei immunsupprimierten Patienten können antivirale Medikamente das Risiko von schwerwiegenden Erkrankungen durch humane Herpesviren oder durch HBV reduzieren.
Die therapeutischen Möglichkeiten bei viralen Atemwegsinfektionen und anderen akut verlaufenden Virusinfektionen sind auf Zeitfenster mit relevanter Virusvermehrung begrenzt. Eine antivirale Therapie hat deshalb in der Frühphase der Erkrankung und in der präsymptomatischen Phase nach der Infektion die größten Erfolgschancen. Hier sind aktuell mehrere Medikamente in der Entwicklung bzw. Zulassung.
Antivirale Prä- oder Postexpositionsprophylaxe haben sich für HBV und HIV durchgesetzt und stehen für Infektionen mit Influenza A/B Viren und durch die nMAB auch für SARS-CoV‑2 zur Verfügung.
Einhaltung ethischer Richtlinien
Interessenkonflikt
J.J. Malin erhielt Beraterhonorare von MAPLE Health Group und Atriva Therapeutics GmbH, Reisekostenerstattungen von Gilead Sciences, ViiV Healthcare und Correvio Pharma sowie institutionelle Forschungsgelder vom Deutschen Zentrum für Infektionsforschung (DZIF) und den U.S. National Institutes of Health (NIH). Christoph Spinner erklärt, Reisekosten- und Kongressunterstützung der Firmen AbbVie, Astellas, Bristol-Meyers Squibb, Gilead Sciences, Janssen-Cilag, Pfizer und ViiV Healthcare erhalten zu haben. Der Autor ist oder war beratend für AbbVie, Apeiron, B. Braun Melsungen, Cepheid, Formycon, Gilead Sciences, GSK, Janssen-Cilag, Merck Sharp & Dome, Molecular Partners und ViiV Healthcare tätig. Der Autor ist oder war an multizentrischen Studien der Firmen AbbVie, Apeiron, B. Braun Melsungen, Gilead Sciences, Janssen-Cilag, Sanofi Aventis und ViiV Healthcare beteiligt. Darüber hinaus bestehen oder bestanden Drittmittelzuwendungen für Forschungsprojekte durch die Firmen Gilead Sciences, Janssen-Cilag, ViiV Healthcare sowie das nationale Netzwerk Universitätsmedizin, Berlin, und das Deutsche Zentrum für Infektionsforschung (DZIF), Braunschweig. Ulrike Protzer ist bzw. war in den letzten 5 Jahren beratend für die Firmen AbbVie, Arbutus, BioNTech, Gilead, GSK, Johnson & Johnson, Pfizer, Roche, Sanofi, Sobi und Vaccitech tätig. Sie ist Mitgründerin und Anteilsinhaberin von SCG Cell Therapy. Ulrike Protzer erhält Forschungsunterstützung von ALiOS and Vir Biotechnology. Zudem werden die Projekte ihres Labors von der Deutschen Forschungsgemeinschaft (DFG), dem NIH, dem DZIF, dem Bundesministerium für Bildung und Forschung (BMBF), dem nationalen Netzwerk Universitätsmedizin, der EU im Rahmen des Horizon-2020-Programms, dem Bayerischen Staatsministerium für Wissenschaft und Kunst im Rahmen der Konsortien FOR-Covid und CoVaKo, der Helmholtz Gemeinschaft sowie der Bayerischen Forschungsstiftung gefördert. T. Bunse gibt an, dass kein Interessenkonflikt besteht.
Für diesen Beitrag wurden von den Autoren keine Studien an Menschen oder Tieren durchgeführt. Für die aufgeführten Studien gelten die jeweils dort angegebenen ethischen Richtlinien.
Footnotes

QR-Code scannen & Beitrag online lesen
Literatur
- 1.Ader F, Bouscambert-Duchamp M, Hites M, Peiffer-Smadja N, Poissy J, Belhadi D, Diallo A, Lê M-P, Peytavin G, Staub T, Greil R, Guedj J, Paiva J-A, Costagliola D, Yazdanpanah Y, Burdet C, Mentré F, Egle A, Greil R, Joannidis M, Lamprecht B, Altdorfer A, Belkhir L, Fraipont V, Hites M, Verschelden G, Aboab J, Ader F, Ait-Oufella H, Andrejak C, Andreu P, Argaud L, Bani-Sadr F, Benezit F, Blot M, Botelho-Nevers E, Bouadma L, Bouchaud O, Bougon D, Bouiller K, Bounes-Vardon F, Boutoille D, Boyer A, Bruel D, Cabié A, Canet E, Cazanave C, Chabartier C, Chirouze C, Clere-Jehl R, Courjon J, Crockett F, Danion F, Delbove A, Dellamonica J, Djossou F, Dubost C, Duvignaud A, Epaulard O, Epelboin L, Fartoukh M, Faure K, Faure E, Ferry T, Ficko C, Figueiredo S, Gaborit B, Gaci R, Gagneux-Brunon A, Gallien S, Garot D, Geri G, Gibot S, Goehringer F, Gousseff M, Gruson D, Hansmann Y, Hinschberger O, Jaureguiberry S, Jeanmichel V, Kerneis S, Kimmoun A, Klouche K, Lachâtre M, Lacombe K, Laine F, Lanoix J-P, Launay O, Laviolle B, Le Moing V, Le Pavec J, Le Tulzo Y, Le Turnier P, Lebeaux D, Lefevre B, Leroy S, Lescure F-X, Lessire H, Leveau B, Loubet P, Makinson A, Malvy D, Marquette C-H, Martin-Blondel G, Martinot M, Mayaux J, Mekontso-Dessap A, Meziani F, Mira J-P, Molina J-M, Monnet X, Mootien J, Mourvillier B, Murris-Espin M, Navellou J-C, Nseir S, Oulehri W, Peiffer-Smadja N, Perpoint T, Pialoux G, Pilmis B, Piriou V, Piroth L, Poissy J, Pourcher V, Quenot J-P, Raffi F, Reignier J, Revest M, Richard J-C, Béatrice CR-P, Roger RP-A, Roger C, Rouveix-Nordon E, Ruch Y, Saidani N, Sayre N, Senneville E, Sotto A, Stefan F, Tacquard C, Terzi N, Textoris J, Thiery G, Timsit J-F, Tolsma V, Turmel J-M, Valour F, Wallet F, Wattecamps G, Yazdanpanah Y, Zerbib Y, Berna M, Reuter J, Staub T, Braz S, Ferreira J-M, Paiva RJ-A, Roncon-Albuquerque R, Bouscambert-Duchamp M, Gaymard A, Lê M-P, Lina B, Peytavin G, Tubiana S, Couffin-Cadièrgues S, Esperou H, Belhadi D, Burdet C, Costagliola D, Dechanet A, Delmas C, Diallo A, Fougerou C, Guedj J, Mentré F, Mercier N, Noret M, Saillard J, Velou P. Remdesivir plus standard of care versus standard of care alone for the treatment of patients admitted to hospital with COVID-19 (DisCoVeRy): a phase 3 randomised controlled open-label trial. The Lancet Infectious Diseases. 2021 doi: 10.1016/S1473-3099(21)00485-0. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 2.Arbeitsgemeinschaft Der Wissenschaftlichen Medizinischen Fachgesellschaften e. V. (AWMF) (2018) Deutsch-Österreichische Leitlinie zur medikamentösen Postexpositionsprophylaxe der HIV-Infektion – Update 2018 (AWMF-Register-Nr.: 055-004). https://www.awmf.org/uploads/tx_szleitlinien/055-004l_S2k_Medikamentoese-Postexpositionsprophylaxe-PEP-nach-HIV-Exposition_2018-12.pdf. Zugegriffen: 16. Sep. 2021
- 3.Arbeitsgemeinschaft Der Wissenschaftlichen Medizinischen Fachgesellschaften e. V. (AWMF) (2018) Deutsch-Österreichische Leitlinien zur HIV-Präexpositionsprohphylaxe (PrEP) (AWMF-Register-Nr.: 055-008). https://www.awmf.org/uploads/tx_szleitlinien/055-008l_S2k_HIV-Praeexpositionsprophylaxe_2019-01_01.pdf. Zugegriffen: 16. Sep. 2021
- 4.Asselah T, Kowdley KV, Zadeikis N, et al. Efficacy of Glecaprevir/Pibrentasvir for 8 or 12 Weeks in Patients With Hepatitis C Virus Genotype 2, 4, 5, or 6 Infection Without Cirrhosis. Clin Gastroenterol Hepatol. 2018;16:417–426. doi: 10.1016/j.cgh.2017.09.027. [DOI] [PubMed] [Google Scholar]
- 5.Arbeitsgemeinschaft Der Wissenschaftlichen Medizinischen Fachgesellschaften e. V. (AWMF) (2019) S2k-Leitlinie Virusinfektionen bei Organ- und allogen Stammzell-Transplantierten: Diag-nostik, Prävention und Therapie (AWMF Registernummer 093-002). https://www.awmf.org/uploads/tx_szleitlinien/093-002l_S2k_Virusinfektionen-Organtransplantierte-alloge-Stammzell-Transplantierten-Diagnostik-Praevention-Therapie__2019-06.pdf. Zugegriffen: 15. Sep. 2021
- 6.Arbeitsgemeinschaft Der Wissenschaftlichen Medizinischen Fachgesellschaften e. V. (AWMF) (2021) S3-Leitlinie Prophylaxe, Diagnostik und Therapie der Hepatitis-B-Virus-Infektion. https://www.awmf.org/uploads/tx_szleitlinien/021-011l_S3_Prophylaxe-Diagnostik-Therapie-der-Hepatitis-B-Virusinfektion_2021-07.pdf. Zugegriffen: 15. Sep. 2021
- 7.Beigel JH, Tomashek KM, Dodd LE, et al. Remdesivir for the treatment of Covid-19—final report. N Engl J Med. 2020;383:1813–1826. doi: 10.1056/NEJMoa2007764. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 8.Bowsher D. The lifetime occurrence of Herpes zoster and prevalence of post-herpetic neuralgia: A retrospective survey in an elderly population. Eur J Pain. 1999;3:335–342. doi: 10.1016/S1090-3801(99)90015-0. [DOI] [PubMed] [Google Scholar]
- 9.Cao Y, Wang J, Jian F, et al. B.1.1.529 escapes the majority of SARS-CoV-2 neutralizing antibodies of diverse epitopes. bioRxiv. 2021 doi: 10.1101/2021.12.07.470392. [DOI] [Google Scholar]
- 10.Cohen MS, Nirula A, Mulligan MJ, et al. Effect of Bamlanivimab vs Placebo on Incidence of COVID-19 Among Residents and Staff of Skilled Nursing and Assisted Living Facilities: A Randomized Clinical Trial. JAMA. 2021;326:46–55. doi: 10.1001/jama.2021.8828. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 11.Deutsche Aids Gesellschaft (DAIG) Deutsch-Österreichische Leitlinien zur antiretroviralen Therapie der HIV-1-Infektion (AWMF-Register-Nr.: 055-001) 2020. [DOI] [PubMed] [Google Scholar]
- 12.Dobson J, Whitley RJ, Pocock S, et al. Oseltamivir treatment for influenza in adults: a meta-analysis of randomised controlled trials. Lancet. 2015;385:1729–1737. doi: 10.1016/S0140-6736(14)62449-1. [DOI] [PubMed] [Google Scholar]
- 13.Duwe SC, Schmidt B, Gärtner BC, et al. Prophylaxis and treatment of influenza: options, antiviral susceptibility, and existing recommendations. GMS Infect. Dis. 2021;9:Doc02. doi: 10.3205/id000071. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 14.Elion GB. Acyclovir: discovery, mechanism of action, and selectivity. J Med Virol Suppl. 1993;1:2–6. doi: 10.1002/jmv.1890410503. [DOI] [PubMed] [Google Scholar]
- 15.European Aids Clinical Society (EACS) (2020) EACS Guidelines 10.1. https://www.eacsociety.org/media/guidelines-10.1_30032021_1.pdf. Zugegriffen: 20. Sep. 2021
- 16.Fielding JE, Kelly HA, Mercer GN, et al. Systematic review of influenza A(H1N1)pdm09 virus shedding: duration is affected by severity, but not age. Influenza Other Respir Viruses. 2014;8:142–150. doi: 10.1111/irv.12216. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 17.Gehring AJ, Protzer U. Targeting Innate and Adaptive Immune Responses to Cure Chronic HBV Infection. Gastroenterology. 2019;156:325–337. doi: 10.1053/j.gastro.2018.10.032. [DOI] [PubMed] [Google Scholar]
- 18.Gilead Sciences. https://www.gilead.com/news-and-press/press-room/press-releases/2021/9/veklury-remdesivir-significantly-reduced-risk-of-hospitalization-in-highrisk-patients-with-covid19. Zugegriffen: 14. Dez. 2021
- 19.Gruell H, Vanshylla K, Tober-Lau P, et al. mRNA booster immunization elicits potent neutralizing serum activity against the SARS-CoV-2 Omicron variant. medRxiv. 2021 doi: 10.1101/2021.12.14.21267769. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 20.Hope-Simpson RE. Postherpetic neuralgia. J R Coll Gen Pract. 1975;25:571–575. [PMC free article] [PubMed] [Google Scholar]
- 21.Ichai P, Samuel D. Management of Fulminant Hepatitis B. Curr Infect Dis Rep. 2019;21:25. doi: 10.1007/s11908-019-0682-9. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 22.Isa F, Forleo-Neto E, Meyer J, et al. Repeat Subcutaneous Administration of REGEN-COV® in Adults is Well-Tolerated and Prevents the Occurrence of COVID-19. 2021. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 23.James C, Harfouche M, Welton NJ, et al. Herpes simplex virus: global infection prevalence and incidence estimates, 2016. Bull World Health Organ. 2020;98:315–329. doi: 10.2471/BLT.19.237149. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 24.Jayk Bernal A, Gomes da Silva MM, Musungaie DB, Kovalchuk E, Gonzalez A, Delos RV, Martín-Quirós A, Caraco Y, Williams-Diaz A, Brown ML, Du J, Pedley A, Assaid C, Strizki J, Grobler JA, Shamsuddin HH, Tipping R, Wan H, Paschke A, Butterton JR, Johnson MG, De Anda C. Molnupiravir for Oral Treatment of Covid-19 in Nonhospitalized Patients. New England Journal of Medicine. 2021 doi: 10.1056/NEJMoa2116044. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 25.Jefferson T, Jones MA, Doshi P, et al. Neuraminidase inhibitors for preventing and treating influenza in healthy adults and children. Cochrane Database Syst Rev. 2014 doi: 10.1002/14651858.CD008965.pub4. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 26.Karagiannidis C, Lang K, Mikolajewska A, Malin JJ, Kluge S, Spinner CD. Dtsch Arztebl. 2021;118(47):A-2212/B-1825. [Google Scholar]
- 27.Kluge S, Malin JJ, Fichtner F, Müller OJ, Skoetz N, Karagiannidis C. Recommendations on the in-hospital treatment of patients with COVID-19. Deutsches Ärzteblatt international. 2021 doi: 10.3238/arztebl.m2021.0374. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 28.Kreuzberger N, Hirsch C, Chai KL, Tomlinson E, Khosravi Z, Popp M, Neidhardt M, Piechotta V, Salomon S, Valk SJ, Monsef I, Schmaderer C, Wood EM, So-Osman C, Roberts DJ, McQuilten Z, Estcourt LJ, Skoetz N. SARS-CoV-2-neutralising monoclonal antibodies for treatment of COVID-19. Cochrane Database of Systematic Reviews. 2021 doi: 10.1002/14651858.CD013825.pub2. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 29.Lehmann C, Malin J, Suárez I, et al. Modern HIV treatment. Internist. 2019;60:411–419. doi: 10.1007/s00108-019-0564-0. [DOI] [PubMed] [Google Scholar]
- 30.Lok AS, Zoulim F, Dusheiko G, et al. Hepatitis B cure: From discovery to regulatory approval. J Hepatol. 2017;67:847–861. doi: 10.1016/j.jhep.2017.05.008. [DOI] [PubMed] [Google Scholar]
- 31.Malin JJ, Suárez I, Priesner V, et al. Remdesivir against COVID-19 and Other Viral Diseases. Clin Microbiol Rev. 2020 doi: 10.1128/cmr.00162-20. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 32.Marty FM, Ljungman P, Chemaly RF, et al. Letermovir prophylaxis for cytomegalovirus in hematopoietic-cell transplantation. N. Engl. J. Med. 2017;377:2433–2444. doi: 10.1056/NEJMoa1706640. [DOI] [PubMed] [Google Scholar]
- 33.Neumann AU, Lam NP, Dahari H, et al. Hepatitis C Viral Dynamics in Vivo and the Antiviral Efficacy of Interferon-α Therapy. Science. 1998;282:103–107. doi: 10.1126/science.282.5386.103. [DOI] [PubMed] [Google Scholar]
- 34.O’brien MP, Forleo-Neto E, Musser BJ, et al. Subcutaneous REGEN-COV Antibody Combination to Prevent Covid-19. N Engl J Med. 2021 doi: 10.1056/NEJMoa2109682. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 35.Pan H, Peto R, Henao-Restrepo AM, et al. Repurposed Antiviral Drugs for Covid-19—Interim WHO Solidarity Trial Results. N. Engl. J. Med. 2021;384:497–511. doi: 10.1056/NEJMoa2023184. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 36.Pattullo V. Prevention of Hepatitis B reactivation in the setting of immunosuppression. Clin. Mol. Hepatol. 2016;22:219–237. doi: 10.3350/cmh.2016.0024. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 37.Ringelhan M, McKeating JA, Protzer U. Viral hepatitis and liver cancer. Philos Trans R Soc Lond B Biol Sci. 2017 doi: 10.1098/rstb.2016.0274. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 38.Simonis A, Theobald SJ, Fätkenheuer G, et al. A comparative analysis of remdesivir and other repurposed antivirals against SARS-CoV-2. EMBO Mol Med. 2021;13:e13105. doi: 10.15252/emmm.202013105. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 39.Spinner CD, Gottlieb RL, Criner GJ, et al. Effect of Remdesivir vs Standard Care on Clinical Status at 11 Days in Patients With Moderate COVID-19: A Randomized Clinical Trial. JAMA. 2020;324:1048–1057. doi: 10.1001/jama.2020.16349. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 40.Taieb V, Ikeoka H, Ma FF, et al. A network meta-analysis of the efficacy and safety of baloxavir marboxil versus neuraminidase inhibitors for the treatment of influenza in otherwise healthy patients. Curr Med Res Opin. 2019;35:1355–1364. doi: 10.1080/03007995.2019.1584505. [DOI] [PubMed] [Google Scholar]
- 41.U.S. Food and Drug Administration Center for Drug Evaluation and Research (2021) FDA Briefing Document Antimicrobial Drugs Advisory Committee Meeting November 30, 2021. Verfügbar unter: https://www.fda.gov/media/154418/download. Zugegriffen: 16. Dez. 2021
- 42.Van Bömmel F, Berg T. Risks and Benefits of Discontinuation of Nucleos(t)ide Analogue Treatment: A Treatment Concept for Patients With HBeAg-Negative Chronic Hepatitis B. Hepatol Commun. 2021 doi: 10.1002/hep4.1708. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 43.Weinreich DM, Sivapalasingam S, Norton T, Ali S, Gao H, Bhore R, Xiao J, Hooper AT, Hamilton JD, Musser BJ, Rofail D, Hussein M, Im J, Atmodjo DJ, Perry C, Pan C, Mahmood A, Hosain R, Davis JD, Turner KC, Baum A, Kyratsous CA, Kim Y, Cook A, Kampman W, Roque-Guerrero L, Acloque G, Aazami H, Cannon K, Simón-Campos JA, Bocchini JA, Kowal B, DiCioccio AT, Soo Y, Geba GP, Stahl N, Lipsich L, Braunstein N, Herman G, Yancopoulos GD. REGEN-COV Antibody Combination and Outcomes in Outpatients with Covid-19. New England Journal of Medicine. 2021;385(23):e81. doi: 10.1056/NEJMoa2108163. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 44.Wang Y, Zhang D, Du G, et al. Remdesivir in adults with severe COVID-19: a randomised, double-blind, placebo-controlled, multicentre trial. Lancet. 2020;395:1569–1578. doi: 10.1016/S0140-6736(20)31022-9. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 45.Yoshii N, Tochino Y, Fujioka M, et al. The Comparison of the Efficacy of Baloxavir and Neuraminidase Inhibitors for Patients with Influenza A in Clinical Practice. Intern Med. 2020;59:1509–1513. doi: 10.2169/internalmedicine.4117-19. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 46.Zuckerman E, Gutierrez JA, Dylla DE, et al. Eight Weeks of Treatment With Glecaprevir/Pibrentasvir Is Safe and Efficacious in an Integrated Analysis of Treatment-Naïve Patients With Hepatitis C Virus Infection. Clin Gastroenterol Hepatol. 2020;18:2544–2553.e6. doi: 10.1016/j.cgh.2020.06.044. [DOI] [PubMed] [Google Scholar]