Abstract
Unter dem Begriff Pseudolymphom (PSL) versteht man eine benigne, reaktive Lymphoproliferation der Haut, die klinisch und/oder histologisch ein malignes Lymphom simulieren kann. Die genaue Ätiopathogenese ist bis heute nicht gänzlich geklärt. Man unterscheidet die primären, idiopathischen PSL ohne erkennbare Ursache von den sekundären PSL mit bekanntem Stimulus. Wir berichten über das Auftreten von Pseudolymphomen nach einer Behandlung mit medizinischen Blutegeln (Hirudotherapie). Bisher wurden nach bestem Wissen und Gewissen insgesamt nur 9 Fälle von kutanen PSL nach Hirudotherapie in der Literatur beschrieben.
Schlüsselwörter: Blutegeltherapie, Lymphoproliferation , Histologie, Immunhistochemie , Molekularpathologie
Abstract
The term cutaneous pseudolymphoma (C-PSL) is defined in the literature as a benign, reactive lymphoproliferation that clinically and/or histopathologically imitates cutaneous lymphoma. The exact etiopathogenesis has not been fully elucidated to date. A distinction is made between primary, idiopathic PSL without an identifiable cause and secondary PSL with a known stimulus. We report the occurrence of pseudolymphoma after treatment with medicinal leeches (hirudotherapy). To the best of our knowledge, a total of only nine cases of cutaneous PSL after hirudotherapy have been reported in the literature to date.
Keywords: Medicinal leech therapy, Lymphoproliferation, Histology, Immunochemistry, Molecular pathology
Anamnese
Eine 76-jährige Patientin stellte sich mit seit über 1 Jahr bestehenden, juckenden, lividen bis erythematösen Plaques an der rechten Ferse sowie im Bereich des unteren Rückens in unserer allgemeinen Ambulanz vor. Auf intensive Nachfrage berichtete die Patientin, dass sie sich aufgrund von Gelenkschmerzen im Lendenwirbelsäulenbereich und eines Fersensporns einige Wochen vor Auftreten der Effloreszenzen 2 Sitzungen einer Blutegeltherapie durch eine Heilpraktikerin unterzogen hatte. Es wurden keine relevanten Nebenerkrankungen angegeben. Die Dauermedikation bestand aus Metoprolol, Ramipril sowie L‑Thyroxin.
Diagnostik
Hautbefund
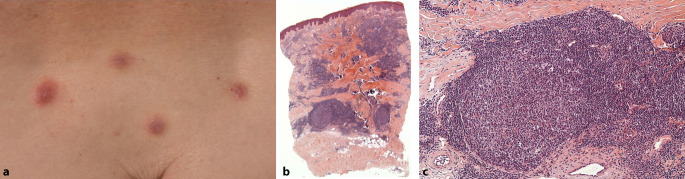
Bei der Ganzkörperinspektion zeigten sich an oben genannten Ansatzstellen der Blutegel insgesamt 7 livide bis erythematöse, infiltrierte Plaques (Abb. 1a). Das übrige Integument und die Schleimhäute kamen unauffällig zur Darstellung. Zur weiteren diagnostischen Einordnung erfolgte die Durchführung einer Probebiopsie.
Histopathologischer Befund
Es zeigten sich knotige, lymphozytär dominierte Entzündungsinfiltrate mit vereinzelten eosinophilen Granulozyten und Plasmazellen um eine zentral gelegene, zur Epidermis senkrecht stehende Narbenzone. Zur Tiefe hin waren regelrecht ausgebildete, reaktive Follikelzentren mit Kerntrümmermakrophagen, zahlreichen Mitosen und erhaltener Mantelzone erkennbar (Abb. 1b, c).
Immunhistochemischer Befund
Immunhistochemische Färbungen zeigten ein gemischtzelliges Infiltrat mit Nachweis von zahlreichen kleinen B‑ und T‑Lymphozyten (Positivität für CD4- und CD20).
Laborbefund
Die Lues- und Borrelienserologie waren negativ.
Diagnose
In Zusammenschau der Anamnese, des klinischen Befundes, der Histopathologie sowie der Immunhistochemie stellten wir die Diagnose kutaner Pseudolymphome (PSL) nach medizinischer Blutegeltherapie.
Therapie und Verlauf
Es wurde eine topische Behandlung mit Mometason eingeleitet. Bei der letzten Wiedervorstellung zur Verlaufskontrolle nach 24 Monaten zeigten sich nur noch dezent sichtbare livide Verfärbungen im Bereich der ehemaligen Knoten an der Lendenwirbelsäule.
Diskussion
Unter dem Begriff Pseudolymphom (PSL) oder kutane lymphoide Hyperplasie versteht man eine benigne, reaktive Lymphoproliferation der Haut, die klinisch und/oder histologisch ein malignes Lymphom simulieren kann [1, 2]. Es handelt sich um eine heterogene Gruppe von Entitäten, die sich klinisch, histologisch, immunhistochemisch sowie ätiologisch unterscheiden [1]. In den letzten Jahren wurden in der Literatur zahlreiche Klassifikationen für Pseudolymphome publiziert [1]. Diese beinhalten Einteilungen der PSL nach dem Immunphänotyp (T-Zell‑, B‑Zell- oder gemischtzellig), den histopathologischen Merkmalen, der Ätiologie sowie nach unterschiedlichen klinischen Merkmalen [2]. Eine international etablierte, konsensusbasierte Klassifikation analog der WHO(World Health Organization)-EORTC(European Organization for Research and Treatment of Cancer)-Klassifikation für kutane Lymphome liegt bis zum jetzigen Zeitpunkt nicht vor [1]. Man unterscheidet die primären, idiopathischen PSL ohne erkennbare Ursache von den sekundären PSL mit bekanntem Stimulus [3, 4]. Triggerfaktoren umfassen u. a. verschiedene Medikamente und Infektionen, aber auch Traumata wie Tattoos, Insektenstiche, Akupunktur und Impfungen [2, 4–6]. Ein typisches histologisches Merkmal der kutanen PSL ist das Vorhandensein eines polyklonalen, lymphozytären Infiltrats in der oberen Dermis [4]. Charakteristisch für die PSL ist ein gutartiger Verlauf. Aufgrund der selten beschriebenen malignen Transformation sowie der mitunter erheblichen differenzialdiagnostischen Schwierigkeiten sollten regelmäßige Nachsorgeuntersuchungen erfolgen [1, 5].
In dem vorliegenden Fall kam es zu einem Auftreten von Pseudolymphomen nach einer Behandlung mit medizinischen Blutegeln (Hirudotherapie). Bisher wurden nach bestem Wissen und Gewissen insgesamt nur 9 Fälle von kutanen PSL nach Hirudotherapie in der Literatur beschrieben [3–11], die in Tab. 1 zusammengefasst sind. Histologisch und immunhistochemisch zeigte sich ein breites Bild ohne Dominanz eines Musters. Therapeutisch wurde zumeist entweder eine topische oder intraläsionale Steroidbehandlung durchgeführt. Hierunter kam es in den berichteten Fällen zu einer Befundbesserung.
| Autor (Jahr, Referenz) | Alter/Geschlecht | Lokalisation | Indikation der Hirudotherapie | Immunhistochemie | Therapie | Follow-up |
|---|---|---|---|---|---|---|
| Hanner et al. (aktueller Fall) | 76/w | Unterer Rücken (lumbal), Ferse | Gelenkschmerzen, Fersensporn | Gemischt T‑ und B‑lymphozytäres Infiltrat | Topische ST | Langsam rückläufige Läsion |
| Sepaskhah et al. (2020), [11] | 44/w | Schienbein | Erythema nodosum | Nicht durchgeführt | Systemische ST | Rückläufige Läsionen |
| Topische ST | ||||||
| Intraläsionale ST | ||||||
| Sadati et al. (2019), [9] | 45/w | Untere Extremitäten | Varikose und Schmerzen | Nicht durchgeführt | Topische ST | Komplett rückläufige Läsionen |
| Kryotherapie | ||||||
| Temiz et al. (2019), [5] | 54/m | Hals | Unbekannt | T‑lymphozytär dominiertes Infiltrat | Intraläsionale ST | Nach 1 Monat: rückläufige Läsionen |
| Nach 6 Monaten: kein Rezidiv | ||||||
| Aktas et al. (2018), [10] | 65/w | Unterer Rücken (lumbal) | Rückenschmerzen | Nicht durchgeführt | Intraläsionale ST | Rückläufige Läsionen |
| Kryotherapie | ||||||
| Tupikowska et al. (2018), [4] | 38/w | Regio pubica | Uterusmyom | Gemischtzelliges, T‑lymphozytär dominiertes Infiltrat | Orale AH | Langsam rückläufige Läsionen |
| Topische ST | ||||||
| Intraläsionale ST | ||||||
| Intramuskuläre ST | ||||||
| Kryotherapie | ||||||
| Altamura et al. (2014), [7] | 50er/w | Rücken | Fibromyalgie | B‑lymphozytär dominiertes Infiltrat | Topische ST | Nach 1 Monat: komplett rückläufige Läsionen |
| Nach 15 Monaten: kein Rezidiv | ||||||
| Khelifa et al. (2013), [6] | 77/w | Unterer Rücken (lumbal) | Rückenschmerzen bei lumbaler Spinalkanalstenose | Gemischt T‑ und B‑lymphozytäres Infiltrat | Topische und intraläsionale ST | Rückläufige Läsionen |
| Choi et al. (2012), [3] | 52/m | Unterlid bds. | Infraorbitale Augenringe | Gemischtzelliges, T‑lymphozytär dominiertes Infiltrat | Intraläsionale ST | Nach 3 Monaten: rückläufige Läsionen |
| Smolle et al. (2000), [8] | 56/w | Unterschenkel bds. | Chronisch venöse Insuffizienz | B‑lymphozytär dominiertes Infiltrat | Intraläsionale ST | Langsam rückläufige Läsionen |
w weiblich, m männlich, ST Steroidtherapie, AH Antihistaminika, bds. beidseits
Im letzten Jahrzehnt gewann die Blutegeltherapie mit neuen Einsatzbereichen an zunehmender Bedeutung [8]. Die Hauptindikationen der medizinischen Blutegeltherapie stellen unterschiedliche Gelenkerkrankungen wie Osteoarthritis und Epikondylitis, Venenerkrankungen sowie die Lappenplastik der plastischen Chirurgie dar [12]. Die Blutegel umfassen mehr als 600 verschiedene Arten, der bekannteste und in der Medizin vorrangig eingesetzte Vertreter ist der Hirudo medicinalis [6, 12]. Bis dato konnten mehr als 20 bioaktive Substanzen im Speichelsekret der Blutegel mit u. a. analgetischen, antiinflammatorischen, plättchenhemmenden, gerinnungshemmenden und Thrombin-regulatorischen Funktionen sowie mit antimikrobiellen und extrazellulären Matrix-abbauenden Wirkungen identifiziert werden [12]. Mögliche Komplikationen sind Infektionen, Blutungen, Anämie, allergische Reaktionen sowie Narbenbildung [3]. Zudem können – wie im dargelegten Fall – kutane PSL als seltene, aber beachtenswerte Nebenwirkungen der Blutegeltherapie auftreten. Die Pathogenese der kutanen PSL nach Hirudotherapie ist bis heute nicht gänzlich geklärt. Die pseudolymphomatösen Reaktionen werden vermutlich durch den Biss der scharfen Zähne, durch Substanzen der Blutegel oder durch infektiöse Erreger, die während der Behandlung übertragen werden, bedingt [6, 8]. Als möglicher Pathomechanismus wird eine verzögerte Hypersensitivitätsreaktion auf Bestandteile der Insekten diskutiert [3]. In der Literatur wurden selten sowohl irritative als auch allergische Kontaktdermatitiden nach medizinischer Blutegeltherapie beschrieben [13]. Hirudin kommt als ein mögliches, auslösendes Agens in Betracht [13]. Die definitive Identifikation des auslösenden Agens ist bei mehr als 100 nachgewiesenen Proteinen mit einem molekularen Gewicht zwischen 10 und 97 kD im Speichelsekret der Blutegel allerdings schwierig [13].
Auch für erfahrene Mediziner ist die Diagnose eines Pseudolymphoms oftmals eine Herausforderung und erfordert nicht selten die Korrelation aller Befunde – der Klinik, der Histologie, der Immunhistochemie und der Molekularpathologie. Es ist zu erwarten, dass mit zunehmender Anwendung der Blutegeltherapie in unterschiedlichen Bereichen der Medizin auch die kutanen Nebenwirkungen häufiger beobachtet werden. Daher sollte bei der differenzialdiagnostischen Abklärung von Pseudolymphomen auch diese seltene Ursache bedacht werden.
Fazit für die Praxis
Auch für erfahrene Mediziner ist die Diagnose eines Pseudolymphoms oftmals eine Herausforderung und erfordert nicht selten die Korrelation aller Befunde – der Klinik, der Histologie, der Immunhistochemie und der Molekularpathologie.
Es ist zu erwarten, dass mit zunehmender Anwendung der Blutegeltherapie in unterschiedlichen Bereichen der Medizin auch die kutanen Nebenwirkungen häufiger beobachtet werden. Daher sollte bei der differenzialdiagnostischen Abklärung von Pseudolymphomen auch diese seltene Ursache bedacht werden.
Author Contribution
Alle Autoren hatten vollen Zugang zu den publizierten Daten und tragen die Verantwortung für deren Richtigkeit. Alle Autoren haben bei der Erstellung des Manuskriptes mitgewirkt.
Funding
Open Access funding enabled and organized by Projekt DEAL.
Einhaltung ethischer Richtlinien
Interessenkonflikt
S. Hanner, H. Stroh, A. Enk und J. Hoffmann geben an, dass kein Interessenkonflikt besteht.
Für diesen Beitrag wurden von den Autoren keine Studien an Menschen oder Tieren durchgeführt. Für die aufgeführten Studien gelten die jeweils dort angegebenen ethischen Richtlinien. Für Bildmaterial oder anderweitige Angaben innerhalb des Manuskripts, über die Patienten zu identifizieren sind, liegt von ihnen und/oder ihren gesetzlichen Vertretern eine schriftliche Einwilligung vor.
Literatur
- 1.Sander CA, Flaig MJ. Pseudolymphome. In: Plewig G, Ruzicka T, Kaufmann R, Hertl M, editors. Braun-Falco’s Dermatologie, Venerologie und Allergologie. Berlin, Heidelberg: Springer; 2018. pp. 1937–1943. [Google Scholar]
- 2.Mitteldorf C, Kempf W. Cutaneous pseudolymphoma—A review on the spectrum and a proposal for a new classification. J Cutan Pathol. 2020;47(1):76–97. doi: 10.1111/cup.13532. [DOI] [PubMed] [Google Scholar]
- 3.Choi Y, Kim S-C. Cutaneous pseudolymphoma induced by Hirudo medicinalis therapy. J Dermatol. 2012;39(2):195–197. doi: 10.1111/j.1346-8138.2011.01263.x. [DOI] [PubMed] [Google Scholar]
- 4.Tupikowska M, Woźniak Z, Wojciechowska-Zdrojowy M, Maj J, Jankowska-Konsur A. Hirudotherapy—a rare cause of pseudolymphoma. Postepy Dermatol Alergol. 2018;35(2):225–226. doi: 10.5114/ada.2018.75250. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 5.Temiz SA, Özer İ, Ataseven A, Dursun R, Fındık S. Cutaneous Pseudolymphoma Due to Hirudotherapy. Turk J Parasitol. 2019;43(1):50–52. doi: 10.4274/tpd.galenos.2018.6037. [DOI] [PubMed] [Google Scholar]
- 6.Khelifa E, Kaya G, Laffitte E. Cutaneous pseudolymphomas after leech therapy. J Dermatol. 2013;40(8):674–675. doi: 10.1111/1346-8138.12198. [DOI] [PubMed] [Google Scholar]
- 7.Altamura D, Calonje E, li Liau J, Rogers M, Verdolini R. Diffuse cutaneous pseudolymphoma due to therapy with medicinal leeches. JAMA Dermatol. 2014;150(7):783–784. doi: 10.1001/jamadermatol.2013.8066. [DOI] [PubMed] [Google Scholar]
- 8.Smolle J, Cerroni L, Kerl H. Multiple pseudolymphomas caused by Hirudo medicinalis therapy. J Am Acad Dermatol. 2000;43(5 Pt 1):867–869. doi: 10.1067/mjd.2000.110043. [DOI] [PubMed] [Google Scholar]
- 9.Sadati MS, Rezaee M, Ghafarpur S, Aslani FS, Dastgheib L, Jahankhah R. Cutaneous lymphoid hyperplasia induced by Hirudo medicinalis (leeches) J Complement Integr Med. 2019 doi: 10.1515/jcim-2016-0056. [DOI] [PubMed] [Google Scholar]
- 10.Aktas H, Hamidi A, Ertuğrul G, Erol H. A case of cutaneous pseudolymphoma induced by medicinal leech application and review of the literature. Arch. Clin Exp Med. 2018;3:198–200. [Google Scholar]
- 11.Sepaskhah M, Yazdanpanah N, Aslani FS, Jahromi MA. Cutaneous pseudolymphoma as a rare adverse effect of medicinal leech therapy: a case report and review of the literature. Cureus. 2020 doi: 10.7759/cureus.7517. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 12.Sig AK, Guney M, Uskudar Guclu A, Ozmen E. Medicinal leech therapy—an overall perspective. Integr Med Res. 2017;6(4):337–343. doi: 10.1016/j.imr.2017.08.001. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 13.Pietrzak A, Kanitakis J, Tomasiewicz K, Wawrzycki B, Kozłowska-Łój J, Dybiec E, et al. Cutaneous complications of improper leech application. Ann Agric Environ Med. 2012;19(4):790–792. [PubMed] [Google Scholar]