Abstract
Hintergrund
Infektionen mit antibiotikaresistenten Bakterien stellen eine hohe Gesundheitsbelastung dar, da sie mit erhöhter Letalität assoziiert sind und längerfristige dramatische Beeinträchtigungen der Lebensqualität hervorrufen können. In Deutschland erkranken jährlich etwa 54.500 Menschen an Infektionen durch antibiotikaresistente Erreger, von denen etwa 2400 Menschen versterben. Infektionen mit multiresistenten gramnegativen Bakterien (MRGN), insbesondere mit carbapenemresistenten Erregern, stellen ein besonderes Risiko dar, da nur eine begrenzte Zahl an Therapieoptionen verfügbar ist.
Fragestellung
Wie sind die Ergebnisse aus Studien und Compassionate-Use-Programm mit dem neuen Siderophorantibiotikum Cefiderocol, das im April 2020 von der Europäischen Arzneimittel-Agentur (EMA) bei Erwachsenen zur Behandlung von Infektionen durch aerobe gramnegative Erreger zugelassen wurde, wenn nur begrenzte Behandlungsmöglichkeiten zur Verfügung stehen? Die Zulassung ist pathogenbasiert und fokusunabhängig [5].
Ergebnisse
Cefiderocol, das über einen innovativen Zelleintrittsmechanismus verfügt, ist als erstes β‑Laktam-Antibiotikum aus der Gruppe der Cephalosporine stabil gegenüber allen klinisch relevanten β‑Laktamasen, einschließlich Carbapenemasen, und hat eine hohe In-vitro-Wirksamkeit gegenüber carbapenemresistenten MRGN. Die Ergebnisse werden durch klinische Studien bei komplizierten Harnwegsinfektionen, nosokomialer Pneumonie/Beatmungspneumonie und schweren Infektionen durch carbapenemresistente Erreger bestätigt.
Fazit
Klinische Studiendaten sowie die Ergebnisse aus den weltweiten Erfahrungsberichten zeigen, dass Cefiderocol eine vielversprechende Behandlungsoption für schwere Infektionen durch multiresistente, insbesondere carbapenemresistente gramnegative Bakterien darstellt.
Schlüsselwörter: Kritisch kranke Patienten, Pseudomonas aeruginosa, 4MRGN, Enterobacterales, Siderophor-Cephalosporin
Abstract
Background
Infections due to antibiotic-resistant bacteria are threatening modern healthcare, and antibacterial resistance has become one of the greatest threats to public health. In Germany 54,500 patients become infected with antibiotic-resistant bacteria per year, causing about 2400 attributable deaths. Rising resistance in Gram-negative bacteria especially carbapenem-resistant pathogens is of particular concern due to the lack of effective and safe alternative treatment options.
Objective
The results from trials and compassionate-use programs with the new antibiotic cefiderocol, which was approved by the European Medicines Agency (EMA) in April 2020 for the treatment of adults with infections caused by aerobic Gram-negative bacteria, are summarized.
Results
The new β‑lactam antibiotic cefiderocol is the first siderophore cephalosporin indicated for the treatment of infections due to aerobic Gram-negative organisms in adults with limited treatment options. Its chemical structure and its unique mechanism of action confer enhanced stability against β‑lactamases including all classes of clinically relevant carbapenemases. In vitro data show high antibacterial activity against multidrug resistant Gram-negative bacteria, Enterobacterales and nonfermenters, including carbapenem-resistant strains. In clinical trials, cefiderocol showed superiority in complicated urinary tract infection in comparison to imipenem and non-inferiority versus meropenem in hospital-acquired/ventilator-associated pneumonia patients and severe infections caused by carbapenem-resistant pathogens.
Conclusion
Clinical trial data and case reports identified in the literature search show that cefiderocol is a promising treatment option for severe infections caused by drug-resistant Gram-negative bacteria, particularly carbapenem-resistant bacteria.
Keywords: Critically ill patients, Pseudomonas aeruginosa, XDR, Enterobacterales, Siderophore-Cephalosporin
Hintergrund
Multiresistente gramnegative Bakterien (MRGN), deren Inzidenz seit Jahren zunimmt, können schwere Infektionen mit hoher Morbidität und Letalität verursachen, da routinemäßig eingesetzte und klinisch etablierte Antibiotika häufig nicht mehr ausreichend wirksam sind [2, 4]. Besonders kritisch ist der Resistenzanstieg gegenüber Carbapenemen, die lange Zeit eine sichere (oftmals letzte) Option bei schweren MRGN-Infektionen waren. Die Weltgesundheitsorganisation (WHO) hat Infektionen durch carbapenemresistente Enterobacteriaceae (Enterobacterales/CRE), Pseudomonas aeruginosa und Acinetobacter baumannii daher als besonders kritisch bewertet [23].
Carbapenemresistente Enterobacterales (CRE), Pseudomonas aeruginosa und Acinetobacter baumannii
Wie Veröffentlichungen des Robert Koch-Instituts (RKI) zeigen, hat sich auch in Deutschland die Zahl der Infektionen durch carbapenemresistente gramnegative Bakterien im Verlauf der Jahre deutlich erhöht [9, 18]. Multiresistente gramnegative Bakterien verfügen über eine Vielzahl an unterschiedlichen Resistenzmechanismen. Hierzu gehören diverse β‑Laktamasen, Veränderungen der Porinkanäle sowie bakterielle Effluxpumpen, die das Antibiotikum aktiv aus der Bakterienzelle herauspumpen können [3, 4]. Wenngleich die antibiotische Pipeline eine Reihe an neuen Substanzen hervorgebracht hat, die bestimmte multiresistente GN-Erreger besser erfassen (z. B. Ceftolozan-Tazobactam für multiresistente Pseudomonas aeruginosa und Ceftazidim-Avibactam für KPC- und „OXA-48-like“ produzierende Enterobacterales), bestehen weiterhin Lücken bei Erregern, die Metallocarbapenemasen (NDM, VIM, IMP u. a.) produzieren, oder solchen, die multiple Resistenzmechanismen vorweisen (Tab. 1). Gleiches gilt für die neuen β‑Laktam-β-Laktamase-Inhibitor-Kombinationen Meropenem-Vaborbactam und Imipenem-Relebactam (Tab. 1; [8]). Zunehmend Probleme bereiten Carbapenem-Resistenzen, die nicht Carbapenemase-bedingt sind wie Mutationen, die wichtige Porinkanäle in der äußeren Membran verschließen oder eine Überproduktion von Effluxpumpen. Das Wirkspektrum der Cephalosporin-Inhibitor-Kombinationen umfasst zudem nicht Stenotrophomonas maltophilia und Burkholderia cepacia, die ebenfalls mit hohen Resistenzen gegenüber vielen Antibiotika assoziiert sind. Mit Cefiderocol steht ein neues β‑Laktam-Antibiotikum aus der Gruppe der Cephalosporine zur Verfügung, das diese Resistenzmechanismen überwindet und die bestehenden Wirklücken schließen kann (Tab. 1; [8, 26]).
| In-vitro-Wirksamkeit | ||||||||
|---|---|---|---|---|---|---|---|---|
| Enterobacteriaceae/Enterobacterales | P. aeruginosa | A. baumannii | S. maltophilia | Indikationen (inkl. erwartete) | Erregerfokussierte Studie (inkl. erwartet) | |||
| Antibiotikum | Klasse-A-Carbapenemase (z. B. KPC) |
Klasse-B-Carbapenemase (z. B. NDM) | Klasse-D-Carbapenemase (z. B. OXA-48) | |||||
| Ceftazidim-Avibactam | Ja | Nein | Ja | Ja | Nein | Nein | cUTI/AP, cIAI, HABP/VABP | Nein |
| Ceftolozan-Tazobactam | Nein | Nein | Nein | Ja | Nein | Nein | cUTI/AP, cIAI, NP | Nein |
| Meropenem-Vaborbactam | Ja | Nein | Nein | Neina | Nein | Nein | cUTI/AP | Ja |
| Imipenem-Cilastatin-Relebactam | Ja | Nein | Nein | Ja | Nein | Nein | cUTI/AP, cIAI, HABP/VABP | Ja |
| Cefiderocol | Ja | Ja | Ja | Ja | Ja | Ja | cUTI/AP, HABP/VABP | Ja |
| Fosfomycin | Ja | Ja | Ja | Variabel | Nein | Nein | cUTI/AP | Nein |
A. baumannii Acinetobacter baumannii, AP akute Pyelonephritis, cIAI komplizierte intraabdominelle Infektion, cUTI komplizierte Harnwegsinfektion, HABP nosokomiale bakterielle Pneumonie, KPC Klebsiella-pneumoniae-Carbapenemase, NDM New-Delhi-Metallo-β-Laktamase, NP nosokomiale Pneumonie, OXA Oxacillinase, P. aeruginosa Pseudomonas aeruginosa, S. maltophilia Stenotrophomonas maltophilia, VABP beatmungsassoziierte bakterielle Pneumonie
aNicht wirksam im Vergleich zu Meropenem allein
Wirkmechanismus von Cefiderocol und Überwindung bakterieller Resistenzmechanismen
Das neue Cephalosporin Cefiderocol ist der erste zugelassene Vertreter der neuartigen Siderophorantibiotika mit einer Katecholeinheit und verfügt aufgrund seiner chemischen Struktur über einen einzigartigen Zelleintrittsmechanismus. Bakterien haben einen natürlichen Eisenbedarf für intrazelluläre Stoffwechselprozesse und können endogene Siderophore aussenden, um extrazelluläres 3‑wertiges Eisen aufzunehmen. Die Katecholgruppe des Cefiderocolmoleküls erfüllt diese Funktion als ein eisenbindendes Siderophor, sodass Cefiderocol mithilfe eines aktiven bakteriellen Fe3+-Transportsystems aktiv in das Zellinnere gramnegativer Bakterien eingeschleust werden kann und hohe Cefiderocolkonzentrationen im periplasmatischen Raum erzielt werden. Ungehindert kann es an die in der Zytoplasmamembran lokalisierten penizillinbindenden Proteine (PBP) binden, dadurch die Zellwandsynthese inhibieren und den Bakterienzelltod herbeiführen. Cefiderocol verhält sich somit wie ein „Trojanisches Pferd“. Aufgrund des siderophorvermittelten Einschleusens von Cefiderocol in die Zelle haben ein Porinverlust oder eine effluxvermittelte Resistenz bei Cefiderocol generell geringere Auswirkungen auf die In-vitro-Aktivität als bei vielen anderen β‑Laktam-Antibiotika. Durch Seitenketten in Position 3 und in Position 7 wird darüber hinaus eine besonders hohe Stabilität gegenüber β‑Laktamasen einschließlich Serin (KPC, OXA), Metallocarbapenemasen (NDM, VIM, IMP) und Carbapenemasen erzielt [8, 11, 25]. Internationale Surveillance-Studien belegen eine hohe In-vitro-Wirksamkeit von Cefiderocol gegenüber einem breiten Spektrum gramnegativer, aerober Infektionserreger einschließlich carbapenemresistenter Stämme. Hierzu gehören Enterobacterales (z. B. Klebsiella spp., E. coli, Enterobacter spp., Proteus spp. Morganella spp., Citrobacter spp., Serratia spp.), weiterhin die Nonfermenter Pseudomonas aeruginosa, Acinetobacter baumannii, Burkholderia cepacia und Stenotrophomonas maltophilia [5, 7, 10, 20].
Aufgrund zunehmender Resistenzen bei gramnegativen Erregern erfüllt Cefiderocol einen wichtigen „medical need“ bei
MRGN mit Effluxpumpenhochregulation und Porinkanalveränderungen;
Metallo-β-Laktamase‑, KPC- und vielen OXA-Carbapenemase-Produzenten;
multiresistenten Erregern einschließlich 4MGRN, wie Pseudomonas aeruginosa, Acinetobacter baumannii und Klebsiella pneumoniae;
intrinsisch β‑Laktam-resistenten Stenotrophomonas maltophilia.
Dosierung und PK/PD bei kritisch kranken Patienten
Kürzlich publizierte Daten weisen darauf hin, dass die Dosierungsempfehlungen für Cefiderocol [5] zu angemessenen Spiegeln im Plasma und in der Epithelflüssigkeit führen. König et al. untersuchten jetzt die PK/PD-Eigenschaften der Substanz bei kritisch kranken Patienten mit septischem Schock und Nierenversagen (einschließlich kontinuierlicher Nierenersatztherapie und Zytokinadsorbertherapie), die mit Cefiderocol unter Bedingungen des klinischen Alltags behandelt wurden. Ursächliche Erreger waren multiresistente Pseudomonas aeruginosa und multiresistente Acinetobacter baumannii. Die Dosierungsanweisungen des Herstellers gemäß Fachinformation waren ausreichend, um einen Wirkstoffspiegel deutlich über der MHK dieser Erreger zu erreichen. Der Zusatz eines Zytokinadsorbers könnte jedoch die Serumspiegel erheblich senken, sodass in diesem Zusammenhang eine therapeutische Überwachung und eine Dosisanpassung empfohlen werden. Im Rahmen dieser Untersuchung konnte trotz der besonderen Schwere der Erkrankung bei 60 % der Patienten ein mikrobiologischer bzw. klinischer Erfolg erzielt werden [12].
Klinische Wirksamkeit in Phase-III-Zulassungsstudien
Komplizierte Harnwegsinfektionen (APEKS-cUTI) durch gramnegative Erreger mit oder ohne Pyelonephritis
Im Rahmen der APEKS-cUTI (Acinetobacter baumannii, Pseudomonas aeruginosa, Escherichia coli, Klebsiella pneumoniae und Stenotrophomonas maltophilia bei Patienten mit komplizierten Harnwegsinfektionen) einer multizentrischen randomisierten Doppelblindstudie wurde die klinische Wirksamkeit von Cefiderocol (3-mal 2 g als Infusion über eine Stunde) bei Patienten mit komplizierten Harnwegsinfektionen (cUTI) durch gramnegative Erreger und/oder akuter unkomplizierter Pyelonephritis (AUP) bei 371 Patienten (MITT-Population) untersucht.
Die Studie war statistisch darauf ausgelegt, die Nichtunterlegenheit von Cefiderocol nachzuweisen. Eine Post-hoc-Analyse zeigte die Überlegenheit von Cefiderocol, das der Vergleichsmedikation Imipenem/Cilastatin sowohl hinsichtlich des primären Zielkriteriums (klinischer und mikrobiologischer Erfolg bei der MITT-Population) als auch bezüglich des sekundären Zielkriteriums (mikrobiologischer Erfolg beim Zeitpunkt „test of cure“ in der MITT-Population) überlegen war [19].
Nosokomiale Pneumonie und Beatmungspneumonie APEKS-NP
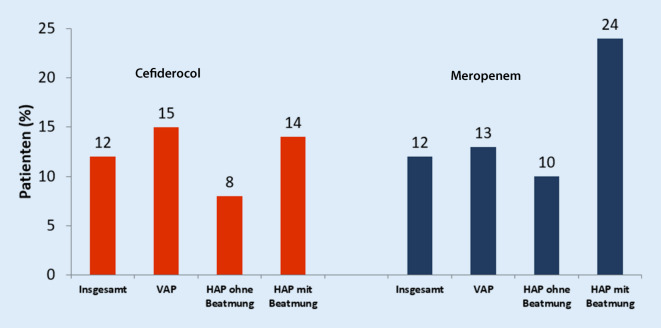
Die Wirksamkeit von Cefiderocol bei nosokomialer Pneumonie (HAP) und ventilatorassoziierter Pneumonie (VAP) durch gramnegative Erreger wurde in der APEKS-NP-Zulassungsstudie, einer internationalen multizentrischen randomisierten Nichtunterlegenheitsdoppelblindstudie, klinisch geprüft. Cefiderocol (2 g als prolongierte Infusion über 3 h alle 8 h) wurde mit einer Meropenemhochdosistherapie (3-mal 2 g) als „extended infusion“ ebenfalls über 3 h verglichen, um nach Expertenbewertung die Meropenemwirkung bei schwer kranken Patienten zu optimieren. Im Gegensatz dazu waren die HAP/VAP-Zulassungsstudien REPROVE (mit Ceftazidim-Avibactam) und ASPECT-NP (mit Ceftolozan-Tazobactam) gegen jeweils nur 1 g Meropenem (3-mal täglich) als Kurzinfusion über 30 bzw. 60 min durchgeführt worden [13, 21, 24]. Die Cefiderocolbehandlung und die Meropenemhochdosisbehandlung erfolgten für 7–14 Tage. Linezolid wurde in beiden Armen für mindestens 5 Tage verabreicht, um methicillinresistente Staphylococcus aureus (MRSA) und andere grampositive Bakterien abzudecken. Insgesamt wurden 300 Patienten in die Studie aufgenommen (Cefiderocol n = 148, Meropenem n = 152), von denen ungefähr zwei Drittel aus Europa stammten. 60 % der Patienten wurden maschinell beatmet; 68 % waren Intensivpatienten bei Randomisierung und 49 % hatten einen APACHE-II-Score ≥ 16 [24]. Häufigste Erreger waren Klebsiella pneumoniae, Pseudomonas aeruginosa, Acinetobacter baumannii, E. coli und Enterobacter cloacae. Der Anteil der mITT-Patienten mit dem Infektionsstatus „schwer“ war höher in der Cefiderocolgruppe (49 %) im Vergleich zur Meropenemgruppe (33 %). Cefiderocol erreichte den primären Endpunkt der Nichtunterlegenheit im Vergleich zu einer Meropenemhochdosistherapie (verabreicht als „extended infusion“) bezüglich der 14-Tage-Gesamtmortalität in der mITT-Population nach Beginn der Studienmedikamentengabe. Bei HAP-Patienten mit Beatmung lag die Gesamtmortalität in der Cefiderocolgruppe mit 14 % numerisch niedriger als in der Hochdosismeropenemgruppe mit „extended infusion“ (24 %; Abb. 1; [24]).
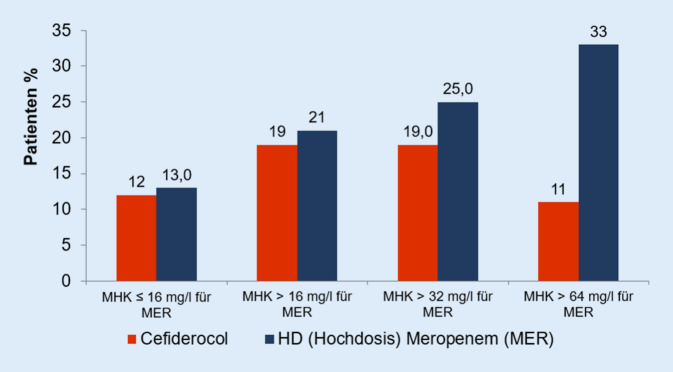
Die Gesamtmortalität an Tag 28 (21,0 % vs. 21,0 %) war vergleichbar in beiden Gruppen, ebenso die klinischen Heilungsraten (65 % vs. 67 %; [24]). Unter Berücksichtigung der mikrobiologisch auswertbaren Patienten (ME-Population) lag die Gesamtmortalität bei 12,4 % in der Cefiderocolgruppe und bei 13 % in der Meropenemgruppe [16]. Eine weitere Auswertung berücksichtigte nur Patientendaten, bei denen ein Erreger isoliert wurde und zusätzlich die minimale Hemmkonzentration (MHK) bestimmt wurde (Abb. 2).
Bei Infektionen durch Erreger mit Meropenemresistenz und höheren Meropenem-MHK-Werten blieben sowohl die Erregereradikationsraten als auch die Gesamtmortalität unter der Cefiderocolbehandlung gleich, wohingegen unter der Meropenembehandlung die Eradikationsraten zurückgingen und die Gesamtletalität anstieg (Abb. 2; [24]).
APEKS-NP ist die bisher einzige Vergleichsstudie gegen Hochdosismeropenem mit verlängerter Infusionszeit und belegt die klinische Wirksamkeit von Cefiderocol auch bei carbapenemresistenten gramnegativen Erregern [24].
CREDIBLE-CR: schwere Infektionen mit carbapenemresistenten Erregern
CREDIBLE-CR ist eine deskriptive, nichtinferentielle, offene, nichtvergleichende, multizentrische, multinationale Studie bei schwerstkranken Patienten mit nosokomialer Pneumonie einschließlich ventilatorassoziierter Pneumonie (HAP/VAP/HCAP), komplizierten Harnwegsinfektionen (cUTI) oder Blutstrominfektionen (BSI) und Sepsis durch carbapenemresistente (CR) gramnegative Erreger. Die Patienten wurden in dieser erregerfokussierten Studie entweder mit Cefiderocol oder der besten verfügbaren Therapie („best available therapy“, BAT) behandelt. Da es sich um kritisch kranke Patienten handelte (vergleichbar mit Compassionate Use), konnten die behandelnden Ärzte bei BAT bis zu 3 verschiedene geeignete Antibiotika für gramnegative Erreger frei kombinieren. Bei Cefiderocol war nur ein weiteres, gegenüber gramnegativen Erregern wirksames Antibiotikum erlaubt [1].
Die überwiegende Mehrheit der Patienten in der Cefiderocolgruppe erhielt eine Cefiderocolmonotherapie (83 %), die überwiegende Mehrheit in der BAT-Gruppe (71 %) eine Kombinationstherapie, überwiegend basierend auf Colistin mit anderen Reserveantibiotika in Zweier- oder Dreierkombination (Tab. 2).
| Cefiderocolgruppe1 | BAT-Gruppe1 | |
|---|---|---|
| Patient auf ICU bei Einschluss | ||
| Alle | 56 %a | 43 %a |
| Acinetobacter-Infektionen | 81 %b | 47 %b |
| Septischer Schock in Vorgeschichte oder bei Randomisierung | 19 %a | 12 %a |
| 26 %b | 6 %b | |
| Anzahl Acinetobacter | 37 | 17 |
| Anzahl Stenotrophomonas | 5 | 0 |
| Alter | ≥ 65: 63 % | ≥ 65: 45 % |
| Antibiotikamonotherapie | 83 % | 29 % |
| Kreatininclearance < 30 | 20 % | 14 % |
| Mortalität CRE2 | 13,8 % | 27,3 % |
| Klinische Heilung CRE1 | 66 % | 45 % |
| Klinische Heilung MBL-Bildner3 | 75 % | 29 % |
| Mortalität bei Pseudomonas4 | 13 % | 22 % |
| Klinische Heilung Pseudomonas4 | 75 % | 55 % |
| Therapiebedingte Nebenwirk.1 | ||
| Alle | 15 % | 22 % |
| Schwere | 1 % | 10 % |
Primäres Zielkriterium war die klinische Heilungsrate beim Zeitpunkt „test of cure“ (TOC) bei Patienten mit HAP/VAP/HCAP, BSI/Sepsis und das mikrobiologische Ansprechen bei Patienten mit cUTI [1].
In den beiden Behandlungsgruppen gab es zum Zeitpunkt der Randomisierung beträchtliche Unterschiede (Tab. 2, oben). Im Vergleich zu den mit BAT behandelten Patienten war ein größerer Anteil der mit Cefiderocol behandelten Patienten ≥ 65 Jahre alt und befand sich bei Randomisierung auf der Intensivstation und/oder hatte einen septischen Schock (oder mit Vorgeschichte, 31 Tage). Weiterhin war die Verteilung der zugrunde liegenden Pathogene (Stenotrophomonas maltophilia) nicht ausgeglichen, da diese kein Kriterium der Stratifizierung darstellten.
34 (34 %) von 101 Patienten, die Cefiderocol erhielten, und 9 (18 %) von 49 Patienten in der BAT-Gruppe starben bis zum Ende der Studie; einer dieser Todesfälle (in der BAT-Gruppe) wurde mit dem Studienmedikament in Verbindung gebracht [1]. Die beobachtete Mortalität in der Cefiderocolgruppe war so, wie man sie in der Patientenpopulation erwarten würde und wie sie in anderen vergleichbaren Studien beobachtet wurde. Die in der BAT-Gruppe beobachtete Mortalität war jedoch auffällig niedriger als erwartet und/oder in anderen Studien beobachtet [1, 14]).
Nonfermenter Acinetobacter baumannii
Subgruppenanalysen zeigten, dass der beobachtete Mortalitätsunterschied primär bei Infektionen mit Beteiligung von CR Acinetobacter spp. bestand.
In dieser an Acinetobacter-Infektionen erkrankten Patientengruppe gab es bei Randomisierung in der Cefiderocolgruppe mit 26 % einen höheren Anteil an Patienten mit septischem Schock (oder mit Vorgeschichte, 31 Tage) im Vergleich zu Patienten in der BAT-Gruppe mit 6 %. Des Weiteren befanden sich in der Cefiderocolgruppe 81 % dieser Patienten bei Randomisierung auf der Intensivstation im Vergleich zu nur 47 % in der BAT-Gruppe (Tab. 2; [1]).
Nonfermenter Pseudomonas aeruginosa
Die Mortalität bei Infektionen mit CR Pseudomonas aeruginosa (ohne Acinetobacter-Beteiligung) war 13 % in der Cefiderocolgruppe vs. 22 % in der BAT-Gruppe (Tab. 2; [15]).
CR Enterobacterales (CRE)
Die Gesamtmortalität bei CRE-Infektionen war niedriger bei Patienten, die mit Cefiderocol behandelt wurden (13,8 % [C] vs. 27,3 % [BAT]; Tab. 2; [14]).
Weitere Studienergebnisse
Alle Unterschiede waren numerisch und nicht signifikant.
Die klinische Heilung (primäres Zielkriterium der Studie) betrug in der Cefiderocolgruppe (C) 53 % und in der BAT-Gruppe (BAT) 50 %. Indikationsspezifische Heilungsraten bei HAP, VAP oder HCAP lagen bei 50 % (C) vs. 53 % (BAT), bei Blutstrominfektionen (BSI) oder Sepsis bei 43 % (C) vs. 43 % (BAT) und bei cUTI 71 % (C) vs. 60 % (BAT; [1]).
Bei Infektionen mit carbapenemresistenten Erregern (CRE) wurde eine höhere Heilungsrate in der Cefiderocolgruppe erzielt als in der BAT-Gruppe (66 % vs. 45 %). Bei Nonfermentern waren sie in beiden Gruppen ähnlich. Bei Infektionen mit Metallo-β-Laktamasen(MBL)-bildenden Erregern lagen die klinischen Heilungsraten bei 75 % in der Cefiderocolgruppe und bei 29 % in der BAT-Gruppe (Tab. 2; [1]).
Fazit der Autoren
Die offene erregerfokussierte CREDIBLE-CR-Studie belegt die Wirksamkeit und Sicherheit von Cefiderocol bei schweren Infektionen bei Hochrisikopatienten durch carbapenemresistente gramnegative Erreger in einer sehr heterogenen Patientenpopulation mit meist komplexen Grunderkrankungen [1]. In den beiden Behandlungsgruppen gab es zum Zeitpunkt der Randomisierung beträchtliche Unterschiede (Tab. 2).
Cefiderocolverträglichkeit
Die bisher ausgewerteten klinischen Studien und Daten aus dem klinischen Alltag bestätigen für Cefiderocol die vielfach dokumentierte gute Verträglichkeit der β‑Laktam-Antibiotika [5]. Dies ist gerade bei Patienten mit schweren Infektionen von besonderer Bedeutung, da diese oftmals multimorbide sind, besondere Risikofaktoren haben, mehrere Medikamente erhalten und häufig auf der Intensivstation behandelt werden. Nach Expertenbewertung sollte unter diesem Aspekt ein β‑Laktam-Antibiotikum bei gleicher In-vitro-Wirksamkeit vor allen anderen Antibiotikaklassen bevorzugt eingesetzt werden [22]. Cefiderocol bleibt trotz Siderophoranteil ohne Einfluss auf den Eisenstoffwechsel. Die Eisenhomöostase des Körpers wird nicht verändert [19]. Bei Patienten mit Nierenfunktionsstörung erfolgt eine Dosisanpassung [5].
Compassionate-Use-Programm und weitere Ergebnisse aus dem klinischen Alltag
Der erfolgreiche Einsatz von Cefiderocol im klinischen Alltag wurde u. a. im Rahmen des Compassionate-Use-Programms dokumentiert [6, 26]. Behandelt wurden Patienten mit sehr schweren Infektionen durch multiresistente oder XDR Erreger:
Aortenklappenendokarditis mit XDR Pseudomonas aeruginosa bei rektaler Kolonisation mit OXA-48 Klebsiella pneumoniae und OXA-23/OXA-51 Acinetobacter baumannii;
Blutstrominfektionen und Beatmungspneumonien durch XDR Acinetobacter baumannii und carbapenemasebildende Klebsiella pneumoniae;
schwere intraabdominelle Infektion durch multiresistente Pseudomonas aeruginosa;
neutropenischer Patient mit chronischer Osteomyelitis durch multiresistente Pseudomonas aeruginosa;
Polytraumapatient mit früher postoperativer implantatassoziierter Infektion mit Acinetobacter baumannii (NDM, OXA-40) ;
Traumapatient mit nosokomialer Pneumonie durch Klebsiella pneumoniae und XDR Acinetobacter baumannii;
Patienten mit polymikrobieller Osteomyelitis (nach mehreren operativen Débridements infolge eines Traumas) und schwerer XDR Acinetobacter-baumannii-Infektion.
Alle Patienten waren vorbehandelt, in erster Linie mit Kombinationen aus Colistin und einem Carbapenem und/oder anderen Antibiotika. Die Umstellung auf Cefiderocol erfolgte aufgrund mangelnden klinischen Ansprechens oder einer Verschlechterung unter der Kombinationstherapie bzw. aufgrund von Nebenwirkungen (z. B. Nierenversagen unter Colistin und Erhöhung der Leberparameter unter Aztreonam; [26]).
Pascale et al. berichten über eine multizentrische Beobachtungsstudie bei 107 Intensivpatienten mit schweren COVID-19-Infektionen und der Diagnose carbapenemresistente Acinetobacter-baumannii-Infektion, überwiegend Infektionen des Blutstroms und der unteren Atemwege. Alle 42 Patienten in der Cefiderocolgruppe (100 %) erhielten eine Monotherapie, Colistin wurde überwiegend (82 %) als Kombinationstherapie verabreicht. Die 28-Tage-Gesamtmortalität lag bei 57 % ohne Unterschiede zwischen den Gruppen (Cefiderocol 55 % vs. Colistin 58 %, p = 0,70). In der multivariablen Analyse war der SOFA-Score der unabhängige Risikofaktor für die Sterblichkeit (HR 1,24; 95 %-KI 1,15–1,38; p < 0,001; [17]). Cefiderocol war mit einem nichtsignifikant niedrigeren Mortalitätsrisiko verbunden (HR 0,64; 95 %-KCI 0,38–1,08; p = 0,10; [17]).
Fazit für die Praxis
Die Studienergebnisse sowie die Ergebnisse aus dem weltweiten Compassionate-Use-Programm und dem klinischen Alltag weisen darauf hin, dass Cefiderocol eine vielversprechende Behandlungsoption für schwere Infektionen durch multiresistente, insbesondere carbapenemresistente gramnegative Bakterien (Enterobacterales, Pseudomonas aeruginosa und Acinetobacter baumannii) ist, wenn nur begrenzte Behandlungsoptionen zur Verfügung stehen [5, 26]. Das In-vitro-Wirkspektrum von Cefiderocol umfasst alle wichtigen aeroben gramnegativen Erreger einschließlich der WHO(„World Health Organisation“)-Problemkeime. Vorteile sind auch die gute Verträglichkeit und das geringe Interaktionspotenzial. Der Einsatz sollte in erster Linie als gezielte Therapie erfolgen.
Funding
Die Erstellung des Beitrags wurde von der Firma Shionogi unterstützt.
Einhaltung ethischer Richtlinien
Interessenkonflikt
O. Witzke erhielt Forschungszuschüsse für klinische Studien, Referentenhonorare sowie Honorare und Reisekostenübernahmen von den Firmen Amgen, Alexion, Astellas, Basilea, Biotest, Bristol-Myers Squibb, Correvio, Chiesi, Gilead, Hexal, Janssen, Dr. Franz Köhler Chemie, MSD, Novartis, Roche, Pfizer, Sanofi, TEVA und UCB. T. Brenner erhielt Honorare für Vorträge, Präsentationen, Manuskripterstellungen oder Bildungsveranstaltungen von den Firmen CSL Behring GmbH, Schöchl Medical Education GmbH, Biotest AG, Baxter Deutschland GmbH, Boehringer Ingelheim Pharma GmbH, Astellas Pharma GmbH, B. Braun Melsungen AG und MSD Sharp & Dohme GmbH. Er war Teilnehmer des Data Safety Monitoring Board bzw. Advisory Board der Baxter Deutschland GmbH. Er erhielt Forschungsförderungen durch die Deutsche Forschungsgemeinschaft (DFG), die Dietmar Hopp Stiftung, Stiftung Universitätsmedizin Essen; die Heidelberger Stiftung Chirurgie und den Innovationsfonds des Gemeinsamen Bundesausschusses (G-BA).
Für diesen Beitrag wurden von den Autoren keine Studien an Menschen oder Tieren durchgeführt. Für die aufgeführten Studien gelten die jeweils dort angegebenen ethischen Richtlinien.
Footnotes

QR-Code scannen & Beitrag online lesen
Literatur
Verwendete Literatur
- 1.Bassetti M, Echols R, et al. Efficacy and safety of cefiderocol or best available therapy for the treatment of serious infections caused by carbapenem-resistant Gram-negative bacteria (CREDIBLE-CR): a randomised, open-label, multicentre, pathogen-focused, descriptive, phase 3 trial. Lancet. 2020 doi: 10.1016/S1473-3099(20)30796-9. [DOI] [PubMed] [Google Scholar]
- 2.Brolund A, EURGen-Net capacity survey group Worsening epidemiological situation of carbapenemase-producing Enterobacteriaceae in Europe, assessment by national experts from 37 countries, July 2018. Eur Commun Dis Bull. 2019;24(9):1900123. doi: 10.2807/1560-7917.ES.2019.24.9.1900123. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 3.Bush K. Past and present perspectives on β-lactamases. Antimicrob Agents Chemother. 2018;62(10):e01076-18. doi: 10.1128/AAC.01076-18. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 4.Cassini A, Diaz-Högberg L, et al. Attributable deaths and disability-adjusted life-years caused by infections with antibiotic-resistant bacteria in the EU and the European Economic Area in 2015: a population-level modelling analysis. Lancet Infect Dis. 2019;19:56–66. doi: 10.1016/S1473-3099(18)30605-4. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 5.Cefiderocol-Fachinformation Stand April 2020
- 6.Dagher M, Ruffin F, et al. Case report: successful rescue therapy of extensively drug resistent (XDR) Acinetobacter baumanni osteomyelitis with cefiderocol. Open Forum Infect Dis. 2020;7(5):ofaa150. doi: 10.1093/ofid/ofaa150. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 7.Delgado-Valverde M. Activity of cefiderocol against high-risk clones of multidrug-resistant enterobacterales, acinetobacter baumannii, pseudomonas aeruginosa and Stenotrophomonas maltophilia. J Antimicrob Chemother. 2020;75(7):1840–1849. doi: 10.1093/jac/dkaa117. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 8.Doi Y. Treatment options for carbapenem-resistant Gramnegative bacterial infections. Clin Infect Dis. 2019;69(S7):S565–S575. doi: 10.1093/cid/ciz830. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 9.https://www.rki.de/DE/Content/Infekt/Antibiotikaresistenz/Uebersichtsbeitraege/AMR_Europa.html. Zugegriffen: 1. Feb. 2022
- 10.Hackel MA, et al. In vitro activity of the siderophore cephalosporin, cefiderocol, against carbapenem-nonsusceptible and multidrug-resistant isolates of gram-negative bacilli collected worldwide in 2014 to 2016. Antimicrob Agents Chemother. 2018;62(2):e01968-17. doi: 10.1128/AAC.01968-17. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 11.Ito A, Nishikawa T, et al. Siderophore cephalosporin cefiderocol utilizes ferric iron transporter systems for antibacterial activity against pseudomonas aeruginosa. Antimicrob Agents Chemother. 2016;60(12):7396–7401. doi: 10.1128/AAC.01405-16. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 12.König C, Wichmann D, et al. Cefiderocol in critically ill patients with multi-drug resistant pathogens: real-life data on pharmacokinetics and microbiological surveillance. Antibiotics. 2021;10:649. doi: 10.3390/antibiotics10060649. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 13.Kollef MH, Novacek M, et al. Ceftolozane–tazobactam versus meropenem for treatment of nosocomial pneumonia (ASPECT-NP): a randomised, controlled, double-blind, phase 3, non-inferiority trial. Lancet Infect Dis. 2019;19:1299–1311. doi: 10.1016/S1473-3099(19)30403-7. [DOI] [PubMed] [Google Scholar]
- 14.Lodise T, Bassetti M, et al. Comparison of 28-day mortality rates of recently completed prospective, randomized treatment studies of adult patients with carbapenem-resistant Gram-negative bacterial infections. 2020. [Google Scholar]
- 15.Longshaw C, Santerre Henriksen A, et al. Post-hoc analysis of the clinical and microbiological outcomes for Cefiderocol against Carbapenem-resistant Non-fermentative Gram negative bacteria in the CREDIBLE-CR study. 2020. [Google Scholar]
- 16.Nagata TD, Wunderink, et al. Efficacy and safety of cefiderocol vs. high-dose meropenem in patients with nosocomial pneumonia—results of a phase 3, randomized, multicenter, double-blind, non-inferiority study. 2019. [Google Scholar]
- 17.Pascale R, Pasquini Z, Bartoletti M, et al. Cefiderocol treatment for carbapenem-resistant Acinetobacter baumannii infection in the ICU during the COVID-19 pandemic: a multicentre cohort study. JAC Antimicrob Resist. 2021;3(4):dlab174. doi: 10.1093/jacamr/dlab174. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 18.Pfennigwerth N. Report of the national reference centre for multidrug-resistant Gram-negative bacteria on carbapenemases in Germany in 2019. 2020. p. A2000. [Google Scholar]
- 19.Portsmouth S, van Veenhuyzen D, et al. Cefiderocol versus imipenem-cilastatin for the treatment of complicated urinary tract infections caused by Gram-negative uropathogens: a phase 2, randomised, double-blind, non-inferiority trial. Lancet Infect Dis. 2018;18:1319–1328. doi: 10.1016/S1473-3099(18)30554-1. [DOI] [PubMed] [Google Scholar]
- 20.Rolston KVI, Gerges B, Shekburne S, et al. Activity of cefiderocol and comparators against isolates from cancer patients. Antimicrob Agents Chemother. 2020;64(5):e01955. doi: 10.1128/AAC.01955-19. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 21.Torres A, Rank D, et al. Randomized trial of ceftazidime-avibactam vs meropenem for treatment of hospital-acquired and ventilator-associated bacterial pneumonia (REPROVE): analyses per US FDA–specified end points. Open Forum Infect Dis. 2019;6(4):ofz149. doi: 10.1093/ofid/ofz149. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 22.Welte T. DIVI, 4.–6.12.2019, Hamburg. 2019. Therapieoptionen bei multiresistenten gramnegativen Erregern – Licht am Ende des Tunnels. [Google Scholar]
- 23.World Health Organization Global priority list of antibiotic-resistant bacteria to guide research, discovery and development of new antibiotics. https://www.who.int/medicines/publications/WHO-PPL-Short_Summary_25Feb-ET_2019. Zugegriffen: 1. Feb. 2022
- 24.Wunderink RG, Matsunaga Y, et al. Cefiderocol versus high-dose, extended-infusion meropenem for the treatment of Gram-negative nosocomial pneumonia (APEKS-NP): a randomised, double-blind, phase 3, non-inferiority trial. Lancet Infect Dis. 2021;21(2):213–225. doi: 10.1016/S1473-3099(20)30731-3. [DOI] [PubMed] [Google Scholar]
- 25.Zhanel GG, Golden AR, et al. Cefiderocol: a siderophore cephalosporin with activity against carbapenem-resistant and multidrug-resistant gram-negative Bacilli. Drugs. 2019;79(3):271–289. doi: 10.1007/s40265-019-1055-2. [DOI] [PubMed] [Google Scholar]
- 26.Zingg S, Nicoletti GJ, et al. Cefiderocol for extensively drug-resistant gram-negative bacterial infections: real-world experience from a case series and review of the literature. Open Forum Infect Dis. 2020;7(6):ofaa185. doi: 10.1093/ofid/ofaa185. [DOI] [PMC free article] [PubMed] [Google Scholar]
Weiterführende Literatur
- 27.Katsube T, Kawaguchi N, Matsunaga Y, et al. Pharmacokinetic/pharmacodynamic analyses of cefiderocol in critically ill patients. Open Forum Infect Dis. 2020;7:669–670. doi: 10.1093/ofid/ofaa439.1498. [DOI] [Google Scholar]