Résumé
Objectif : Evaluer l’impact de la phase pré-analytique sur les prélèvements de bactériologie reçus au laboratoire de bactériologie médicale de CHU Ibn Sina à Rabat afin de propose des actions correctives.
Méthodes: Une étude descriptive quantitative des non-conformités de la phase pré-analytique relevées au sein du laboratoire central de bactériologie médicale de l’hôpital Ibn Sina à Rabat sur une période de 6 mois (du 01 janvier au 01 juillet 2020). Elle a concerné les prélèvements provenant des différents services cliniques et unités de soins de l’hôpital Ibn Sina, ainsi que les prélèvements externes. Afin d’agir sur ces différents dysfonctionnements, nous nous sommes basés sur des outils qualité comme le diagramme de Pareto et d’Ishikawa.
Résultats: Nous avons recensé 424 cas de non-conformités (NC) pré-analytiques sur 14468 échantillons reçus au Laboratoire Central de Bactériologie de l’Hôpital Ibn Sina Rabat soit 2,93%. Il s’agit principalement des erreurs de l'identification des échantillons et identité du patient (59.66%), de la qualité et la quantité des échantillons (25.02%) et d’anomalies relatives aux conditions d’acheminement et de conditionnement (15.32%).
Conclusion: la maîtrise de la phase préanalytique nécessite d’une part, une étroite collaboration entre les différents services, prescripteurs, préleveurs et biologistes et d’autre part le respect de chaque étape de cette phase par le personnel hospitalier.
Mots Clés: Non-conformités, phase pré-analytique, bactériologie médicale, échantillon biologique, amélioration qualité.
Abstract
Introduction: The errors in the pre-analytic phase are at the origin of 60 to 85% of the errors in the results proceeded from laboratory.
Aim: To evaluate the impact of the pre-analytical phase on the received bacteriology samples received at the medical bacteriology laboratory of Ibn Sina UH in Rabat Morocco in order to propose corrective actions.
Methods: A descriptive and quantitative study of the non-conformities of the pre-analytical phase identified in the central laboratory of medical bacteriology of the Ibn Sina hospital in Rabat over a period of 6 months (from January 01 to July 01, 2020). It concerned samples from various clinical services and care units of Ibn Sina Hospital, as well as external samples. In order to act on these various dysfunctions, we used quality tools such as the Pareto chart and from Ishikawa.
Results: We counted 424 cases of pre-analytical NC on 14468 samples received to the Central Laboratory of Bacteriology or 2.93%. These are mainly errors of sample identification and patient identity (59.66%), quality and quantity of samples (25.02%) and problem of conditions of transport and packaging (15.32%).
Conclusion: Its mastery requires firstly, a close collaboration between the various services, prescribers, samplers and biologists and secondly the respect of each stage of this phase by the hospital staff.
Keywords: Non-conformities, pre-analytical phase, medical bacteriology, biological sample, quality improvement.
Introduction:
Dans les laboratoires d’analyses de biologie médicale, les non-conformités de prélèvements sont sans aucun doute les plus fréquentes et les plus simples à tracer. Aujourd’hui, les biologistes sont conscients que les erreurs dans les pratiques de laboratoire de biologie médicale ont directement un impact négatif sur les résultats pour les patients et peuvent altérer le diagnostic et les traitements médicaux (1 ). Le Guide de Bonne exécution des Analyses de biologie médicale (GBEA) définit le processus analytique qui se déroule en trois grandes étapes distinctes et enchainées dans le temps dont l’une influence l’autre : la phase pré-analytique, la phase analytique et post-analytique (2 ).
En microbiologie médicale, la phase pré-analytique qui fait l’objet de notre étude est une étape importante au laboratoire, qui a des répercussions sur la phase analytique et la phase post-analytique. C’est une phase complexe recouvrant l’ensemble des étapes qui se déroulent depuis la prescription médicale jusqu’à la prise en charge des échantillons pour la réalisation proprement dite de l’analyse. Ces étapes doivent être de grande qualité, sinon, le résultat de l’examen peut n'avoir aucune utilité clinique (3 ). Plusieurs chercheurs ont conclu que les non-conformités (NC) auront plusieurs conséquences possibles pour le patient telle une erreur de diagnostic, de prise en charge et de traitement, ainsi qu’une abstention thérapeutique (4 ). Selon la définition Iso 9000, une NC correspond à la non satisfaction d’une exigence (5 ). Elle concerne toutes les étapes de l’examen biologique et n’autorisant pas la prise en charge directe de l’échantillon par les laboratoires (6 ).
Depuis 2017, le centre hospitalier universitaire Ibn Sina (CHUIS) s’est engagé dans une démarche de certification ISO 9001 V2015 de ses laboratoires de biologie médicale dont le but est de conformer les pratiques aux exigences réglementaires relatives au guide de bonne exécution des analyses (GBEA) (2, 7, 8 ) puisque la phase pré-analytique en microbiologie médicale constitue l’un des principaux garants de la fiabilité des résultats car elle conditionne la majeure partie du pouvoir informatif contenu dans le résultat biologique final (9 ). La présente étude, du 01 janvier au 01 juillet 2020, est une évaluation normative et réglementaire des non-conformités du laboratoire de bactériologie médicale de CHUIS afin d’évaluer l’impact de la phase pré-analytique sur les prélèvements de bactériologie reçus au Laboratoire Central de Bactériologie Médicale du CHU Ibn Sina Rabat, de relever les défaillances de cette phase et de proposer des solutions afin d’améliorer la qualité de nos prestations.
Méthodes
Il s’agit d’une étude descriptive quantitative des non-conformités de la phase pré-analytique, relevées au sein du laboratoire de bactériologie médicale de l’hôpital Ibn Sina à Rabat. Elle a été réalisée sur une période de 6 mois et a concerné les prélèvements provenant des différents services cliniques et unités de soins de l’hôpital Ibn Sina, ainsi que les prélèvements externes. Les critères d’inclusion établis comprennent les différents types de NC. Une fiche de NC a été établie, comportant les motifs de la NC et les actions entreprises pour traiter immédiatement le dysfonctionnement. Sur cette fiche, nous avons reporté les NC bloquantes (empêchant la réalisation de l'examen) et non bloquantes (levées secondairement par échanges d’informations) liées à la prescription et l’acte de prélèvement, à l’échantillon prélevé et l’étiquetage ou non de l’échantillon et aux conditions d’acheminement et de conservation.
Principaloutil qualité appliqué dans l’étude
Nous avons utilisé un diagramme de Pareto (10 ) et diagramme causes-effets également appelé diagramme d’Ishikawa. Il s’agit des outils graphiques, d’une démarche qui permet d’identifier les causes possibles d’un problème ou d’une NC pour tenter de le diminuer ou de l’anéantir. Puis en cherchant leur poids relatif, on peut déterminer sur quelle cause agir en priorité en mettant en place des actions correctives appropriées. Cet outil est en effet, utilisé pour comprendre un phénomène, analyser un défaut et identifier l’ensemble des causes du problème afin de trouver des solutions (11, 12 ). Le diagramme de Pareto permet de visualiser rapidement les priorités et les mesures correctives à prendre (13, 14 ).
Pour une analyse plus profonde des non-conformités enregistrées et l’évaluation de leur criticité, nous avons également exploité la Méthode AMDEC « Analyse des Modes, des Effets et de la Criticité des défaillances» comme approche complémentaire d’analyse des risques liés à la phase pré-analytique. L’outil nous a permis de présenter une cartographie des scenarios et situations dangereuses, leurs causes correspondantes, les événements redoutés ainsi que les conséquences qui peuvent en découler. Les événements sont côtés en termes de gravité (G) et de vraisemblance (V) sur la base d’échelles génériques. À partir de ces événements, une matrice de criticité est établie pour aboutir à une échelle de décision. Un scénario de criticité de niveau 3 peut amener à refuser toute l’activité.
On peut alors évaluer la criticité, parfois appelée IPR (Indice de Priorité du Risque), par le produit : IC = V × G × D dont le D est l’indice ou la probabilité de détection de la NC (Indice 1: facilement détectable par l'opérateur Indice 2: Difficilement Détectable par l'opérateur, Indice 2: Indétectable). Plus l’IC est grand, plus le mode de défaillance est critique
Résultats
Représentation globale des causes des NC de la phase pré analytique
Durant la période de l’étude, nous avons recensé 424 cas de NC pré-analytiques sur 14468prélèvements reçus au laboratoire central de bactériologie médicale de l’hôpital Ibn Sina Rabat soit un taux de 2.93%. Les NC en phase pré-analytique recensées sont en rapport avec la prescription, les prélèvements, l’identification ou les conditions d’acheminement (Tableau 1 ).
Tableau 1. Les différents types de non-conformités recensées au Laboratoire de bactériologie médicale de CHU Ibn Sina du 01 janvier au 01 juillet 2020.
|
Niveau de NC |
Type de NC |
Nombre |
Fréquence% |
|---|---|---|---|
|
Bon de demande d’examen |
Discordance identification tube/bon de prescription |
110 |
25.94 |
|
Code à barre incomplet, illisible ou absent |
66 |
15.56 |
|
|
Absence de bon de prescription |
24 |
5.66 |
|
|
Ne contient pas les prestations demandées |
15 |
3.53 |
|
|
Prélévement 138 |
Absence d’identification de tube |
53 |
12.5 |
|
Prétraitement incorrect |
41 |
9.66 |
|
|
Tube manquant |
18 |
4.24 |
|
|
Volume insuffisant pour l’analyse |
14 |
3.30 |
|
|
Tube de prélèvement reçu vide |
12 |
2.83 |
|
|
Conditions d'acheminement et de conversation 65 |
Prélèvement accidenté ou renversé |
32 |
7.54 |
|
Délai d’acheminement incorrect |
19 |
4.48 |
|
|
Conditions d’acheminement incorrectes |
14 |
3.30 |
|
|
Erreur d’acheminement |
6 |
1.41 |
Proportions des principales NC selon leur niveau
Les erreurs enregistrées sont dues à la fois l'identification des échantillons et l’identité du patient représentaient 59.66%. Les prélèvements non-conformes liés à la qualité et la quantité des échantillons avaient un pourcentage de 25.02%.Les causes profondes des non-conformités constatées sont présentées dans le tableau(Tableau 1 ).
Après classement des fréquences des causes possibles de non-conformités et calcul de leurs pourcentages et leur accumulation, nous avons tracé le diagramme de Pareto en prenant en considération les établissements de provenance (Figure 1 ), les types d’analyse demandée et les types de non-conformités enregistrées (Figure 2 ).
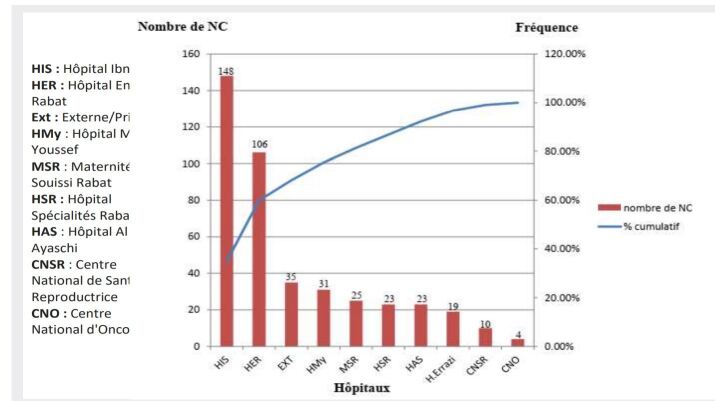
Figure 1.Répartition des non-conformités recensées au laboratoire de bactériologie médicale de CHU Ibn Sina selon l’établissement de provenance.
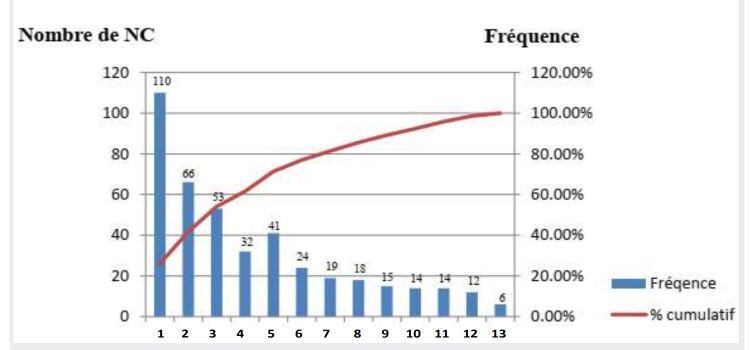
Figure 2.Histogramme de Pareto des différents types de NC relevées au laboratoire de bactériologie médicalee.
Les NC enregistrées au niveau des prélèvements des patients des différents établissements
Les résultats de la répartition des non-conformités recensées au laboratoire de bactériologie médicale de CHU Ibn Sina selon l’établissement de provenance sont représentés sur la figure (Figure 1 ). Après application de la loi de Pareto, il apparaît que 60% de ces non-conformités identifiées sont liées à des échantillons en provenance du HIS (Hôpital Ibn Sina) et HER (Hôpital Enfants Rabat) (Figure 1 ). Ainsi, la plupart des non-conformités constatées en provenance de l’HIS sont dues à une discordance entre le bon de demande d’examen et l'échantillon (67 NC pour 148 échantillons non-conformes reçus de l’HIS).
LesNCrecensées au niveau du laboratoire selon les différents types
Selon l’histogramme de Pareto, Les résultats ont également montré que 42 à 86% des cas d'erreurs recensées résultent de la discordance d’identification entre l'échantillon et le bon de prélèvement, d’un code à barre illisible et de l'absence totale de l’identification des échantillons biologiques (Figure 2 ). Afin de guider nos actions, nous avons cherché à mieux comprendre la relation entre le taux de non-conformités et le type de test demandé. Les résultats ont démontré que 50 à 80% de ces non-conformités ont touché principalement le service de sérologie, la tuberculose et l’ECBU (Examen Cyto-Bactériologique des Urines).
Résultats de l’application des outils qualité à la gestion des NC relevées :
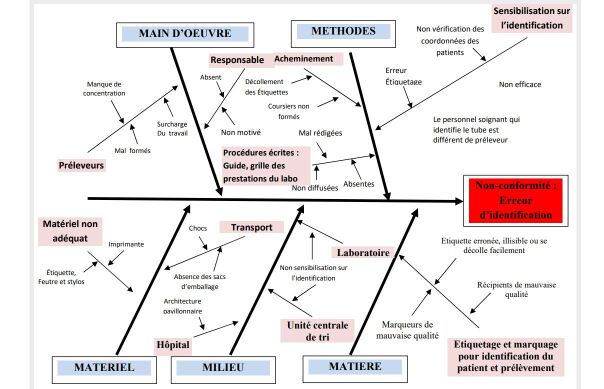
Afin d’agir sur les principales causes de ces NC et planifier une démarche qualité adéquate, nous avons adopté un outil de qualité adapté. Un diagramme d’Ishikawa est donc élaboré dans ce sens en considérant comme problème l’erreur d’identification (Figure 3 ).
Figure 3. Diagramme Ishikawa es différents types de NC relevées au laboratoire de bactériologie.
Les résultats du tableau (Tableau 2 ) confirment et mettent en évidence trois défaillances critiques avec l'indice de criticité le plus élevé. Ceci est dû à une discordance d’identification entre le tube de prélèvement et le bon de prescription [IC (V.G.D)= 48 (4.4.3)], le code à barre absent ou illisible ainsi que la mauvaise identification du tube de prélèvement biologique [IC = 36 (3.4.3)].
Tableau 2. Indice de criticité des non-conformités .
|
Type de NC |
Causes |
Effets potentiels |
V.G.D |
IC |
|---|---|---|---|---|
|
Identification |
Discordance bon de demande d’examen /Echantillon |
Compte rendu erroné |
4.4.3 |
48 |
|
Code à barre du bon d’examen illisible ou absent |
Compte rendu erroné |
3.4.3 |
36 |
|
|
Absence d’identification de l’échantillon |
Compte rendu erroné |
3.4.3 |
36 |
|
|
Prescription |
Absence de bon de prescription |
Analyse non réalisée |
3 .2.2 |
12 |
|
La qualité et la quantité d'échantillon |
Volume insuffisant pour l’analyse Prélèvement accidenté ou renversé Conditions d’acheminement incorrectes |
Résultats biaisés ou pas fiable |
4.3.2 |
24 |
A la lumière de ces données, un service d’assurance qualité a été crée au sein du laboratoire pour dynamiser le système et piloter le processus de certification. Ces actions entreprises ont abouti à une diminution du nombre des demandes d’analyse biologique non-conformes recensées par le personnel du laboratoire et principalement les non-conformités associées à l’identification des échantillons et l’identité du patient. Durant les derniers 6 mois de l’année 2021, nous avons recensé 131 cas de NC pré-analytiques sur 67 277 prélèvements reçus au laboratoire central de bactériologie médicale soit un taux de 1.95% NC. 39.9% des erreurs enregistrées concernaient à la fois l'identification des échantillons et l’identité du patient sur le bon de prélèvement. 35.05% était sur la qualité et la quantité des échantillons. 25.05% était sur les conditions d’acheminement et conditionnement. Ce constat a été également confirmé par le personnel des services cliniques et de l’unité de prélèvement de l’hôpital sous forme d’une remarque liée à la diminution des demandes pour refaire des prélèvements pour motif lié a l’identité du patient au bon d’examen ou/et l’identification de l’échantillon.
Discussion :
La plupart des prélèvements reçus au laboratoire de bactériologie médicale sont conformes (≈ 97%). Ce résultat prouve que le niveau des connaissances et de maitrise des variables pré-analytiques ne constituent pas un problème majeur dans le bon déroulement des analyses biologiques puisque le taux de non conformité ne représente que 2.9%.
L’analyse profonde des causes et hiérarchisation des non-conformités étudiées, selon la loi de Pareto, montre que la majorité des erreurs sont essentiellement dues à une discordance entre l'identification du bon d’examen et celle de l'échantillon. Ce résultat peut être expliqué par la charge de travail pour les personnels des hôpitaux ainsi que l’insuffisance des moyens de travail mis à leur disposition. Le pourcentage important des non-conformités liées à l’identité du patient est dû également au fait que l’identification se déroule à l’extérieur et échappe ainsi au contrôle du personnel du laboratoire (15 ). Il est certain que pour les laboratoires hospitaliers polyvalents qui gèrent toute l’étape pré-analytique externe et interne, ce pourcentage sera moins élevé.
L’erreur d’identification du prélèvement constitue un critère de NC qui doit générer le non exécution des actes (16, 17 ). Elle doit faire l’objet d’un signalement immédiat sur la feuille de NC. Selon le GBEA chapitre II 1-3 portant sur l’identification des échantillons biologiques primaires et secondaires ; l’identification doit comporter les noms, prénoms ou numéros d’identification, la date de prélèvement et la personne préleveur au moment du prélèvement, par la personne l’ayant réalisée (2 ).
De nombreuses études menées sur la détection d’erreurs au laboratoire de biologie médicale, allant de la phase pré-analytique jusqu’à la phase post-analytique, ont révélés des taux d’erreur de 31,6% à 75% (18 ). Une étude réalisée en 2014 au laboratoire de bactériologie médicale de l’hôpital Ibn Sina de Rabat a dénombré 310 prélèvements non conformes sur un total de 12398 prélèvements reçus au laboratoire durant la période de l’étude avec une ration de 2.5%. Il s’agit essentiellement de prélèvements non-conformes à cause de l’identification de l’échantillon biologique et l’identité du patient (61%), de conditions et délai d’acheminement de prélèvements (29%), 10% des NC était lié à la qualité et la quantité de l ‘échantillon biologique (19 ). D’après cette étude, les non-conformités dues aux erreurs de moyen et délai d’acheminement sont plus fréquentes que dans notre enquête. On note un taux de 29% contre un taux de 7.78% dans notre enquête (19 ). Il est nécessaire de signaler que 90% des NC dues au moyen et délai d’acheminement ont été dénombrées dans le laps de temps de deux semaines. Cette période coïncide avec la panne de système de transport pneumatique installé par le laboratoire de bactériologie en 2015 pour faciliter l’acheminement des échantillons biologiques de différents services cliniques et unités cliniques vers le laboratoire. En fait, l’expérience montre que la distance géographique entre les hôpitaux et le laboratoire influence de manière significative le taux et le type de non-conformités (20 ).
En effet, Le taux de non-conformités liée aux erreurs d’identification peut servir comme indicateur qualité et permet l'établissement des tableaux comparatifs (mensuels, annuels) pour suivre la qualité des soins offerts aux patients (21 ). Le suivi de ces indicateurs peut conduire à la correction et l’élimination de ces dysfonctionnements. Les moyens informatiques et l’analyse statistique sont principalement utilisés pour exploiter les données déjà établies (22, 23 ). Les résultats obtenus avec la méthode AMDEC complètent ceux de la carte de Pareto et diagramme d’Ishikawa et il s’avère que ces trois causes des non-conformités sont liées à l’identité du patient. L’analyse des causes et des risques montre que les points les plus critiques et les causes les plus fréquentes des erreurs détectées au sein de notre structure sont définis par un facteur humain(24, 25 ). Il s’agit essentiellement d’un manque de sensibilisation et d’information, mais aussi à cause d’une surcharge de travail importante. L’absence d’un programme de qualification et de formation continue pour le personnel en est une autre cause.
Dans ce cadre, les exigences des textes réglementaires et normatifs exigent la définition des responsabilités, l’habilitation et la formation des personnes impliquées dans la phase pré-analytique PPA, qu’elles soient internes ou externes au laboratoire (26, 27 ). Au Maroc, l’arrêté de la ministre de la santé n°2598-10 du 27 ramadan 1431 (7 septembre 2010), instaure le guide de bonne exécution des analyses de biologie médicale (2 ). Le management de la phase pré-analytique reste sous l’entière responsabilité du biologiste qui doit s’assurer de la bonne diffusion du manuel et guide de prélèvement aux personnels concernés (26, 28 ). Le référentiel en microbiologie médicale (REMIC) et le référentiel en virologie médicale (Revir), deux publications de la Société française de microbiologie, sont d’un grand apport pour le microbiologiste afin d’élaborer leur guide de prélèvements. (29 ).
En pratique, il ne suffit pas de détecter une non-conformité, mais il faut la gérer correctement, et entreprendre des actions correctives et d’amélioration avec vérification de leur efficacité (30 ). Pour assurer le management de la phase pré-analytique, il importe de définir avant tout une politique de détection et de maîtrise des erreurs par la mise en place d’un référentiel interne (31 ). Le recensement et l’analyse des NC aident à mettre en place des mesures correctives sur la base de l’utilisation des outils de gestion de qualité à travers des procédures de contrôles écrites correspondant aux points les plus critiques que nous avons pu identifier. Parmi ces points critiques, il est à noter que dans certains services, il y a un seul infirmier qui se charge des soins, de la préparation des malades aux examens et des prélèvements, qui de ce fait ne se faisaient pas de façon optimale. Afin d’apporter des solutions adéquates, il est alors important de connaitre les conditions matérielles et organisationnelles dans lesquelles se trouve l’infirmier ou le préleveur au moment des prélèvements. La maitrise et le contrôle du moyen de transport des prélèvements soit par pneumatique soit par coursier sont très importants. En effet, depuis l’installation d’un système de transport pneumatique des prélèvements au sein du laboratoire, la durée moyenne de l’acheminement des échantillons a beaucoup diminué et le transport s’effectue de manière optimale afin que le prélèvement ne subisse aucune modification.
Notre travail était certes limité dans le temps, mais il a permis en revanche d’initier un projet éternel d’amélioration continue. Quelque mois après la présentation et la discussion des résultats de l’enquête avec le personnel du laboratoire, des réunions régulières, à l’échelle du laboratoire et les différents services cliniques, ont été organisées et ont permis d’engager une réflexion globale et discussion sur les différentes causes de ces dysfonctionnements et l'identification des causes selon le diagramme d'Ishikawa. La répartition des erreurs selon leur nature et leur origine, possible par la traçabilité, a permis d’établir un vrai dialogue avec les unités de soins pour les encourager à mettre les étiquettes des prélèvements au moment de l’acte et au lit du malade. Les personnels préleveurs de HIS et HER ont été formés, informés et rappelés régulièrement sur les bonnes pratiques du laboratoire afin de minimiser les NC dues à l’identification du prélèvement et l’identité du patient. Le matériel nécessaire et de qualité a été également mis à la disposition des services cliniques pour éviter quelques sources d’erreurs (imprimante, marqueurs…). Une plate-forme intranet des NC consultable à distance a été mise disposition des personnels médicaux afin de suivre l’état de la demande d’analyse.
Ce résultat encourageant prouve l’utilité et l’efficacité des actions entreprises et confirme qu’actuellement la gestion des non-conformités est prise au sérieux par le laboratoire de bactériologie médicale du CHU Ibn Sina et fait partie permanente de son engagement dans la politique d’assurance qualité et le nombre de ces dernières va être adopté comme indicateur qualité afin de l’évaluer d’une façon continue. Le personnel veille plus que jamais à l’application, avec l’aide du chef de laboratoire, des normes relatives à la phase pré-analytique (GBEA, Norme ISO 15189). Pour que les résultats des tests en microbiologie médicale offrent un pouvoir informatif fiable, il est important que le laboratoire veille à ce que toutes les étapes pré-analytiques soient respectées. Nous avons pu démontrer à travers l’enquête menée, que toutes les étapes sont aussi importantes les unes que les autres. Qu’il s’agisse de la prescription, du prélèvement, du transport ou de la réception. Les résultats de notre étude ont révélé l’absence des outils et des méthodes qualité pour la gestion des non-conformités, ainsi qu’un manque au niveau de l’application des référentiels qualité au laboratoire. Le personnel du laboratoire se contente du GBEA d’application obligatoire et qui ne renseigne pas effectivement sur la gestion des non-conformités, d’où la nécessité d’utiliser des référentiels ISO tel que la norme ISO 9001 V2015 complétée par ISO 15189V2012.
References
- Forsman R W. Clinical Chemistry. 5. Vol. 42. Oxford University Press (OUP); 1996. Why is the laboratory an afterthought for managed care organizations? pp. 813–816. [PubMed] [Google Scholar]
- Arrêté de la ministre de la santé n°2598-10 relatif au guide de bonne exécution des analyses de biologie médicale. http://www.sgg. gov.ma/Portals/0/profession_reglementee/Dec_2598.10_ Fr.pdf Bulletin Officiel. 2010;5892:2046–2050. [Google Scholar]
- Cheminel V, Prévosto J.-M, Muraillat D, Renard C. Mise en place d’un manuel assurance qualité dans un laboratoire de biologie hospitalière. https://www.jle.com/fr/revues/abc/edocs/ mise_en_place_dun_manuel_dassurance_qualite_dans_un_ laboratoire_de_biologie_hospitaliere_50763/article.phtml. Ann Biol Clin. 2000;58:228–260. [PubMed] [Google Scholar]
- Breijo Stéphanie, Pelisse Christelle, Theveny Aline, Traigneau Florence, Schabad Caroline, Agbovon Olivier, Salmon Patricia, Arronis Ysabel, Goulas Elodie, Cassereau Catherine, Pressiat Claire, Challine Dominique, Bastard Jean-Philippe. Annales de Biologie Clinique. 6. Vol. 78. John Libbey Eurotext; 2020. Improvement of the pre-examination phase of medical biology exams at the Henri Mondor University Hospitals: a pilot study; pp. 686–690. [DOI] [PubMed] [Google Scholar]
- Norme ISO 9000. Systèmes de management de la qualité — Principes essentiels et vocabulaire. Afnor, 2015. : https://www.boutique.afnor.org/fr-fr/norme/ nf-en-iso-9000/systemes-de-management-de-la-qualite-principes-essentiels-et-vocabulaire/fa171778/1515 [Google Scholar]
- Elargoubi A, Mastouri M, Najjar M-F. Management de la phase pré-analytique: expérience pratique au laboratoire de microbiologie de l’hôpital Fattouma Bourguiba de Monastir. Annales de Biologie Clinique. 2014 doi: 10.1684/abc.2014.0992. [DOI] [PubMed] [Google Scholar]
- Circulaire n °34/09 relative au système de santé et à l’offre de soins (BO N 5962 du 21-07-2011). https://www.sante.gov.ma/Reglementation/Pages/systemede-santé-et-offre-de-soins.aspx. [Google Scholar]
- Circulaire du CHUIS 2007 aux services médico-techniques, relative à la mise en place une politique de management qualité et aux exigences du GBEA : http:// www.churabat.ma/index.php/2020-07-21-10-25-52/2020-07- 21-10-30-59/2020-07-21-10-32-34/2020-07-21-10-36-22. [Google Scholar]
- Gris Jean-Christophe C, Mercier Eric. Revue Française des Laboratoires. 317. Vol. 1999. Elsevier BV; 1999. Les constantes pré-analytiques en hémostase; pp. 63–70. [Google Scholar]
- Cattan Michel, Idrissi Nathalie, Knockaert Patrick. Editions Eyrolles; 2008. Ma\^\itriser les processus de l'entreprise; pp. 266–267. [Google Scholar]
- Poonam G, Mincy T, Rn, Nidal S, Gracy C. A Quality Improvement Initiative to Reduce Rejected Laboratory Samples and Enhance Specimen Acceptability. The Joint Commission Journal on Quality and Patient Safety. 2021;47(8) doi: 10.1016/j.jcjq.2021.04.005. [DOI] [PubMed] [Google Scholar]
- Bertrand D. Accréditation et qualité des soins hospitaliers. Adsp. 2001;35:17–17. [Google Scholar]
- AM Chauvel. dunod; Paris: 1996. Méthodes et outils pour résoudre un problème: 30 outils pour améliorer la qualité de votre organisation. [Google Scholar]
- M Erbault, J Glikman, MJ Ravineau, N Lajzerowicz, J Orvain. Méthodes et outils des démarches qualité pour les établissements de santé, guide méthodologique 2000. http://www.has-santé.fr [Google Scholar]
- Séguéla Jean-Paul, Sampol José. L'etape pre-analytique en biologie medicale. Revue Francaise des Laboratoires. 1999;317(1999):25. [Google Scholar]
- Etablissement Français du Sang EFS - Manuel de prélèvement du laboratoire d’immuno-hématologie érythrocytaire [Google Scholar]
- G Delaport. Laboratoire Delaporte 2009; Manuel des Prélèvements. . [Google Scholar]
- Bonini Pierangelo, Plebani Mario, Ceriotti Ferruccio, Rubboli Francesca. Clinical Chemistry. 5. Vol. 48. Oxford University Press (OUP); 2002. Errors in Laboratory Medicine; pp. 691–698. [PubMed] [Google Scholar]
- El Hani Y, Alaoui Lamrani, Mahassini H, Radi N, L. Risk analysis and management of nonconformities of the pre-analytical phase in a university testing laboratory of bacteriology. J. Med. Lab. Diagn. 2014;5(1):1–10. [Google Scholar]
- Hinckley C M. Quality and Safety in Health Care. 5. Vol. 12. BMJ; 2003. Make no mistake--errors can be controlled; pp. 359–365. [DOI] [PMC free article] [PubMed] [Google Scholar]
- Observatoire prospectif des Métiers et des qualifications dans les Professions Libérales OMPL (2012). . https://www.ompl.fr/images/RapportsActivite/ RAPPORTACTIVITE_OMPL_2011.PDF. Étude réalisée par le cabinet Pollen Conseil pour l’OMPL. 2012
- Dash Sabyasachi, Shakyawar Sushil Kumar, Sharma Mohit, Kaushik Sandeep. Journal of Big Data. 1. Vol. 6. Springer Science and Business Media LLC; 2019. Big data in healthcare: management, analysis and future prospects; pp. 54–54. [Google Scholar]
- Hammerling Julie A. Laboratory Medicine. 2. Vol. 43. Oxford University Press (OUP); 2012. A Review of Medical Errors in Laboratory Diagnostics and Where We Are Today: Table 1; pp. 41–44. [Google Scholar]
- Larrose C, Carrer Le, D. Traitement des non conformités en pratique quotidienne. Ann. Biol. Clin. 2007;65:99–105. [PubMed] [Google Scholar]
- Ridoux M, AMDEC Moyen. Techniques de l’ingénieur. https:// www.techniques-ingenieur.fr/base-documentaire/genieindustriel-th6/methodes-de-production-42521210/amdecmoyen-ag4220/ L’entreprise industrielle. 1999;1:4–220. [Google Scholar]
- Norme internationale ISO 15189-2012, relative aux exigences particulières concernant la qualité et la compétence dans les laboratoires d’analyses de biologie médicale. https://www.iso.org/fr/standard/42641.htm
- L Degos, F Romanex. Manuel de certification des établissements de santé. Direction de l’Amélioration de la Qualité et de la Sécurité des Soins 2009 . http://optimiz-sih-circ-med.fr/Documents/HAS_manuel_ certif_v2010_12-11-2008.pdf :100. [Google Scholar]
- Serge B. Internes en biologie : « rendre le biologiste incontournable dans le parcours de soins du patient. Option Bio. 2013;487:1–3. [Google Scholar]
- microbiologie Société française de. Phase préanalytique des analyses de microbiologie médicale. Remic. 3e édition. . Paris : CMIT Alinéa Plus. 2007:7–14. [Google Scholar]
- Lima-Oliveira Gabriel, Guidi Gian Cesare, Guimaraes Andre Valpassos Pacifici, Correa Jose Abol, Lippi Giuseppe. Journal of Medical Biochemistry. 1. Vol. 36. Centre for Evaluation in Education and Science (CEON/CEES); 2017. Preanalytical Nonconformity Management Regarding Primary Tube Mixing in Brazil; pp. 39–43. [DOI] [PMC free article] [PubMed] [Google Scholar]
- Leblanc R M. Option/Bio. 486. Vol. 24. Elsevier BV; 2013. Accréditation : les points critiques en pré-analytique; pp. 23–24. [Google Scholar]