Abstract
대퇴슬와동맥의 말초동맥폐쇄질환은 일반적으로 죽상경화증에 의해 발생하며, 질병의 정도에 따라 간헐적 파행에서부터 심각한 사지 허혈 또는 조직 손상에 이르는 다양한 증상으로 나타날 수 있다. 따라서, 증상을 개선하고 사지를 형태적, 기능적으로 보존하기 위해서는 적절한 치료가 필요하다. 대퇴슬와동맥 질환에서 시행되는 대표적인 인터벤션 치료로는 혈관 성형술, 스텐트 삽입술, 죽종절제술 등이 있다. 수년에 걸쳐, 혈관 내 재개통술은 최소 침습적이라는 이점과 더불어 시술 방법 및 사용 기기의 지속적인 발전을 토대로 말초동맥폐쇄질환의 치료에 널리 시행되고 있다. 이번 종설에서는 대퇴슬와동맥 질환의 다양한 혈관 내 치료 방법에 대해 소개하고, 문헌 고찰을 통해 현재까지 나온 임상 연구의 결과들을 논의하며, 대퇴슬와동맥질환의 치료에 적용되는 시술 방법에 대한 영상을 제시하여 독자의 이해를 돕고자 한다.
Keywords: Peripheral Arterial Disease, Angioplasty, Stents, Atherectomy, Paclitaxel
Abstract
Peripheral arterial occlusive disease (PAOD) of the femoropopliteal artery is commonly caused by atherosclerosis. It can present with varying clinical symptoms depending on the degree of disease, ranging from intermittent claudication to critical limb ischemia and tissue loss. Therefore, appropriate and timely treatment is required to improve symptoms and salvage the affected limbs. Interventional approaches for femoropopliteal arterial disease commonly include percutaneous transluminal angioplasty, atherectomy, and stent placement. Over the years, endovascular recanalization has been widely performed for treating PAOD due to continuous developments in its techniques and availability of dedicated devices with the inherent advantage of being minimal invasive. In this review, we introduce various types of endovascular treatment methods, discuss the results of clinical research from existing literature, and illustrate the treatment procedures using representative images.
서론
말초동맥질환(peripheral arterial disease)은 관상동맥질환 및 뇌혈관질환과 더불어 3대 죽상경화증후군(atherosclerotic syndrome) 중 하나이다. 말초동맥질환은 전신 동맥경화증의 가장 흔한 발현 형태인데, 이는 하지의 동맥 내경이 죽상판(atheromatous plaque)에 의해 점진적으로 막히는 질환이다. 말초동맥질환을 가진 환자는 모든 원인에 의한 사망 위험이 3배가 증가하는데, 특히 관상동맥질환으로 인한 사망률은 6배 이상 증가한다고 알려져 있다. 하지만, 말초동맥질환은 동맥경화질환 중에서 가장 과소진단(underdiagnosis)을 받고 있으며, 치료 또한 적절하게 이루어지지 않고 있는 실정이다(1,2).
말초동맥질환 중 대퇴슬와동맥(femoropopliteal artery)의 만성협착 및 폐쇄는 운동 시 근육에 불편감이 있다가 휴식 시에 호전되는 간헐파행(intermittent claudication)의 증상을 보인다. 간헐파행을 치료하지 않고 방치하면 허혈성 궤양 또는 휴지기에도 통증이 발생하는 임계하지허혈(critical limb ischemia)로 진행할 수 있다. 간헐파행과 감별해야 할 질환으로는 만성구획증후군, 정맥파행, 신경근압박, 베이커 낭종, 고관절염, 척추협착, 또는 발이나 발목의 관절염 등이 있고, 임계하지허혈과 감별해야 할 질환들로는 당뇨신경병증, 복합부위통증증후군, 신경근압박, 야경증 및 버거병 등이 있다(3,4).
오랫동안 대퇴슬와동맥의 죽상경화증에 의한 협착 및 폐쇄성 병변은 수술적 우회술(surgical bypass)로 치료해 왔으나, 최근에 혈관 내 치료(endovascular treatment)가 그 치료 결과를 인정받아 수술적 우회술이 가능한 경우에도 우선적으로 혈관 내 치료가 권장되고 있다(5,6).
대퇴슬와동맥 혈관 내 치료에 대한 가이드라인은 1994년 American Heart Association의 태스크포스 팀이 처음 제안한 이후로 2016 가이드라인을 갱신하였고, 2017 European Society of Cardiology와 European Society of Vascular Surgery가 협력하여 가이드라인을 발표하였다(3,6). 또한, 2007년 하지동맥 질환의 질병 양상과 형태에 따른 치료 지침인 Trans-Atlantic Inter-Society Consensus (이하 TASC-II는 2015년에 슬와하 분절(infrapopliteal segment)을 포함하여 완전한 해부학적 하지의 TASC 계층화를 제공하였고, 새로운 혈관 내 기술과 임상적 양상을 갱신한 문헌을 포함하여 발표하였다. 이번 개정은 복잡한 해부학을 TASC 분류 카테고리로 더 간단히 재분류하여 혈관 내 치료의 적응증을 확대하였다는 점에서 의미가 크다(5).
이와 더불어 최근 혈관 내 치료에 paclitaxel과 같은 약물을 이용한 풍선이나 스텐트가 많이 활용되고 있어, 이와 관련한 연구들이 활발하게 진행되고 있다.
이 종설에서는 대퇴슬와동맥 질환에서 혈관 내 치료의 방법과 최신 지견을 알아보고자 한다.
대퇴슬와동맥 혈관 내 치료
풍선혈관성형술[Balloon Angioplasty (Plain Old Balloon, Drug Coated Balloon)]
적응증
가장 중요한 적응증은 환자의 임상증상이다. 일반적으로 증상이 없다면 예방적 재개통술을 시행하지 않는 것이 원칙이며, 증상이 있는 다리동맥폐쇄성질환을 가진 환자만이 재개통술의 대상이 된다(7). 고식적 풍선혈관성형술은 치료 결과에 있어 만족할 만한 개통률을 가져오지 못하였다. 하지만, 최근에는 풍선카테터에 내막증식(intimal hyperplasia)을 줄일 수 있는 paclitaxel과 같은 약물을 코팅하여 개통률이 증가하게 되었는데, 이는 스텐트와 같은 체내 특정 삽입물을 남기지 않는 치료 방법으로서 현재 많이 시행되고 있다.
술기
일반적으로 초음파 유도하에 총대퇴동맥을 천자하여 병변이 있는 대퇴슬와동맥에 접근한다. 접근 방식은 반대편(contralateral)을 통해 접근하는 역행성 접근(retrograde approach)과 동측(ipsilateral)을 통해서 선행성(antegrade)으로 접근하는 방식이 있다. 상황에 따라 시술자가 적절하게 적용하는 것이 중요하지만, 일반적으로 폐쇄나 협착이 한쪽 대퇴동맥 또는 그 이하에 국한된 경우에는 앞방향천자를 통한 동측 접근 방법을 많이 사용한다.
시술 시에는 일반적으로 5~8 Fr sheath 중 시술자가 상황에 맞게 선택을 하며, sheath를 삽입 전후 heparin을 주입한다. 카테터나 sheath를 협착 또는 폐쇄된 혈관의 근위부에 위치시키고 유도철사로 병변의 통과를 시도한다. 병변의 협착 정도나 길이에 따라 다양한 종류의 유도철사를 이용하여 병변을 통과시킨다. 이때 내막하 통과(subintimal passage)가 되면, 재진입 구멍(reentry tear)을 만들거나 재진입 기구(reentry device)를 사용하여 true lumen으로 재진입을 시도할 수 있다.
유도철사가 병변을 통과하면 유도철사를 유지한 채로 카테터를 제거하고 주위 정상 혈관의 지름과 같거나 약간 큰 풍선카테터를 병변의 위치에 삽입한다. 대퇴슬와동맥에는 주로 6 mm 크기의 풍선카테터를 사용하나, 혈관 크기에 따라 5~8 mm까지 선택할 수 있다. 풍선의 잘록한 부위(waist)가 소실될 때까지 풍선카테터를 팽창시킨 후 1분 안팎으로 유지한다.
약물코팅 풍선카테터를 이용하여 시술할 경우에는, 먼저 1 mm 작거나 같은 크기의 일반풍선카테터로 전확장(predilatation)을 시행 후(vessel preparation), 혈관 크기와 같은 약물코팅 풍선카테터로 혈관성형술을 시행하여야 하며, 약물이 알맞게 방출되도록 풍선 확장 후 3분간 유지하도록 권고하고 있다.
풍선혈관성형술 후 유도철사를 유지하고 혈관조영술 등으로 병변의 호전 정도를 확인한다. 이때, 혈관의 파열, 박리, 원위부 색전 등의 합병증 유무를 반드시 살펴보아야 한다(Fig. 1). 환자의 증상으로도 어느 정도 파악할 수 있는데, 풍선을 팽창시키면서 느꼈던 통증이 수축 이후에도 지속되면 혈관 파열이나 원위부 색전 같은 합병증을 의심하여야 한다.
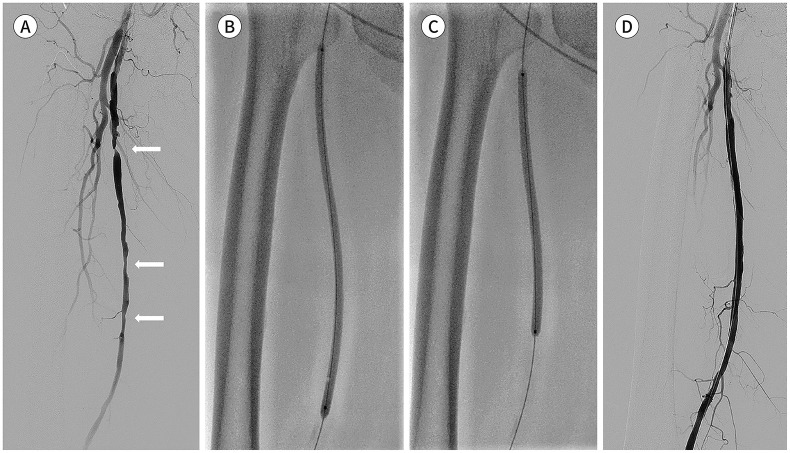
Fig. 1. A 72-year-old male patient with intermittent claudication.
A. Angiographic image shows multiple stenoses in the right SFA (arrows).
B, C. A 5 × 200-mm pre-balloon and 6 × 150-mm drug-coated balloon were inflated in the stenotic segment of the right SFA.
D. Final angiography shows improvement of the stenoses.
SFA = superficial femoral artery
결과
과거 일반 풍선카테터를 이용한 장기 개통률이 45% 정도로 저조한 것에 비하면 약물코팅 풍선카테터는 훨씬 좋은 결과를 보인다. 2019년에 발표된 메타 분석에 따르면, 2년 추적 결과에서 약물코팅 풍선카테터를 이용한 혈관성형술이 고식적 풍선카테터를 이용한 경우보다 표적병변혈관 재개통률(target lesion revascularization rate; 이하 TLR) [odds ratio (이하 OR) 0.29, 95% confidence interval (이하 CI) 0.20~0.40], 일차 개통률(primary patency) (OR 0.38, 95% CI 0.27~0.54), 후기 내강 손실(late lumen loss) (mean diameter −0.80 mm, −1.44~−0.16) 및 Rutherford category (OR 0.82, 95% CI 0.57~1.19) 측면에서 모두 통계적으로 유의하게 우수한 결과를 보였다(8).
장기 추적 관찰 결과에서도 약물코팅 풍선카테터를 이용한 혈관성형술이 우수한 성적을 보였는데, Schneider 등(9)의 보고에 따르면, 3년 개통률과 clinically driven TLR이 각각 69.5% vs. 45.1%, 15.2% vs. 31.1%로 약물코팅 풍선카테터가 더 우수하였고, Laird 등(10)과 Xu 등(11)의 연구에서 5년 freedom from clinically driven TLR이 각각 74.5%, 77.5%로 고식적 풍선카테터와 비교하여(각각 65.3%, 59.1%) 더 우수한 결과를 나타냈다.
길이가 긴(≥ 10 cm) 대퇴슬와동맥 병변에 대해서도 1년 개통률이 20~43%로 저조했던 기존 일반 풍선카테터를 이용한 혈관성형술과는 달리(12,13), 약물코팅 풍선카테터를 이용한 혈관성형술은 1년, 2년 개통률이 각각 83.2%, 70.4%로 우수한 성적을 나타냈다(14,15).
스텐트 설치술[Stent Placement (Bare Metal Stent, Drug Eluting Stent)]
고식적 풍선혈관성형술의 장기 개통률이 만족스럽지 못한 결과를 보여 이를 극복하기 위한 노력의 대표적인 예가 스텐트 설치술이다. 최근 스텐트 설치술에서도 풍선카테터 혈관성형술과 유사하게 약물방출 스텐트가 출시되어 이에 대한 연구가 활발히 진행되고 있다.
적응증
대퇴슬와동맥에 스텐트 설치술은 TASC-II 분류를 따르지만, 풍선혈관성형술과 스텐트 설치술 중 어떤 시술을 우선적으로 시행해야 하는지에 대해서는 아직까지 논란이 있다.
과거의 스텐트 설치술은 풍선혈관성형술과 비교하여 개통률에 큰 차이가 없어(16,17), 풍선혈 관성형술에 반응이 없거나 혈류 제한을 일으키는 박리가 발생하였을 때만 제한적으로 사용되어 왔다(18).
그러나, 스텐트의 기술력이 지속적으로 발전하여 대퇴동맥의 스텐트 설치술의 결과가 과거보다 우수할 뿐만 아니라, 풍선혈관성형술과 비교한 무작위 대조실험에서도 우수함이 입증되었고(19,20), 최근에 출시된 약물방출 스텐트는 풍선혈관성형술보다 더 좋은 성적을 보이고 있어 많은 경우에 일차적으로 스텐트 설치술이 고려되고 있다.
술기
기본적으로 술기 과정은 풍선혈관성형술과 유사하다. 일반적으로 지름 5~8 mm의 자가팽창형 스텐트(self-expandable stent)를 사용하며, 협착이 심하거나 폐색된 경우에는 스텐트 직경보다 작은 풍선카테터로 전확장을 시행하고 스텐트를 설치하기도 한다. 스텐트 설치술 이후에는 스텐트 직경보다 1~2 mm 작은 풍선카테터로 후확장을 시행한다(Fig. 2).
Fig. 2. A 79-year-old male patient who presented with intermittent claudication.
A. Angiographic image shows segmental, moderate stenosis with eccentric severe stenosis (arrow) in the left proximal SFA.
B. A 6 × 120-mm balloon was inflated in the stenotic segment of the left SFA.
C. Follow-up angiogram shows segmental dissection (arrows) in the prior ballooning segment.
D. A 6 × 80-mm drug eluting stent was deployed in the dissection segment.
E. Final angiography shows improvement of the dissected segment.
SFA = superficial femoral artery
결과
초기 모델의 스텐트는 장기 개통률이 풍선혈관성형술과 비교하여 큰 차이가 없었다(21,22,23). 이후, 니켈과 티타늄의 합금인 니티놀(nitinol)을 이용한 스텐트의 재질 및 종류가 매우 빠르게 발전하였고, 이는 기존의 스테인리스 스틸 스텐트에 비해 우수한 성적을 보였다(24). 니티놀 스텐트를 이용한 대퇴동맥의 스텐트 설치술에 대한 초기 연구들을 보면, 비교적 긴 병변(평균 12.2 cm)에서 개통률이 6개월에 92%, 1년에 76%, 2년 추적 관찰에서 60%로 보고되었고(25), 풍선혈관성형술과 비교한 여러 무작위 대조 연구에서도 우수함이 입증되었다(19,26,27,28).
약물방출 스텐트가 나온 이후로 스텐트 설치술은 더 활발하게 연구가 진행되었다. 이 중 초기 연구인 sirolimus 방출 스텐트를 이용한 연구(SIROCCO trial)에서는 약물방출 스텐트와 기존 스텐트 사이에 큰 차이를 보이지 않았으나(2년 재협착률: 22.9% vs. 21.1%) (29), 이후에 출시된 paclitaxel 방출 스텐트를 이용한 연구 결과는 좋은 성적을 보였다. Zilver PTX (Cook Medical, Bloomington, IN, USA)는 paclitaxel을 최초로 이용한 말초동맥용 약물방출 스텐트로서, 574명의 표재대퇴동맥 병변에 풍선혈관성형술, 고식적 스텐트 및, paclitaxel 방출 스텐트를 비교한 다기관 무작위 실험에서 paclitaxel 약물방출 스텐트의 1년 일차 개통률이 의미 있게 높았고(30), 5년 개통률도 66.4% vs. 43.4%로 약물방출 스텐트가 고식적 스텐트보다 더 좋은 결과를 보였다. Freedom from TLR도 83.1% vs. 67.6%로 약물방출 스텐트가 우세하였으며, 해당 결과들은 모두 통계적으로 유의하였다(31).
최근에 출시된 Eluvia (Boston Scientific, Marlborough, MA, USA) 역시 paclitaxel을 방출하는 스텐트이지만, 약물을 방출하는 방식에 차이가 있다. Zilver PTX가 중합체(polymer) 없이 paclitaxel을 방출했다면, Eluvia는 스텐트에 중합체가 코팅되어 있어 약물이 오랜 시간에 걸쳐 서서히 방출되는 방식을 구사하고 있다. 이를 이용한 전향적, single arm clinical trial인 MAJESTIC 연구에서는 해당 스텐트의 1년 및 2년 개통률이 각각 96%, 83.5%를 보였고, 3년 freedom from TLR이 85.3%로 우수한 성적을 보였다(32,33). 또한, 14 cm 초과 19 cm 이하의 긴 병변을 가진 50명의 환자에서도 1년 개통률이 91% 및 freedom from TLR이 93.9%로 우수한 성적을 나타냈다(34).
이후 Eluvia와 Zilver PTX 간의 비열등성 무작위 대조 임상실험이 진행되었는데, 1년 개통률에서 92.1% vs. 81.8%로 Eluvia가 유의하게 우수한 성적을 보였다. 2년 개통률에서도 83% vs. 77.1%로 Eluvia가 우수한 결과를 보였지만 통계적 유의성은 보이지 않았다. Clinically driven TLR의 경우, 1년차와 2년차 모두 Eluvia가 더 좋은 성적을 보였고(9% vs. 4.5%, 20.1% vs. 12.7%), 이 결과에서는 오히려 2년차에서 통계적 유의성을 보였다. 하지만, non-clinically driven TLR의 경우에는 Zilver PTX 군에서는 한 명도 없었으나, Eluvia 군에서는 2명이 있는 것으로 보아 좀 더 장기적인 연구 결과를 확인할 필요가 있다(35,36).
약물방출 스텐트는 다른 그룹들과의 비교 연구도 활발하게 진행되고 있다. 30 cm 이하의 대퇴슬와동맥 병변에서 시행된 Zilver PTX와 약물코팅 풍선카테터 간의 무작위 대조 연구(real PTX RCT)에서 1년 개통률에는 큰 차이가 없었지만, 시간이 지날수록 두 군 모두 개통률이 감소하는 결과를 보였고, 시간이 지날수록 두 군 간의 차이가 벌어져 3년 개통률에서는 약물방출 스텐트 군이 더 좋은 성적을 보였다(56.7% vs. 42.4%). 그러나, 이 결과는 통계적 유의성을 보이지는 않았다(37).
수술적 치료인 우회술(bypass)과 비교한 연구(ZILVERPASS study)에서도, 1년 개통률이 Zilver PTX 군 74.5%, 우회술 군 72.5%로 큰 차이를 보이지 않았다. Freedom form TLR도 각각 80.9%, 76.2%로 Zilver PTX 군이 약간 더 좋기는 하였으나 통계적으로 유의하지는 않았다. 하지만, 30일 합병증 발생률에 있어서 Zilver PTX 군이 유의하게 적었고, 시술 시간이나 입원 기간에서도 Zilver PTX 군이 좋은 성적을 보였다(38). 앞으로 장기 추적 결과를 기다려봐야 할 것이다.
이러한 최근 자료를 종합해 볼 때, 대퇴슬와동맥의 치료에서 스텐트 설치술은 풍선혈관성형술과 비교하여 과거보다 우수한 결과를 보이며, 특히 약물방출 스텐트는 더욱 좋은 성적을 나타내고 있다. 그러나 기본적으로 대퇴슬와동맥은 굽힘(flexion), 폄(extension), 비틀림(torsion) 및 외인성 압박(extrinsic compression) 등의 다양한 힘을 받는 혈관이기 때문에 스텐트 골절이 발생할 수 있다는 한계점이 있다. 최근 연구들에 따르면 스텐트 골절의 발생빈도가 0~6%로 많이 낮아졌지만(30,39,40), 스텐트 골절이 발생하면 이로 인해 재협착이나 폐색이 야기될 수 있어 세심한 주의가 필요하다. 또한, 같은 이유로 풍선팽창형 스텐트 역시 외력에 의해 스텐트가 쉽게 변형되어 내막증식(intimal hyperplasia)을 일으킬 수 있으므로 대퇴슬와 동맥 치료에서는 피하는 것이 좋다(41).
죽종절제술(Atherectomy)
일반적으로 대퇴슬와동맥의 혈관 내 치료는 풍선혈관성형술이나 스텐트 설치술이 주를 이루고 있다. 하지만 이러한 치료법들은 안쪽에서 바깥쪽으로 혈관을 팽창시키는 방법이므로 혈관벽에 압력손상(barotrauma)을 주게 되고, 이로 인해 탄력반동(elastic recoil), 박리(dissection), 신생혈관내막증식(neointimal hyperplasia) 등이 발생할 수 있다. 이에 대한 대체 기술로서 만들어진 것이 죽종절제술이다. 최근, “leave nothing behind”라는 개념이 일반화되면서, 죽종절제술 자체보다는 약물방출 풍선카테터의 약물을 더 효과적으로 전달하기 위한 병합치료로서의 죽종절제술이 더 각광받게 되었다(42).
Paclitaxel과 관련된 논쟁
앞서 소개한 약물코팅 풍선카테터나 약물방출 스텐트에 주로 사용되는 약물인 paclitaxel은 항증식제(antiproliferative agent) 역할을 하여 시술 후 재협착을 줄여주고, 이로 인해 반복적인 시술을 줄일 수 있다.
최근 Katsanos 등(43)에 의해 발표된 메타 분석 결과에서, paclitaxel의 사용과 연관된 사망 위험률이 증가한다고 보고되어 약물코팅기구의 장기 안정성에 대한 논란이 일어났다. 이후 이와 관련된 수많은 논쟁이 있었고, 해당 문제를 확인하기 위한 일환으로 중단되었던 약물코팅기구를 검토하는 Swedish Drug Dlution Trial in Peripheral Arterial Disease (이하 SWEDEPAD) 연구가 중간 분석을 진행하였고, 최근에 결과를 발표하였다. 다기관 무작위 오픈라벨 레지스트리 SWEDEPAD 연구는 총 2289명의 말초동맥질환 환자를 포함하였고, 평균 2.49년 추적 관찰에서 574명의 환자가 사망하였다. 이들 중 약물코팅기구군에는 293명(25.5%), 비약물코팅기구군에서는 281명(24.6%)이 사망하였고, 이는 통계적으로 유의한 차이가 없었다(hazard ratio 1.06, 0.92~1.22). 1년 시점에서 모든 원인 사망률도 두 군 간의 유의한 차이가 없었고(10.2% vs. 9.9%), 전체 추적 관찰 기간동안 만성중증하지허혈 환자들 또는 간헐파행 환자들 사이에서 발생한 사망률 모두 유의한 차이를 보이지 않았다(33.4% vs. 33.1%, 10.9% vs. 9.4%). 이 연구에서 모든 원인 사망률에 대해 분석한 결과, 1년에서 4년까지 추적 관찰 하는 동안 두 그룹 간의 사망률에는 통계적으로 유의한 차이가 없다고 결론지었다(44). 최근 paclitaxel 기구 사용과 관련하여 FDA에서 권고안을 발표하였는데, paclitaxel 기구로 치료를 받은 환자는 지속적으로 꾸준히 관찰해야 하고, 치료 권고안을 작성하거나 동의서를 받는 과정에서 paclitaxel 기구로 치료를 받는 환자에서는 장기 사망률이 증가할 수도 있다는 점을 고려하라고 제시하고 있다. 또한 모든 말초동맥질환 치료 옵션에 있어 위험과 이점에 대해 환자와 상의를 해야 하는데, 특히 paclitaxel 기구의 대체 치료 방법에 대해 유익성과 위해성에 대해 설명해야 함을 권고하고 있다. 재협착 위험이 높거나 반복적인 시술을 받을 가능성이 높은 환자의 경우는 임상의가 paclitaxel 기구를 사용했을 경우의 이점이 사망률의 위험보다 높다고 결정할 수 있다고 제시하고 있다. 환자는 말초동맥질환 및 기타 심혈관 위험 인자에 대해 최적의 치료를 받아야 하고 체중 조절, 금연 및 운동을 포함한 건강한 생활 습관에 대한 지침을 제공받도록 해야 한다고 권고하고 있다(45).
기타 치료법
내막하혈관성형술(Subintimal Angioplasty)
대퇴슬와동맥의 폐쇄를 유도철사로 통과할 때, 막힌 혈관의 내막의 안쪽인 true lumen이 아닌 내막의 외측으로 지나갈 수도 있는데(subintimal passage), 이를 이용하여 인위적으로 혈관을 박리하여 false lumen으로 유도철사가 지나가게 한 후 다시 true lumen으로 재진입시켜 false lumen을 풍선카테터로 확장하는 것을 내막하혈관성형술이라고 한다(Fig. 3) (46,47). 이 치료법은 죽종과 같은 혈관 폐쇄물질을 편심성으로 밀어내어 매끄럽고 병변이 없는 새로운 길을 만들어 주는 방법이다. 하지만, 드물지 않게 true lumen으로의 재진입이 어려운 경우가 발생하는데, 이런 경우 여러가지 방법을 이용하여 재진입을 시도해 볼 수 있다. 말단 모양이 다른 유도철사나 카테터로 교체하거나, 무릎 관절 이하로 내려가지 않는 한에서 좀 더 원위부 내막 밑 공간에서 재시도를 해볼 수 있다. 또한, Outback LTD reentry catheter (Cordis, Miami Lakes, FL, USA)와 같은 재진입카테터를 사용하거나, 폐색병변 하부의 재구성된 오금동맥 또는 경골동맥을 역방향으로 천자하여 폐색병변의 내막 밑 공간(이때, 풍선카테터를 이용하여 공간을 넓힐 수도 있다) 또는 true lumen을 통해 진입시킨 후, 대퇴동맥 경로를 통해 snare catheter를 이용하여 유도철사를 잡은 후 밖으로 빼내어 경로를 확보하는 방법도 있다(48). 내막하혈관성형술과 관련하여 최근 발표된 체계적 고찰에 따르면, 총 87개의 연구에서 발표된 결과에서 1년 개통률이 22%에서 94.1%까지 너무 넓은 범위의 값을 나타냈고, 그나마 최근의 연구들은 70%에서 94.1%로 이전보다는 좋은 결과를 보였다. 또한, 시술 후 혈관파열과 같은 합병증도 1.6%에서 28%까지 다양하게 나타났다(49).
Fig. 3. Intraluminal angioplasty and subintimal angioplasty.
A. Intraluminal angioplasty: the catheter and guidewire are located in the true lumen (arrows).
B. Subintimal angioplasty: the catheter and guidewire are located in the false lumen outside the intima; the false lumen is extended to replace the true lumen (arrows).
Adapted from Korean Society of Interventional Radiology. Interventional radiology. 2nd ed. Seoul: Ilchokak 2014 (47).
내막하혈관성형술은 개통률 측면에서 다른 치료법들보다 뛰어나다고 볼 수는 없지만, 긴 폐쇄성 병변에서 인터벤션 치료의 기회가 좀 더 많아졌으며, 대상 환자들이 임계하지허혈 또는 그에 준하는 환자들이 많다는 점을 고려할 때 사지 구제(limb sal vage) 측면에서 주목할 필요가 있다.
Cutting Balloon
풍선 외벽에 4개의 긴 칼날이 부착되어 있는 풍선카테터로 증식된 내막의 섬유탄성조직의 지속성(fibroelastic continuity)을 단절시켜 탄력 반동을 방지하고, 일반적인 풍선혈관성형술에 반응하지 않는 협착을 해결하는 데 유용하게 사용된다. 대퇴슬와동맥 병변에서 고식적 풍선혈관성형술과의 비교에서 우수한 결과들을 보여주고는 있으나(50,51), 풍선의 길이가 짧아 긴 병변에서는 적용하기가 어렵다는 단점이 있다.
스텐트-그라프트설치술(Stent-Graft Placement)
스텐트 그라프트는 기존의 메탈 스텐트 틀에 polytetrafluoroethylene로 구성된 graft가 덮여 있는 것으로, 대퇴슬와동맥에서의 주요 적응증으로는 동맥류(aneurysm), 동정맥루(arteriovenous fistula) 및 혈관파열(vascular rupture) 등이 있다. 그라프트가 덮여 있어 스텐트 내부로 혈관내막 증식을 막을 수 있어 우수한 개통률을 기대하였으나, 스텐트를 뛰어넘는 우수한 결과가 증명되지 못하였다. Tsujimura 등(52)의 연구에 따르면, 10 cm 이상의 대퇴슬와동맥 병변에 대해 약물방출 스텐트인 Zilver PTX와 스텐트-그라프트인 Viabahn (Gore Medical, Flagstaff, AZ, USA)을 비교했을 때, 3년 개통률이 59.5% vs. 69.6%로 스텐트 그라프트가 더 좋은 것으로 나타났지만, freedom from stent thrombosis는 93.6% vs. 82.4%로 Zilver PTX가 더 좋게 보고되었다. 최근 헤파린을 부착한 스텐트 그라프트를 대퇴슬와동맥의 긴 병변에서 사용하였으나, 36개월 개통률이 40.6%라는 저조한 성적을 보여(53), 추후 더 많은 연구가 필요할 것으로 생각된다. 하지만, 현재 국내에서는 Goremedical이 철수하여 Viabahn의 국내 사용이 불가한 상황이다.
혈관 내 치료의 합병증
대퇴슬와동맥 혈관 내 치료의 주요 합병증은 주로 천자 부위와 시술 부위에서 발생할 수 있다. 천자 부위에 생길 수 있는 합병증으로는 혈종(hematoma), 가성 동맥류(pseudoaneurysm), 동정맥루(arteriovenous fistula) 등이 있고, 시술 부위에 발생하는 합병증으로는 혈전색전증(thromboembolism), 동맥박리(dissection), 동맥파열(rupture) 등이 있다. 혈전색전증은 흡인혈전제거술(aspiration thrombectomy)이나 혈전용해술(thrombolysis)로 해결할 수 있고, 동맥 박리는 스텐트 설치술, 동맥파열은 스텐트-그라프트 설치술로 해결할 수 있다(54). 스텐트 설치술의 주요 합병증으로는 스텐트 골절이 있다(39,40).
결론
식습관의 변화, 생활양식의 변화, 인구의 고령화 등 다양한 원인에 의해 대퇴슬와동맥을 포함하는 말초동맥질환의 유병률은 지속적으로 증가할 것으로 예상된다. 대퇴슬와동맥의 죽상경화증의 경우, 일반적으로 환자들의 나이가 많고, 급성 증상이 적으며, 병변이 여러 부위에 걸쳐 발생하는 등 추가적인 위험 요소들이 있다. 이 종설에서 살펴본 대로, 지난 20여 년간 혈관 내 인터벤션 시술은 전례 없이 발전하였으며, 다양한 연구들을 통해 지속적으로 기술의 향상 및 개선이 이루어지고 있다. 이로 인해 최근에는 말초동맥질환에 대한 치료가 수술적 치료를 벗어나 첫 번째 치료방식으로 혈관 내 인터벤션 시술로 전환되는 결과를 가져왔다. 따라서, 현시점에서 대퇴슬와동맥의 동맥 경화성 병변에 대한 주요 과제는 적절한 시기에 진단할 수 있도록 해당 질환의 환자들을 식별하고, 이들이 보다 적극적으로 치료하도록 초점을 맞추는 데 있다. 말초동맥질환의 인터벤션은 현재까지 확립된 방법 외에도 다양한 장비와 기술들이 임상검증단계에 있는데, 많은 연구를 통해서 보다 개선된 치료 결과가 검증되고, 다양한 모범적 치료 사례들이 알려진다면, 향후 인터벤션 시술을 이용한 동맥경화성 질환의 치료는 지속적으로 확장될 것으로 기대된다.
Acknowledgments
We would like to thank Dr. Hye Jin Baek for the useful comments on the manuscript and careful reading of the manuscript.
Footnotes
- Investigation, all authors.
- visualization, C.S.B.
- writing—original draft, C.S.B.
- writing—review & editing, all authors.
Conflicts of Interest: The authors have no potential conflicts of interest to disclose.
Funding: None
References
- 1.Song P, Rudan D, Zhu Y, Fowkes FJI, Rahimi K, Fowkes FGR, et al. Global, regional, and national prevalence and risk factors for peripheral artery disease in 2015: an updated systematic review and analysis. Lancet Glob Health. 2019;7:e1020–e1030. doi: 10.1016/S2214-109X(19)30255-4. [DOI] [PubMed] [Google Scholar]
- 2.Mohler ER., 3rd Peripheral arterial disease: identification and implications. Arch Intern Med. 2003;163:2306–2314. doi: 10.1001/archinte.163.19.2306. [DOI] [PubMed] [Google Scholar]
- 3.Gerhard-Herman MD, Gornik HL, Barrett C, Barshes NR, Corriere MA, Drachman DE, et al. 2016 AHA/ACC guideline on the management of patients with lower extremity peripheral artery disease: a report of the American College of Cardiology/American Heart Association Task Force on clinical practice guidelines. Circulation. 2017;135:e726–e779. doi: 10.1161/CIR.0000000000000471. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 4.Norgren L, Hiatt WR, Dormandy JA, Nehler MR, Harris KA, Fowkes FG, et al. Inter-society consensus for the management of peripheral arterial disease (TASC II) Eur J Vasc Endovasc Surg. 2007;33 Suppl 1:S1–S75. doi: 10.1016/j.ejvs.2006.09.024. [DOI] [PubMed] [Google Scholar]
- 5.Jaff MR, White CJ, Hiatt WR, Fowkes GR, Dormandy J, Razavi M, et al. An update on methods for revascularization and expansion of the TASC lesion classification to include below-the-knee arteries: a supplement to the Inter-Society Consensus for the management of peripheral arterial disease (TASC II) Ann Vasc Dis. 2015;8:343–357. doi: 10.3400/avd.tasc.15-01000. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 6.Aboyans V, Ricco JB, Bartelink MEL, Björck M, Brodmann M, Cohnert T, et al. 2017 ESC Guidelines on the Diagnosis and Treatment of Peripheral Arterial Diseases, in collaboration with the European Society for Vascular Surgery (ESVS): Document covering atherosclerotic disease of extracranial carotid and vertebral, mesenteric, renal, upper and lower extremity arteriesEndorsed by: the European Stroke Organization (ESO) The Task Force for the Diagnosis and Treatment of Peripheral Arterial Diseases of the European Society of Cardiology (ESC) and of the European Society for Vascular Surgery (ESVS) Eur Heart J. 2018;39:763–816. doi: 10.1093/eurheartj/ehx095. [DOI] [PubMed] [Google Scholar]
- 7.European Stroke Organisation. Tendera M, Aboyans V, Bartelink ML, Baumgartner I, Clément D, et al. ESC guidelines on the diagnosis and treatment of peripheral artery diseases: document covering atherosclerotic disease of extracranial carotid and vertebral, mesenteric, renal, upper and lower extremity arteries: the Task Force on the Diagnosis and Treatment of Peripheral Artery Diseases of the European Society of Cardiology (ESC) Eur Heart J. 2011;32:2851–2906. doi: 10.1093/eurheartj/ehr211. [DOI] [PubMed] [Google Scholar]
- 8.Caradu C, Lakhlifi E, Colacchio EC, Midy D, Bérard X, Poirier M, et al. Systematic review and updated meta-analysis of the use of drug-coated balloon angioplasty versus plain old balloon angioplasty for femoropopliteal arterial disease. J Vasc Surg. 2019;70:981–995.e10. doi: 10.1016/j.jvs.2019.01.080. [DOI] [PubMed] [Google Scholar]
- 9.Schneider PA, Laird JR, Tepe G, Brodmann M, Zeller T, Scheinert D, et al. Treatment effect of drug-coated balloons is durable to 3 years in the femoropopliteal arteries: long-term results of the IN. PACT SFA randomized trial. Circ Cardiovasc Interv. 2018;11:e005891. doi: 10.1161/CIRCINTERVENTIONS.117.005891. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 10.Laird JA, Schneider PA, Jaff MR, Brodmann M, Zeller T, Metzger DC, et al. Long-term clinical effectiveness of a drug-coated balloon for the treatment of femoropopliteal lesions. Circ Cardiovasc Interv. 2019;12:e007702. doi: 10.1161/CIRCINTERVENTIONS.118.007702. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 11.Xu Y, Liu J, Zhang J, Zhuang B, Jia X, Fu W, et al. Long-term safety and efficacy of angioplasty of femoropopliteal artery disease with drug-coated balloons from the AcoArt I trial. J Vasc Surg. 2021 doi: 10.1016/j.jvs.2021.01.041. [Epub] [DOI] [PubMed] [Google Scholar]
- 12.Hewes RC, White RI, Jr, Murray RR, Kaufman SL, Chang R, Kadir S, et al. Long-term results of superficial femoral artery angioplasty. AJR Am J Roentgenol. 1986;146:1025–1029. doi: 10.2214/ajr.146.5.1025. [DOI] [PubMed] [Google Scholar]
- 13.Lu CT, Zarins CK, Yang CF, Sottiurai V. Long-segment arterial occlusion: percutaneous transluminal angioplasty. AJR Am J Roentgenol. 1982;138:119–122. doi: 10.2214/ajr.138.1.119. [DOI] [PubMed] [Google Scholar]
- 14.Micari A, Vadalà G, Castriota F, Liso A, Grattoni C, Russo P, et al. 1-year results of paclitaxel-coated balloons for long femoropopliteal artery disease: evidence from the SFA-Long study. JACC Cardiovasc Interv. 2016;9:950–956. doi: 10.1016/j.jcin.2016.02.014. [DOI] [PubMed] [Google Scholar]
- 15.Micari A, Nerla R, Vadalà G, Castriota F, Grattoni C, Liso A, et al. 2-year results of paclitaxel-coated balloons for long femoropopliteal artery disease: evidence from the SFA-Long study. JACC Cardiovasc Interv. 2017;10:728–734. doi: 10.1016/j.jcin.2017.01.028. [DOI] [PubMed] [Google Scholar]
- 16.Hunink MG, Wong JB, Donaldson MC, Meyerovitz MF, Harrington DP. Patency results of percutaneous and surgical revascularization for femoropopliteal arterial disease. Med Decis Making. 1994;14:71–81. doi: 10.1177/0272989X9401400109. [DOI] [PubMed] [Google Scholar]
- 17.Muradin GS, Bosch JL, Stijnen T, Hunink MG. Balloon dilation and stent implantation for treatment of femoropopliteal arterial disease: meta-analysis. Radiology. 2001;221:137–145. doi: 10.1148/radiol.2211010039. [DOI] [PubMed] [Google Scholar]
- 18.Sapoval MR, Long AL, Raynaud AC, Beyssen BM, Fiessinger JN, Gaux JC. Femoropopliteal stent placement: long-term results. Radiology. 1992;184:833–839. doi: 10.1148/radiology.184.3.1509075. [DOI] [PubMed] [Google Scholar]
- 19.Laird JR, Katzen BT, Scheinert D, Lammer J, Carpenter J, Buchbinder M, et al. Nitinol stent implantation versus balloon angioplasty for lesions in the superficial femoral artery and proximal popliteal artery: twelve-month results from the RESILIENT randomized trial. Circ Cardiovasc Interv. 2010;3:267–276. doi: 10.1161/CIRCINTERVENTIONS.109.903468. [DOI] [PubMed] [Google Scholar]
- 20.Kawamura Y, Ishii H, Aoyama T, Tanaka M, Takahashi H, Kumada Y, et al. Nitinol stenting improves primary patency of the superficial femoral artery after percutaneous transluminal angioplasty in hemodialysis patients: a propensity-matched analysis. J Vasc Surg. 2009;50:1057–1062. doi: 10.1016/j.jvs.2009.07.017. [DOI] [PubMed] [Google Scholar]
- 21.Cejna M, Thurnher S, Illiasch H, Horvath W, Waldenberger P, Hornik K, et al. PTA versus Palmaz stent placement in femoropopliteal artery obstructions: a multicenter prospective randomized study. J Vasc Interv Radiol. 2001;12:23–31. doi: 10.1016/s1051-0443(07)61397-9. [DOI] [PubMed] [Google Scholar]
- 22.Grimm J, Müller-Hülsbeck S, Jahnke T, Hilbert C, Brossmann J, Heller M. Randomized study to compare PTA alone versus PTA with Palmaz stent placement for femoropopliteal lesions. J Vasc Interv Radiol. 2001;12:935–942. doi: 10.1016/s1051-0443(07)61572-3. [DOI] [PubMed] [Google Scholar]
- 23.Martin EC, Katzen BT, Benenati JF, Diethrich EB, Dorros G, Graor RA, et al. Multicenter trial of the wallstent in the iliac and femoral arteries. J Vasc Interv Radiol. 1995;6:843–849. doi: 10.1016/s1051-0443(95)71198-8. [DOI] [PubMed] [Google Scholar]
- 24.Sabeti S, Schillinger M, Amighi J, Sherif C, Mlekusch W, Ahmadi R, et al. Primary patency of femoropopliteal arteries treated with nitinol versus stainless steel self-expanding stents: propensity score-adjusted analysis. Radiology. 2004;232:516–521. doi: 10.1148/radiol.2322031345. [DOI] [PubMed] [Google Scholar]
- 25.Mewissen MW. Self-expanding nitinol stents in the femoropopliteal segment: technique and mid-term results. Tech Vasc Interv Radiol. 2004;7:2–5. doi: 10.1053/j.tvir.2004.01.007. [DOI] [PubMed] [Google Scholar]
- 26.Schillinger M, Sabeti S, Loewe C, Dick P, Amighi J, Mlekusch W, et al. Balloon angioplasty versus implantation of nitinol stents in the superficial femoral artery. N Engl J Med. 2006;354:1879–1888. doi: 10.1056/NEJMoa051303. [DOI] [PubMed] [Google Scholar]
- 27.Schillinger M, Sabeti S, Dick P, Amighi J, Mlekusch W, Schlager O, et al. Sustained benefit at 2 years of primary femoropopliteal stenting compared with balloon angioplasty with optional stenting. Circulation. 2007;115:2745–2749. doi: 10.1161/CIRCULATIONAHA.107.688341. [DOI] [PubMed] [Google Scholar]
- 28.Dick P, Wallner H, Sabeti S, Loewe C, Mlekusch W, Lammer J, et al. Balloon angioplasty versus stenting with nitinol stents in intermediate length superficial femoral artery lesions. Catheter Cardiovasc Interv. 2009;74:1090–1095. doi: 10.1002/ccd.22128. [DOI] [PubMed] [Google Scholar]
- 29.Duda SH, Bosiers M, Lammer J, Scheinert D, Zeller T, Oliva V, et al. Drug-eluting and bare nitinol stents for the treatment of atherosclerotic lesions in the superficial femoral artery: long-term results from the SIROCCO trial. J Endovasc Ther. 2006;13:701–710. doi: 10.1583/05-1704.1. [DOI] [PubMed] [Google Scholar]
- 30.Dake MD, Ansel GM, Jaff MR, Ohki T, Saxon RR, Smouse HB, et al. Paclitaxel-eluting stents show superiority to balloon angioplasty and bare metal stents in femoropopliteal disease: twelve-month Zilver PTX randomized study results. Circ Cardiovasc Interv. 2011;4:495–504. doi: 10.1161/CIRCINTERVENTIONS.111.962324. [DOI] [PubMed] [Google Scholar]
- 31.Dake MD, Ansel GM, Jaff MR, Ohki T, Saxon RR, Smouse HB, et al. Durable clinical effectiveness with paclitaxel-eluting stents in the femoropopliteal artery: 5-year results of the Zilver PTX randomized trial. Circulation. 2016;133:1472–1483. doi: 10.1161/CIRCULATIONAHA.115.016900. discussion 1483. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 32.Müller-Hülsbeck S, Keirse K, Zeller T, Schroë H, Diaz-Cartelle J. Twelve-month results from the MAJESTIC trial of the Eluvia paclitaxel-eluting stent for treatment of obstructive femoropopliteal disease. J Endovasc Ther. 2016;23:701–707. doi: 10.1177/1526602816650206. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 33.Müller-Hülsbeck S, Keirse K, Zeller T, Schroë H, Diaz-Cartelle J. Long-term results from the MAJESTIC trial of the Eluvia paclitaxel-eluting stent for femoropopliteal treatment: 3-year follow-up. Cardiovasc Intervent Radiol. 2017;40:1832–1838. doi: 10.1007/s00270-017-1771-5. [DOI] [PubMed] [Google Scholar]
- 34.Golzar J, Soga Y, Babaev A, Iida O, Kawasaki D, Bachinsky W, et al. Effectiveness and safety of a paclitaxeleluting stent for superficial femoral artery lesions up to 190 mm: one-year outcomes of the single-arm IMPERIAL long lesion substudy of the eluvia drug-eluting stent. J Endovasc Ther. 2020;27:296–303. doi: 10.1177/1526602820901723. [DOI] [PubMed] [Google Scholar]
- 35.Gray WA, Keirse K, Soga Y, Benko A, Babaev A, Yokoi Y, et al. A polymer-coated, paclitaxel-eluting stent (Eluvia) versus a polymer-free, paclitaxel-coated stent (Zilver PTX) for endovascular femoropopliteal intervention (IMPERIAL): a randomised, non-inferiority trial. Lancet. 2018;392:1541–1551. doi: 10.1016/S0140-6736(18)32262-1. [DOI] [PubMed] [Google Scholar]
- 36.Müller-Hülsbeck S, Benko A, Soga Y, Fujihara M, Iida O, Babaev A, et al. Two-year efficacy and safety results from the IMPERIAL randomized study of the eluvia polymer-coated drug-eluting stent and the zilver PTX polymer-free drug-coated stent. Cardiovasc Intervent Radiol. 2021;44:368–375. doi: 10.1007/s00270-020-02693-1. [DOI] [PubMed] [Google Scholar]
- 37.Bausback Y, Wittig T, Schmidt A, Zeller T, Bosiers M, Peeters P, et al. Drug-eluting stent versus drug-coated balloon revascularization in patients with femoropopliteal arterial disease. J Am Coll Cardiol. 2019;73:667–679. doi: 10.1016/j.jacc.2018.11.039. [DOI] [PubMed] [Google Scholar]
- 38.Bosiers M, Setacci C, De Donato G, Torsello G, Silveira PG, Deloose K, et al. ZILVERPASS study: ZILVER PTX stent vs bypass surgery in femoropopliteal lesions. J Endovasc Ther. 2020;27:287–295. doi: 10.1177/1526602820902014. [DOI] [PubMed] [Google Scholar]
- 39.Bosiers M, Deloose K, Callaert J, Moreels N, Keirse K, Verbist J, et al. Results of the Protégé EverFlex 200-mm-long nitinol stent (ev3) in TASC C and D femoropopliteal lesions. J Vasc Surg. 2011;54:1042–1050. doi: 10.1016/j.jvs.2011.03.272. [DOI] [PubMed] [Google Scholar]
- 40.Lammer J, Bosiers M, Zeller T, Schillinger M, Boone E, Zaugg MJ, et al. First clinical trial of nitinol self-expanding everolimus-eluting stent implantation for peripheral arterial occlusive disease. J Vasc Surg. 2011;54:394–401. doi: 10.1016/j.jvs.2011.01.047. [DOI] [PubMed] [Google Scholar]
- 41.Rosenfield K, Schainfeld R, Pieczek A, Haley L, Isner JM. Restenosis of endovascular stents from stent compression. J Am Coll Cardiol. 1997;29:328–338. doi: 10.1016/s0735-1097(96)00498-6. [DOI] [PubMed] [Google Scholar]
- 42.Zeller T, Langhoff R, Rocha-Singh KJ, Jaff MR, Blessing E, Amann-Vesti B, et al. Directional atherectomy followed by a paclitaxel-coated balloon to inhibit restenosis and maintain vessel patency: twelve-month results of the DEFINITIVE AR study. Circ Cardiovasc Interv. 2017;10:e004848. doi: 10.1161/CIRCINTERVENTIONS.116.004848. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 43.Katsanos K, Spiliopoulos S, Kitrou P, Krokidis M, Karnabatidis D. Risk of death following application of paclitaxel-coated balloons and stents in the femoropopliteal artery of the leg: a systematic review and meta-analysis of randomized controlled trials. J Am Heart Assoc. 2018;7:e011245. doi: 10.1161/JAHA.118.011245. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 44.Nordanstig J, James S, Andersson M, Andersson M, Danielsson P, Gillgren P, et al. Mortality with paclitaxel-coated devices in peripheral artery disease. N Engl J Med. 2020;383:2538–2546. doi: 10.1056/NEJMoa2005206. [DOI] [PubMed] [Google Scholar]
- 45.FDA. August 7, 2019 UPDATE: treatment of peripheral arterial disease with paclitaxel-coated balloons and paclitaxel-eluting stents potentially associated with increased mortality. [Assessed Aug 7, 2019]. Available at. https://www.fda.gov/medical-devices/letters-health-care-providers/august-7-2019-update-treatment-peripheral-arterial-disease-paclitaxel-coated-balloons-and-paclitaxel .
- 46.Bolia A, Miles KA, Brennan J, Bell PR. Percutaneous transluminal angioplasty of occlusions of the femoral and popliteal arteries by subintimal dissection. Cardiovasc Intervent Radiol. 1990;13:357–363. doi: 10.1007/BF02578675. [DOI] [PubMed] [Google Scholar]
- 47.Korean Society of Interventional Radiology. Interventional radiology. 2nd ed. Seoul: Ilchokak; 2014. [Google Scholar]
- 48.Lee HJ, Park SW, Chang IS, Jeon HJ, Park JH. Strategies for successful percutaneous revascularization of chronic total occlusion of the femoropopliteal arteries when the antegrade passage of a guide wire fails. Korean J Radiol. 2012;13:467–475. doi: 10.3348/kjr.2012.13.4.467. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 49.Kokkinidis DG, Katsaros I, Jonnalagadda AK, Avner SJ, Chaitidis N, Bakoyiannis C, et al. Use, safety and effectiveness of subintimal angioplasty and re-entry devices for the treatment of femoropopliteal chronic total occlusions: a systematic review of 87 studies and 4,665 patients. Cardiovasc Revasc Med. 2020;21:34–45. doi: 10.1016/j.carrev.2019.03.016. [DOI] [PubMed] [Google Scholar]
- 50.Cotroneo AR, Pascali D, Iezzi R. Cutting balloon versus conventional balloon angioplasty in short femoropopliteal arterial stenoses. J Endovasc Ther. 2008;15:283–291. doi: 10.1583/08-2366.1. [DOI] [PubMed] [Google Scholar]
- 51.Amighi J, Schillinger M, Dick P, Schlager O, Sabeti S, Mlekusch W, et al. De novo superficial femoropopliteal artery lesions: peripheral cutting balloon angioplasty and restenosis rates--randomized controlled trial. Radiology. 2008;247:267–272. doi: 10.1148/radiol.2471070749. [DOI] [PubMed] [Google Scholar]
- 52.Tsujimura T, Takahara M, Iida O, Soga Y, Katsuki T, Fujihara M, et al. Clinical outcomes of polymer-free, paclitaxel-coated stents vs stent grafts in peripheral arterial disease patients with femoropopliteal artery lesions. J Vasc Surg. 2021 Jan; doi: 10.1016/j.jvs.2020.12.061. [Epub] [DOI] [PubMed] [Google Scholar]
- 53.Böhme T, Noory E, Brechtel K, Scheinert D, Bosiers M, Beschorner U, et al. Heparin-bonded stent-graft for the treatment of TASC II C and D femoropopliteal lesions: 36-month results of the viabahn 25 cm trial. J Endovasc Ther. 2021;28:222–228. doi: 10.1177/1526602820965965. [DOI] [PubMed] [Google Scholar]
- 54.Pentecost MJ, Criqui MH, Dorros G, Goldstone J, Johnston KW, Martin EC, et al. Guidelines for peripheral percutaneous transluminal angioplasty of the abdominal aorta and lower extremity vessels. A statement for health professionals from a special writing group of the Councils on Cardiovascular Radiology, Arteriosclerosis, Cardio-Thoracic and Vascular Surgery, Clinical Cardiology, and Epidemiology and Prevention, the American Heart Association. Circulation. 1994;89:511–531. doi: 10.1161/01.cir.89.1.511. [DOI] [PubMed] [Google Scholar]