Abstract
Operationsziel
Wiederherstellung der Hüftkongruenz und des Containments durch zentrale Hüftkopfresektion/Reduktion über eine erweiterte chirurgische Hüftluxation unter Erhaltung/Respektierung der Hüftkopfdurchblutung. Eine gleichzeitige oder spätere Reorientierung des Acetabulums durch Triple-Osteotomie oder PAO bei instabiler Hüfte kann in speziellen Fällen notwendig werden.
Indikationen
Die Indikation zur chirurgischen Hüftkopfreduktion ist praktisch unabhängig vom Alter bei jeglicher inkongruenten, asphärischen Hüftkopfsituation mit „hinged abduction“ (zu erwartende Endsituation wie Stulberg IV und V) gegeben. Dies kann noch bei aktivem wie auch bei bereits ausgeheiltem Morbus Perthes der Fall sein. Zudem kann bei einer Stulberg-V-Situation selbst im adulten Alter noch eine Verbesserung erziel werden. Nach Resektion muss noch ein tragfähiger Resthüftkopf vorhanden bleiben, d. h. mindestens noch 50 % des ausgeweiteten Hüftkopfes. Die dafür beste Planung erfolgt in der „vergleichenden“ 3‑D-Rekonstruktion.
Kontraindikationen
Völlig zerstörter Knorpel oder Hüftkopf.
Operationstechnik
Identisches Operationsvorgehen wie für die klassische chirurgische Hüftluxation. Präparation der retinakulären Flaps. Unter Respektierung und in Kenntnis der Gefäßversorgung Spaltung des Hüftkopfes gemäß dem zu entfernenden, nekrotischen Kopfanteil. Bildung eines möglichst sphärischen Hüftkopfes und Verschraubung der beiden Kopfanteile auf Schenkelhalsniveau. Distalisation und Fixierung des großen Trochanters. Je nach Kongruenz und Stabilität des Hüftkopfs in der Hüftpfanne kann eine primäre oder sekundäre Triple-OT oder PAO notwendig werden.
Weiterbehandlung
Die intraoperative Stabilität des Femurkopfes im Acetabulum muss erzielt worden sein, um eine beckengipsfreie, funktionelle Nachbehandlung zu gewährleisten: Stockentlastung mit Bodenkontakt ist erlaubt; keine aktive Rotation; Flexion aktiv und passiv bis 90 Grad ist erlaubt; vorerst keine spezifische Physiotherapie; je nach Heilungsverlauf sind diese Maßnahmen 8 bis 10 Wochen einzuhalten.
Ergebnisse
Gemäß unseren publizierten Nachuntersuchungen (aktuell 21 Jahre) sehen wir bei technisch korrekt durchgeführter Operation und korrekter Indikation sowie adäquater Nachbehandlung durchwegs gute Ergebnisse. Nekrosen des reduzierten Hüftkopfs haben wir nie beobachtet. Alle gespaltenen Hüftköpfe, respektive Schenkelhälse sind primär geheilt.
Schlüsselwörter: Asphärizität Hüftkopf, Inkongruenz, Containment-Verlust, Hüftkopfreduktion, Chirurgische Hüftluxation
Abstract
Objective
Restoration of hip congruence and containment through central femoral head resection/reduction via an extended surgical hip dislocation, while maintaining/respecting the femoral head blood flow. Simultaneous or subsequent reorientation of the acetabulum by triple TPO (Pediatric Triple Osteotomy) or PAO (Peri-Acetabular Osteotomy) may be necessary.
Indications
Surgical hip dislocation with femoral head reduction can be performed at any age in cases with hinge abduction and Stulberg class IV and V deformity. Procedure indicated for patients with active or healed disease. After the resection, a viable residual femoral head must remain, i.e. at least 50% of the expanded femoral head, which is best planned using “comparative” 3D reconstruction.
Contraindications
Completely destroyed cartilage or femoral head.
Surgical technique
The same surgical procedure as described for classic surgical hip dislocation is followed. Preparation of retinacular flaps. With detailed knowledge of the vascular supply and precise execution of this technique, blood supply to the femoral head will be preserved; once safely surgically dislocated, the femoral head and neck can be split and the necrotic part of the femoral head removed. Reformation of the femoral head as spherical as possible is achieved by screw fixation of the femoral neck to align the two articular parts of the femoral head. Distalization and fixation of the great trochanter helps to restore offset (functional femoral neck length). Depending on the congruence and stability of the femoral head in the acetabulum, a primary TPO or PAO may also be necessary.
Postoperative management
Intraoperative stability must be achieved to ensure functional posttreatment without a hip spica cast. Walking with crutches with toe contact only is advised. Active rotation is not allowed. Active and passive flexion up to 90° allowed. These measures have to be observed for 8–10 weeks. Then, active physiotherapy rehabilitation may commence, depending on healing, as assessed clinically and radiologically.
Results
Our published follow-up examinations (currently 21 years) show consistently good results with a technically correct operation and correct indication as well as adequate follow-up treatment. No necrosis of the reduced femoral head has been observed. All split femoral heads and femoral necks are primarily healed.
Keywords: Femoral head asphericity, Incongruence, Loss of containment, Femoral head reduction, Surgical hip dislocation
Vorbemerkungen
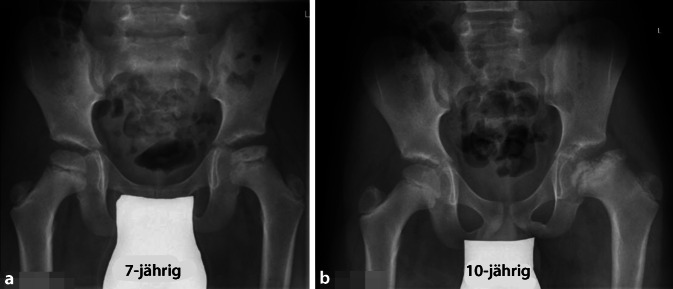
Der Verlauf eines Morbus Perthes ist extrem variabel, von kaum sichtbaren Veränderungen des Femurkopfes bis hin zu schwersten Deformitäten und steifen Hüftgelenken. Dabei ist zu beobachten, dass die Symptomatik nicht immer synchron zur Schwere und der zu erwartenden Kopfdeformität einhergeht. Wir gehen davon aus, dass sehr viele Erkrankungen „stumm“ verlaufen und unter Umständen wegen Früharthrose der Hüfte erst im Alter von 30 oder 40 Jahren retrospektiv diagnostiziert werden [6, 19].
Lange Zeit hat man sich nur auf die von Catterall [2, 4] erstellten Stadieneinteilung verlassen, um die Schwere des Verlaufes einzuschätzen, später kamen andere Einteilungen wie die „Lateral Pillar“-Klassifikation [1] und andere dazu. Auf der anderen Seite haben Stulberg et al. eine Klassifikation geschaffen, die „post festum“ das Ausheilungsergebnis beschreibt [4, 12].
Zwischenzeitlich hat sich eine differente Betrachtungsweise des Morbus-Perthes-Verlaufes eingestellt. Es wird mehr Wert auf die Entwicklung/Beziehung der Stellung zwischen Hüftkopf und Hüftpfanne gelegt. Das große Schlagwort heißt dabei „Containment“ und beschreibt die Relation zwischen dem Hüftkopf, praktisch unabhängig der Schwere des Kopfbefalles, und der Hüftpfanne. Solange diese Relation stimmt und der Hüftkopf ein perfektes Containment zeigt, ist im Prinzip keine spezifische Therapie notwendig, zeigt sich jedoch im Verlauf, auch wenn der Hüftkopf nur gering befallen ist, dass dieses Containment nur minimal verloren geht, sollte eine Containment-verbessernde Operation im Sinne einer Triple Osteotomie/PAO oder milden intertrochantären Osteotomie angestrebt werden [6, 15]. Eine Salter-Osteotomie empfehlen wir wegen der zusätzlichen Lateralisation, Druckerhöhung und der Gefahr der Retroversion nicht.
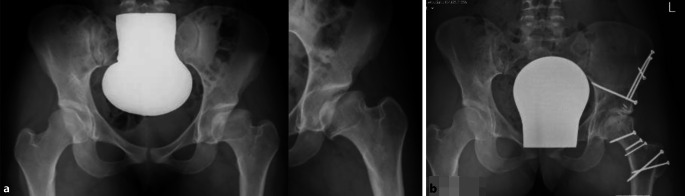
Da sich einerseits diese Denkweise der optimalen Containment-Erhaltung noch nicht flächendeckend durchgesetzt hat, sehen wir im Früh- wie auch dann im Spätstadium schwere Kopfdeformierungen, die man sicherlich hätte vermeiden können. Auf der anderen Seite, wie oben beschrieben, gibt es sehr stille Verläufe, wo die Symptomatik erst in einem späten Stadium aufgrund von schon vorhandenen Gelenkschäden auftritt. Der Femurkopf hat dabei eine typische, asphärische, inkongruente Form (als Stulberg IV und V bezeichnet) und ist oft auch massiv vergrößert, dafür jedoch abgeflacht. Er weist die typische „Champignon“-Form auf, wobei der Kopfrand meist den Schenkelhals überragt. In der Literatur wird dafür der Term „coxa magna“ oder „coxa plana“ verwendet. Der vergrößerte und abgeflachte Kopf verliert sein Containment und lateralisiert sich. Dabei kommt es zum typischen Impingement und progressiver Zerstörung des Labrums bis hin zum knöchernen, lateralen Pfannenrand [6, 19, 21]. Passiert dieser Prozess in einem frühen Stadium der Krankheit, resultiert durch Abduktion der Hüfte ein „zweihöckriger“ Hüftkopf als sog. „Kamelbuckel-Form“. Funktionell resultiert die in der Literatur beschriebene „hinged abduction“, welche dazu führt, dass der Femurkopf progredient bei jeder Abduktion aus der Pfanne gehebelt wird ([22]; vgl. Abb. 2). Die Delle zwischen den beiden Höckern entspricht auch meist der Region mit der ausgeprägtesten Nekrose.
In der Vergangenheit wurde versucht, dieses Problem durch augmentierende Operationen wie die Chiari Osteotomy oder Shelf-Operationen zu behandeln. Dabei konnte jedoch die Kopfdeformität nie adressiert werden, sondern die Operation bestand darin, den extraartikulären Kopfanteil zu überdachen. Die Sphärizität wurde nicht verbessert. Zudem hat man versucht, mehrheitlich im Frühstadium, durch eine varisierende proximale Femurosteotomie den Hüftkopf wiederum ins Acetabulum einzustellen, was prinzipiell nur möglich ist, wenn die Abduktionsaufnahme eine Reposition der Hüfte zeigt. Definitionsgemäß ist dies jedoch bei einem 2‑höckrigen Hüftkopf mit „hinged abduction“ nicht möglich.
Der direkte Einblick in die Hüfte respektive auf den vom Perthes veränderten Hüftkopf aufgrund einer heute als sicher geltenden operativen Methode zur Luxation des Hüftkopfes [5] hat einerseits das Verständnis um die Veränderungen an der Hüfte in vielen Belangen verändert und verbessert, andererseits aber auch den Weg zu einem aktiven chirurgischen Vorgehen direkt am Ort der Veränderung ermöglicht – dies im Gegensatz zu all den bisherigen, bekannten operativen Verfahren am proximalen Femur oder an der Hüftpfanne, die fernab der eigentlichen Deformität des Hüftkopfes korrigieren und in den meisten Fällen in sekundären, durch die Operation bedingten Veränderungen enden, wie z. B. groteske Varusstellungen nach intertrochantärer Osteotomie [3]. Die Erfahrungen der ersten 21 Jahre sind sehr Erfolg versprechend und zeigen zumindest über diese Zeitperiode bei allen Patienten eine sehr gute Funktion und Hüftsituation, die einen allfälligen hüftprothetischen Ersatz deutlich in ein späteres Alter zu verschieben mag [8–11, 16, 17].
Um eine sichere Femur-Kopf-Verkleinerungsoperation vornehmen zu können, ist die Kenntnis der Blutversorgung am proximalen koxigialen Femurende [7, 8] ebenso notwendig wie die Beherrschung der schonenden und sicheren chirurgischen Hüftluxation [14]. Im vorliegenden Artikel sollen deshalb nur die wesentlichsten Schritte der chirurgischen Hüftluxation dargestellt werden. Das Hauptaugenmerk ist dabei auf die Präparation der reticulären Flaps und der eigentlichen Kopfverkleinerung gerichtet. Zum Studium der Präparation der retinakulären Flaps wie der chirurgischen Hüftluxation sei folgende Literatur empfohlen: [5, 8, 11, 16, 20].
Operationsprinzip und -ziel
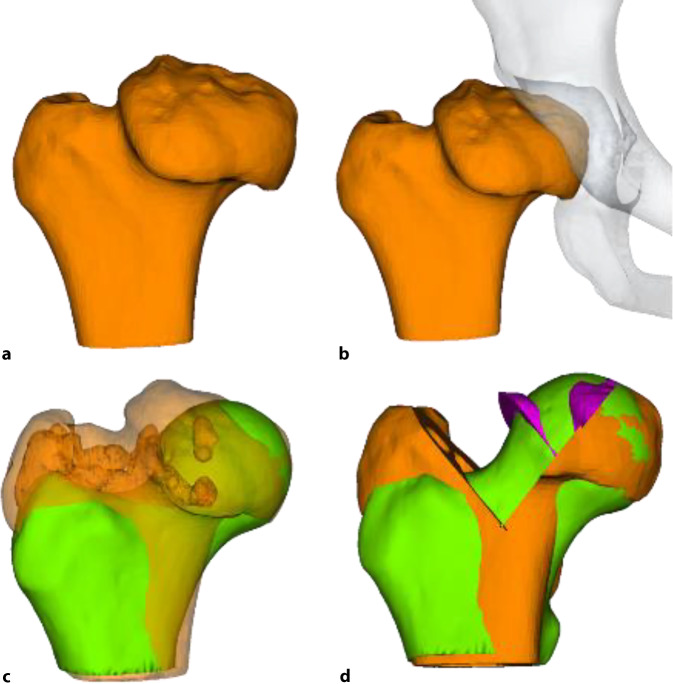
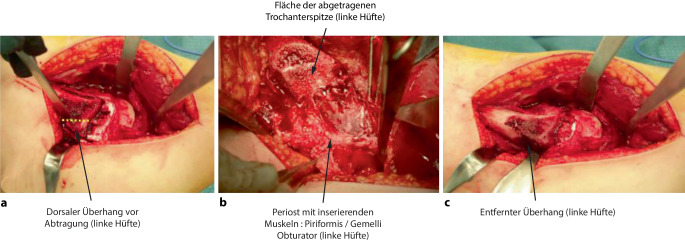
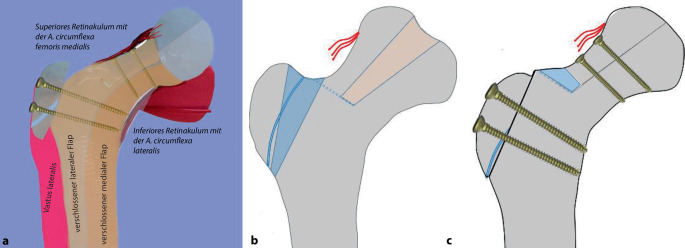
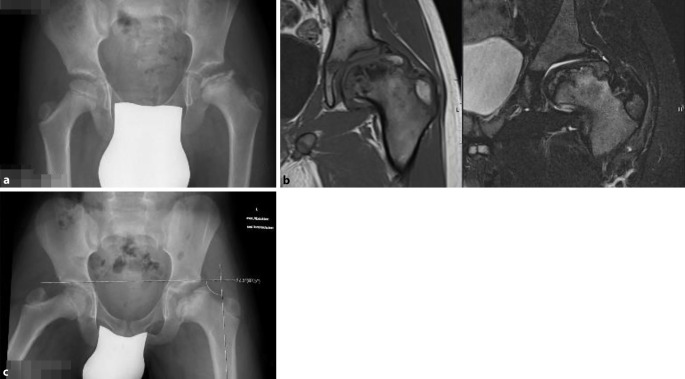
Das Operationsprinzip besteht darin, dass man über eine heute als sicher durchführbar und somit als sicher geltende chirurgische Hüftluxation den vollen 3‑dimensionalen Überblick auf den veränderten Hüftkopf bekommt [5]. Anhand der vorgängig durchgeführten hochauflösenden MRI-Untersuchung sowie der vor Ort sich darstellenden Situation wird eine zentrale Hüftkopfresektion vorgenommen, um eine bestmögliche Sphärizität zu erreichen. Die Schnittführung für eine optimale Sphärizität kann heute auch vorgängig aufgrund einer 3‑D-CT-Planung (Abb. 1a–c) vorgenommen werden, da diese Planung einen Vergleich mit der gesunden Seite erlaubt (Abb. 1d). Man muss sich jedoch bewusst sein, dass dies eine „theoretische“ Planung ist und allfällig wegen der Gefäßversorgung nicht genau so durchgeführt werden kann. Deshalb sei nochmals betont, dass die Kenntnis um die Gefäßversorgung des Hüftkopfs absolute Voraussetzung für diese Operation ist.
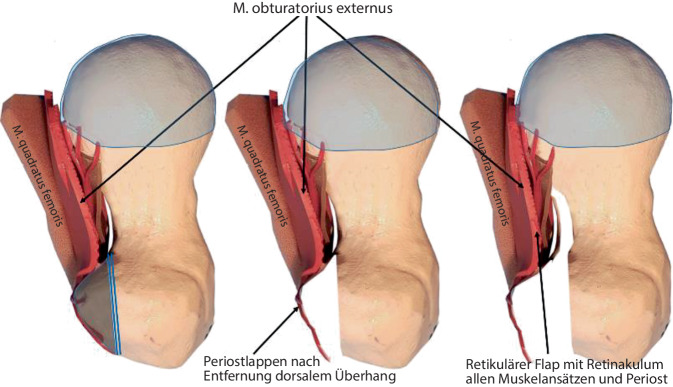
Es kann kaum genügend betont werden, wie wichtig es ist, die sog. retinakulären Flaps zu bilden, um die Blutversorgung der verbleibenden Kopfanteile sicherzustellen [8]. Schlussendlich ist das Operationsziel, eine möglichst optimale Kongruenz/Containment der Hüfte zu erreichen mit einer bestmöglichen Restfunktion. Es ist evident, und es wäre illusorisch zu behaupten, dass man auf jeden Fall eine normale Hüftfunktion erreichen kann. Diese Operation soll dem Patienten bei fehlenden anderen äquivalenten Möglichkeiten erlauben, über eine Periode von 20 bis 30 Jahren einer normalen täglichen Aktivität nachzugehen, ohne dabei von Schmerzen geplagt zu werden. Dass dieses Ziel erreicht werden kann, zeigen die ersten Resultate nach 21 Jahren.
Vorteile
Bestmögliche Wiederherstellung der Hüftkopfsphärizität
Verbesserung der Funktion
Reduktion der Früharthrose
Nachteile
Gefahr der zusätzlichen Verschlechterung der Hüftkopfzirkulation durch unsachgemäßer chirurgischer Hüftluxation
Heilungsstörungen
Erfordert fundierte hüftchirurgische Kenntnisse
Im Falle einer verbliebenen Incongruenz infolge eines „ausgeweiteten Acetabulum“ sollte dies erkannt und durch eine zusätzliche PAO oder Triple OT behoben werden.
Indikationen
Die Indikationsstellung richtet sich im Wesentlich nach den nachfolgend aufgeführten Punkten. Im Einzelnen müssen diese sehr gut abgewogen, auf alternative Verfahren geprüft und diskutiert werden. „Harte“ Fakten existieren im Moment noch nicht. Wichtig scheint uns, dass sicherlich noch 50 % des ursprünglich deformierten Kopfes nach der Resektion einen noch tragfähigen Hüftkopf bilden können. Um diese Abschätzung bereits präoperativ machen zu können, wird sich in Zukunft sicherlich die vergleichende 3‑D-Darstellung eignen (nicht berücksichtigt wird hier die Gefäßversorgung).
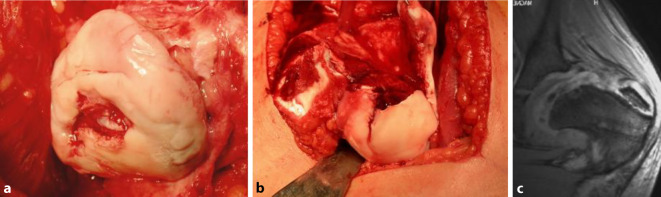
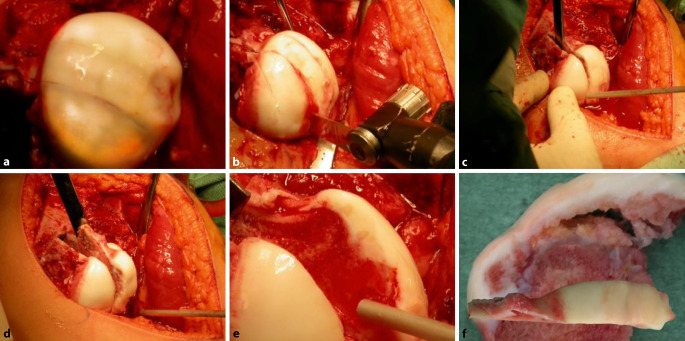
Der Zustand des Knorpels im zu entfernenden Kopfanteil sowie die Tiefe der Nekrose spielen dabei keine Rolle. Obwohl eine obligate MRT-Untersuchung gute Anhaltspunkte über den Kopf-/respektive Knorpelzustand geben kann, zeigt doch die klinische Erfahrung, dass die abschließende Beurteilung nur bei luxierter Hüfte gemacht werden kann. Der in Abb. 3 dargestellte Kopf zeigte sich im MRT als stabil in den Randzonen, intraoperativ jedoch war eine Rekonstruktion im Sinne der Kopfreduktion nicht möglich. Hier wurde ein Kopfaufbau mit trikortikalem Knochenblock durchgeführt.
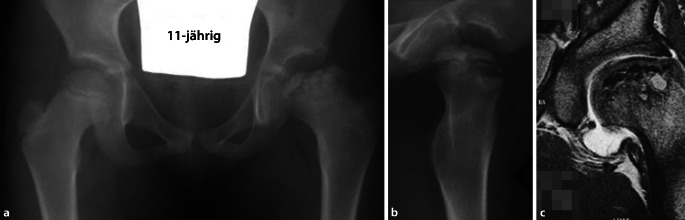
Jegliche Inkongruenz, Asphärizität des Hüftkopfes praktisch unabhängig vom Alter (Stuhlberg IV und V) wie in Abb. 2a ersichtlich ist
„Hinged abduction“
Noch aktiver oder bereits abgeschlossener Morbus Perthes
Kontraindikationen
Völlig zerstörter Hüftkopf (Abb. 3)
Kinder unter 6 bis 8 Jahren (nur bedingte KI)
Patientenaufklärung
Offene und umfassende Aufklärung der Eltern/Patienten über alle möglichen Behandlungsverfahren zur Behandlung von Komplikationen beim Morbus Perthes
Begründung, weshalb in der vorliegenden Situation dieses Verfahren gewählt wird
Allgemeine Operationsrisiken
Spezifische Risiken dieser Operation wie: Nichtverheilen der beiden zusammengefügten Kopfanteile, Nekrose der verbleibenden Kopfanteile, verzögerte Heilung der Trochanterosteotomie
Allfällige Erweiterung des Eingriffes im Sinne einer PAO respektive Triple-OT
Mögliche Zweitoperation im Falle einer Hüftinstabilität, die initial nicht so eingeschätzt wurde
Mögliche residuelle Fehlstellungen oder Fehlfunktionen
Diskussion, weshalb ein Hüftgelenkersatz in diesem Alter nicht als sinnvolle Alternative gesehen werden kann
Angebot einer krankenhausexternen Pflege
Heilungsdauer
Physiotherapie
Operationsvorbereitungen
Röntgen Becken a.-p. sowie Abduktionsaufnahme zur Verifizierung der „hinged abduction“
MRT (wenn immer möglich Arthro-MRT und radiäre Sequenzen) zur Beurteilung des Nekroseausmaßes
Bildanalyse und evtl. Studium zusätzlicher bildgebender Verfahren
Zumindest skizzenhafte Planung der möglichen Schnittführung durch den Femurkopf und Ausmaß der Reduktion, am besten anhand der speziellen radiären MRT-Sequenzen
CT- und 3‑D-Darstellung nicht obligat, kann im Einzelfall hilfreich sein zur Planung der Resektionsflächen (noch in der experimentellen Phase der Umsetzung)
Lagerungsmaterial bereitstellen
Möglichkeit der intraoperativen Durchleuchtung prüfen
Besprechung mit der Anästhesie bezüglich Relaxation, Blutverlust und Operationsdauer; allfällig Einsatz eines „Cell Saver“
Orientierung/Besprechung dieses komplexen Eingriffes mit dem OP-Personal
Instrumentarium
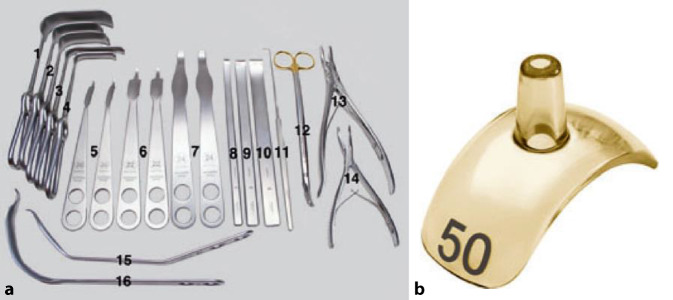
Bei diesem doch sehr spezifischen und komplexen Eingriff ist das richtige Instrumentarium von entscheidender Wichtigkeit; dies wird sehr oft unterschätzt. Wir empfehlen das von uns entworfene und über spezialisierte Instrumentenfirmen1 vertriebene Instrumentenset. Dieses sollte als Minimum folgende Instrumente enthalten:
verschieden breite und hohe Wundretraktoren mit abgerundeten Kanten (Breite 14 mm, 25 mm, 30 mm; Höhe 55 mm, 70 mm, 100 mm), alle in zweifacher Ausführung
Je 2 Hohmann Haken schmal 8 mm und breit 18 mm
Je 2 große und kleine, sog. „reversed“ abgerundete Hohmann-Haken
240 mm lange schmale (10 mm), mittlere (15 mm) und breite (20 mm) Lambotte (Simal)-Meißel gerundet
Nervenhäkchen lang
Lange, stark gekurvte Schere (aus Gynäkologie bekannt)
Zwei verschieden große und scharfe Rongeur-Zangen
Kräftiger 1‑Zinker-Haken zum Hochheben des Femurs bei der Luxation
Doppelt gekrümmter langer Hohmann-Haken (bei uns Giraffe genannt)
Lang gebogener, breiter Hohmann-Haken (auch Easy Rider genannt)
FAI (Femoral Template) zur Überprüfung der Grösse und Sphärizität (42–58 mm) des zerstörten Hüftkopfes (Abb. 4)
Anästhesie und Lagerung
Intubationsnarkose; Relaxation ist Voraussetzung und erleichtert die Präparation und Luxation
Epiduralkatheter zur postoperativen Schmerztherapie
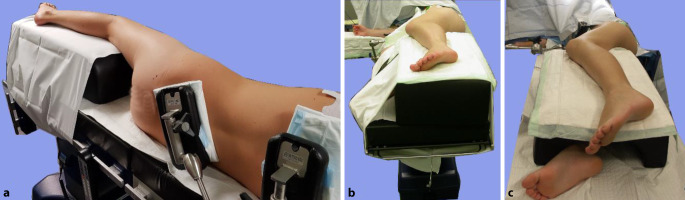
- Je nach Durchleuchtungstechnik
- C‑Arm so positionieren, dass er über den Patienten gefahren werden kann oder
- unter dem Operationstisch durch. Diese Positionierung lässt aus Sterilitätsgründen (die unter dem Operationstisch nicht gegeben ist) weniger Manipulationen des C‑Armes zu (Abb. 5).
Wir bevorzugen wegen des besseren Bildes, des größeren Bildausschnittes, der genaueren Durchleuchtungspositionierung und der dadurch kürzeren Durchleuchtungszeit, dass die Bildplatte des Durchleuchtungsgerätes direkt von dorsal am Patienten anliegt (Abb. 5).
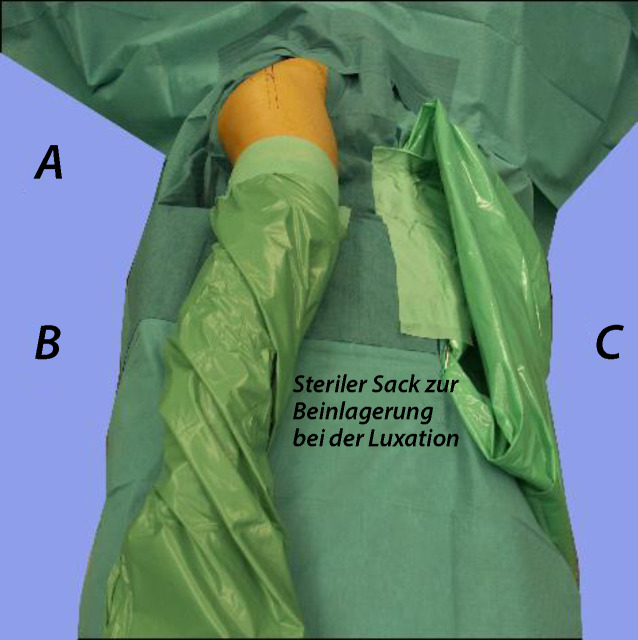
Desinfektion und Abdeckung des ganzen Beines bis auf Höhe des Nabels. Der Unterschenkel bis Mitte Oberschenkel wird dann zusätzlich steril eingepackt.
Anbringen eines sterilen Sackes auf der ventralen Operationstischseite des Patienten zwecks steriler Lagerung des Unterschenkels nach der Hüftluxation [5].
Operationstechnik
Abb. 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19 und 20.
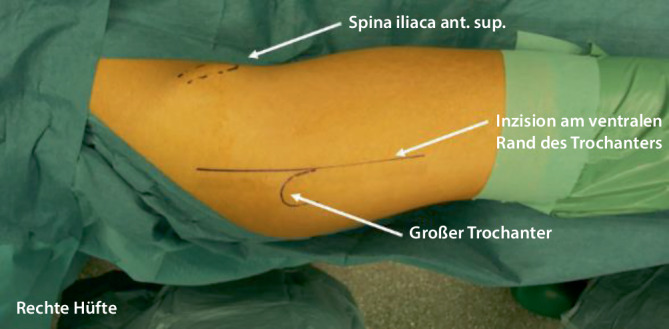
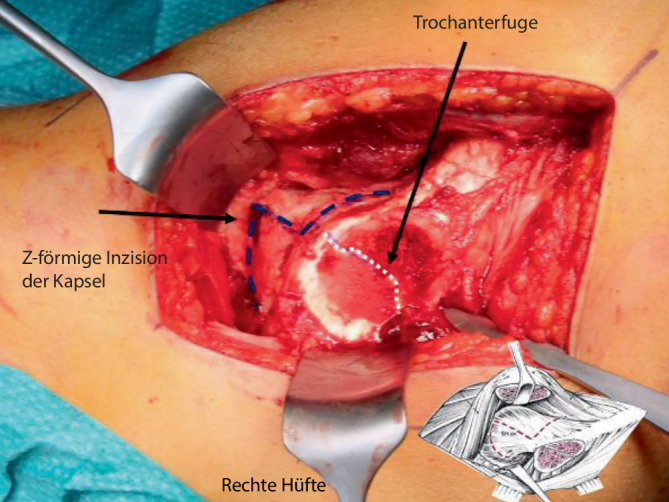
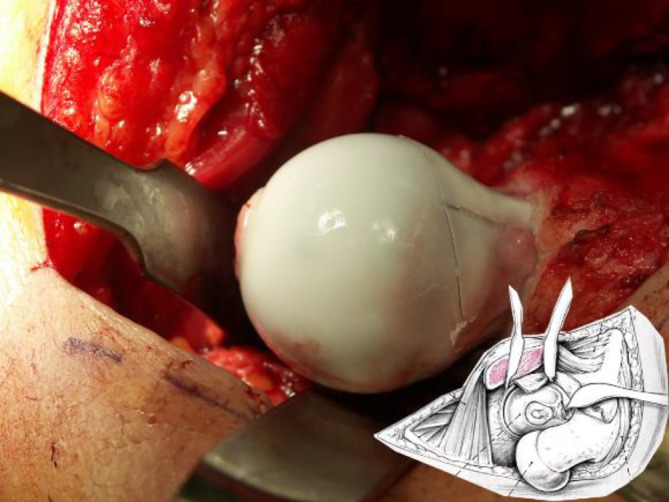
Schritt 1: Lagerung und chirurgische Hüftluxation
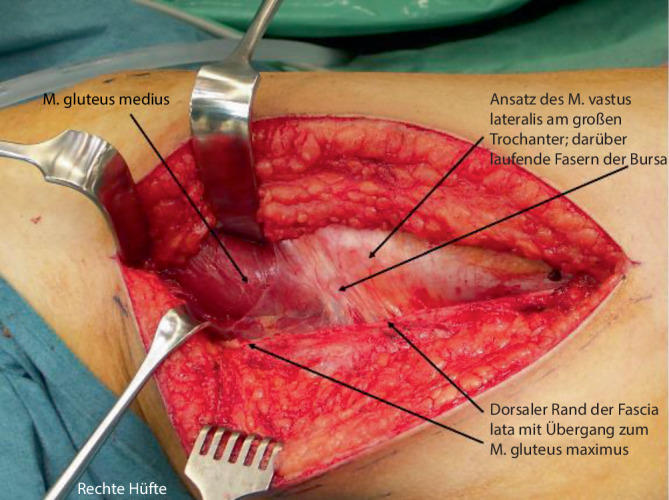
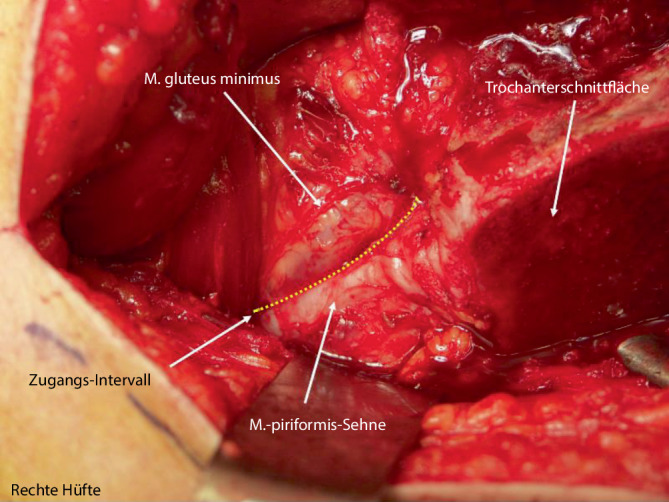
Schritt 2: Präparation der retinakulären Flaps
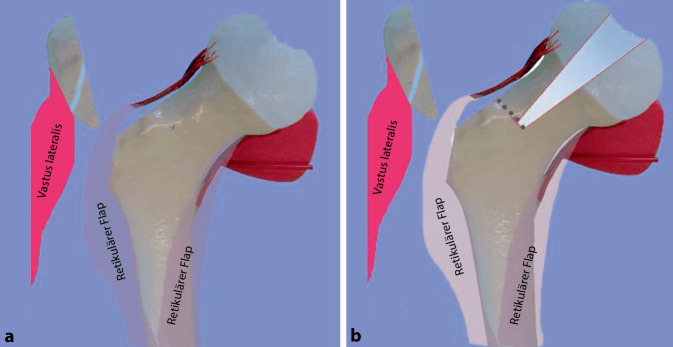
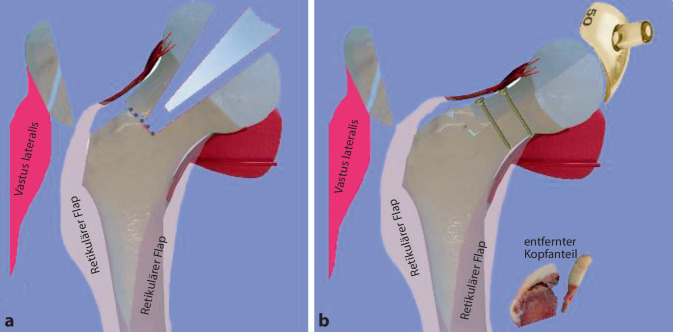
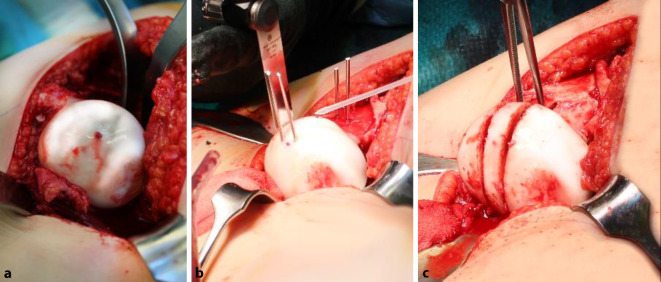
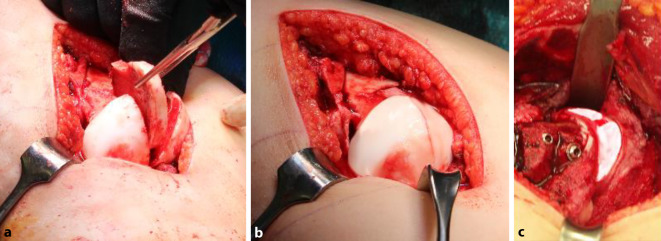
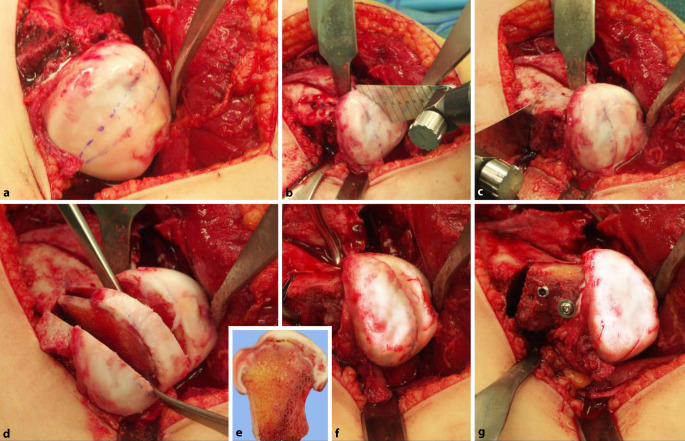
Schritt 3: Hüftkopfreduktionsplastik
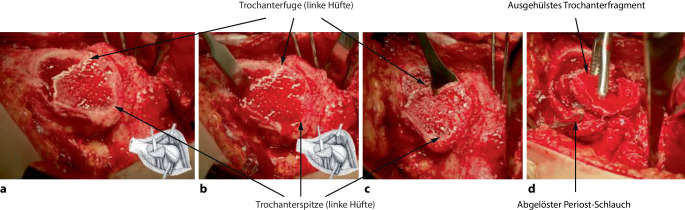
Die Abb. 18, 19 und 20 zeigen die einzelnen Schritte anhand des von uns anhand von CT-Bildern angefertigten Knochenmodelles.
Besonderheiten
Nach stabiler Verschraubung der Kopfanteile und Readaptation der beiden Flaps/Retinacula + Gefäße erfolgt die behutsame Reposition der Hüfte. Ein Einklemmen der Gefäße muss vermieden werden … Oft ist aufgrund der Kopfdeformität das Acetabulum „ausgeweitet“ und der Hüftkopf steht nicht stabil in der Pfanne, oder wir haben ein extremes Missverhältnis zwischen Kopf- und Hüftpfannenradius. Es ist wichtig, sich dieses Umstandes bewusst zu sein und zu entscheiden, brauche ich eine stabilisierende Zusatzoperation im Sinne einer Triple-OT oder PAO, oder kann ich zuwarten. Wie von uns in der Literatur beschrieben [16–18], ist dieser Entscheid nicht immer einfach, die Stabilität sollte aber immer angestrebt werden. Es ist auch wichtig, dass im Vorfeld der Operation der Patient respektive die Eltern darüber in zweierlei Hinsicht orientiert worden sind; erstens, dass es im Entscheid des Operateurs liegen muss, ob gleichzeitig eine Pfannen-Schwenk-Operation gemacht wird, oder zweitens, dass es sein kann, dass innerhalb von Monaten eine solche Operation durchgeführt werden muss, sollte sich zeigen, dass die Hüfte nicht stabil ist. In unserem Krankengut, das inzwischen größer ist als die publizierten Fälle, zusätzlich die noch in Drittkliniken versorgten Fälle haben wir in etwa folgende Situation: 40 % brauchen keine zusätzliche azetabuläre Korrektur, weder initial noch später, ca. 30 % brauchen initial eine Triple oder PAO und 30 % innerhalb des ersten Jahres. Bei diesen Zahlen besteht die berechtigte Frage, weshalb man nicht bei allen unsicheren Fällen gleich zur Pfannenoperation übergeht. Dieser Entscheid ist nicht nur aus ärztlicher Sicht zu sehen, sondern wird auch durch die Ansprüche, Wünsche des Patienten mitbeeinflusst. Tendenziell möchte der Patient so wenig wie möglich operiert haben, obwohl von der Sache her doch eine umfassende Operation angezeigt wäre. Es ist dann das Geschick und die Kompetenz des Chirurgen, den Patienten von der Notwendigkeit eines kombinierten Eingriffs zu überzeugen.
Im Weiteren ist ebenfalls wichtig zu erklären, dass nach einer solchen Operation die Hüfte niemals „normal“ sein kann; Ziel ist es, die initial schwerstens veränderte Hüfte für einen möglichst langen Zeitraum schmerzfrei und funktionsfähig zu halten. Aktuell überblicken wir einen Zeitraum von 21 Jahren und können feststellen, dass weit über 80 % der Patienten keine weitere Operation brauchten.
Sicher ist auch zu diskutieren, was man bei völlig zerstörtem Hüftkopf, der sich jedoch im MRT nicht so dargestellt hat (Abb. 3), als intraoperativen Plan B hat. Für uns ist bis heute der Einbau einer Hüfttotalprothese keine Option; vielmehr würden wir in dieser Situation auf eine Arthrodese ausweichen. Der Hauptgrund gegen TP in diesem Alter ist das Überstrapazieren der TP durch den jugendlichen Übermut und Aktivität! Die Arthrodese kann dann im höheren Alter, falls notwendig, in eine TP umgewandelt werden. Die Diskussion über dieses Vorgehen ist sicherlich noch offen, ist aber in unserer Praxis der adäquateste Schritt. Zudem wird diese Option im Vorfeld mit dem Patienten respektive den Eltern immer diskutiert.
Postoperative Behandlung
Prinzipiell unterscheidet sich die postoperative Behandlung nicht wesentlich von anderen hüfterhaltenden Operationen wie Impingement, SCFE oder relativer SH-Verlängerung oder selbst nur intertrochantären Korrekturen.
Radiologische Kontrolle mit Becken a.‑p. unmittelbar postoperativ sowie nach 6 bis 8 Wochen zur Konsolidations- und Stellungskontrolle
Mobilisation in der Sagittalebene Flexion/Extension bis 60°, vorzugsweise mit CPM
Stockentlastung mit Bodenkontakt
Nach sicherer Konsolidation Übergang zur Vollbelastung und Beginn mit rotatorischen Übungen und Krankengymnastik
Sportverbot für mindestens 3 Monate
Eine routinemäßige Thromboseprophylaxe sehen wir aufgrund der fehlenden Evidenz und der eigenen Erfahrung im Kindes- und Jugendalter nicht als indiziert; Ausnahmen bilden Übergewicht, rauchen, Antikonzeption, familiäre Belastung
Fehler, Gefahren, Komplikationen
Der größte Fehler besteht darin, ohne genügend Erfahrung oder Beiziehen eines erfahrenen Kollegen, sich an eine solche Operation zu wagen!
Verursachen einer AVN als schwere Komplikation schon rein durch den Zugang zur Hüfte, der lediglich als eigentliche Vorbereitung der Chirurgie am Hüftkopf gilt
Fehlende Kenntnis der retikulären Flap-Präparation
Trotz Femurkopfverkleinerung keine genügende Reposition → Überprüfen der azetabulären Situation, allfällig zusätzlich Pfannenschwenkung
Non-Union des Trochanter major → bessere Fixierung
Schädigung des N. ischiadicus durch ungenügend ausgedehnte Präparation für die chirurgische Hüftluxation
Heterotope Ossifikationen (beim Jugendlichen selten)
Intraartikuläre Verwachsungen mit massiver Bewegungseinschränkung → allfällig arthroskopische Revision und Adhäsiolyse
Trotz optimaler Operation rasch fortschreitende Verschlechterung der Hüftsituation; möglicher Grund: falsch eingeschätzte, bereits zu fortgeschrittene Knorpelzerstörung respektive auf azetabulärer Seite Delamination (auch als Carpet-Phänomen bezeichnet) des Knorpels
Ergebnisse
Unsere Erfahrungen mit der Hüftkopfreduktionsplastik über eine chirurgische Hüftluxation sind über die letzten 15 Jahre sehr positiv. Wie unseren in dieser Zeit durchgeführten Publikationen [8, 11, 16, 17] zu entnehmen ist, haben wir keine chirurgisch-technischen Komplikationen wie auch keine Nekrose des freien, nur noch am superioren Retinaculum hängenden Kopfanteiles gesehen. Dies ist sicherlich auch darauf zurückzuführen, dass diese Operationen praktisch nur durch 4 eng miteinander zusammenarbeitende Chirurgen durchgeführt wurde. Auch von den zahlreichen als Teaching-Operation durchgeführten Eingriffen in Drittkliniken kamen nur positive Rückmeldungen. Dennoch darf der Erfolg dieser Operationstechnik nicht überbewertet werden, und weitere Langzeitverläufe müssen deren zumindest mittelfristig positiven Resultate bestätigen. Als mittelfristig sehen wir eine Verbesserung zumindest über 15 bis 20 Jahre an. Aktuell ist in 1 Falle nach 10 Jahren eine rapide Verschlechterung im Sinne einer schweren Arthrose aufgetreten, obwohl das Containment perfekt war. Hier konnte jedoch durch intertrochantäre Umstellung zumindest kurzfristig die Situation wiederum verbessert werden.
Der hier dargestellte Verlauf dokumentiert die Wichtigkeit, initial die Schwere der Femur-Kopfschädigung einerseits und der Zerstörung des Kopfknorpels richtig einzuschätzen. Ein solches Beispiel ist in Abb. 3 dargestellt. Obwohl MRT-mäßig hätte vermutet werden können, die Situation durch eine Kopfverkleinerung verbessern zu können, hatte sich intraoperativ gezeigt, dass dies in diesem Fall nicht zielführend gewesen wäre.
Klinische Fallbeispiele
Darstellung von 3 typischen Fallbeispielen entsprechend den verschiedenen Optionen:
nur Kopfreduktion,
Kopfreduktion und gleichzeitig Pfannenschwenkung,
Kopfreduktion und sekundäre Pfannenschwenkung.
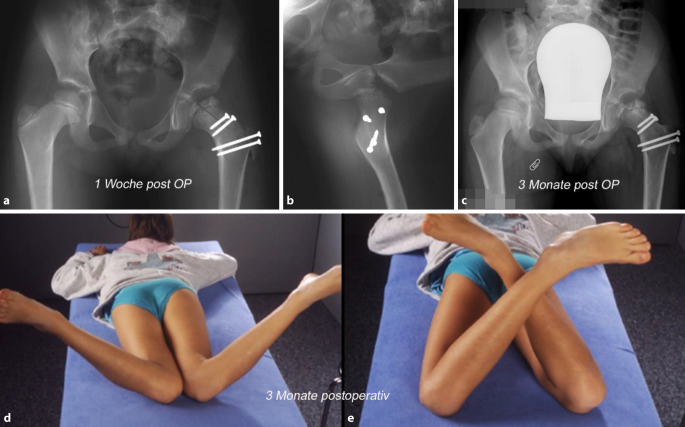
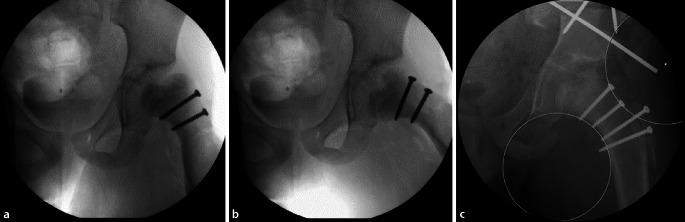
Fall 1: alleinige Kopfreduktion
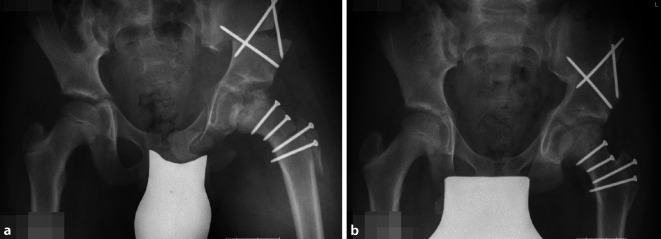
Fall 2. Kopfreduktion und gleichzeitige Triple-Osteotomie, Operation im Alter von 10 ½ Jahren
Abb. 24, 25, 26, 27, 28 und 29.
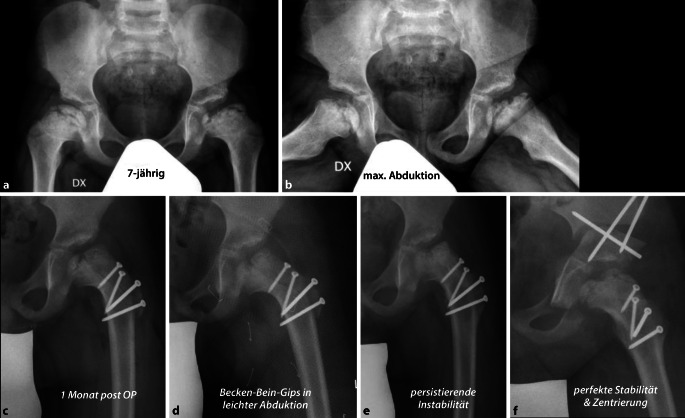
Fall 3: Hüftkopfreduktion und aufgeschobene Triple-Osteotomie
Funding
Open access funding provided by University of Bern.
Einhaltung ethischer Richtlinien
Interessenkonflikt
T. Slongo und K. Ziebarth geben an, dass kein Interessenkonflikt besteht.
Für diesen Beitrag wurden von den Autoren keine Studien an Menschen oder Tieren durchgeführt. Für die aufgeführten Publikationen gelten die jeweils dort angegebenen ethischen Richtlinien. Für Bildmaterial oder anderweitige Angaben innerhalb des Manuskripts, über die Patienten zu identifizieren sind, liegt von ihnen und/oder ihren gesetzlichen Vertretern eine schriftliche Einwilligung vor.
Footnotes
Manufaktur; Accuratus AG, Holligenstrasse 94, 3008 Bern, Switzerland. Referenzen: https://subtilis.ch/referenzen.html, mit freundl. Genehmigung von Accurates AG, Bern.

QR-Code scannen & Beitrag online lesen
Literatur
Verwendete Literatur
- 1.Herring JA, Neustadt JB, Williams JJ, et al. The lateral pillar classification of legg calve perthes disease. J Pediatr Orthop. 1992;12:143. doi: 10.1097/01241398-199203000-00001. [DOI] [PubMed] [Google Scholar]
- 2.Catterall A. The natural history of Perthes disease. J Bone Joint Surg Br. 1971;53:37. doi: 10.1302/0301-620X.53B1.37. [DOI] [PubMed] [Google Scholar]
- 3.Wenger D, Pandya NK. Advanced containment methods for the treatment of Perthes disease: salter plus varus osteotomy and triple pelvic osteotomy. J Pediatr Orthop. 2011;31:S198–S205. doi: 10.1097/BPO.0b013e31822602b0. [DOI] [PubMed] [Google Scholar]
- 4.Stulberg SD, Cooperman DR, Wallensten R. The natural history of Legg calve Perthes disease. J Bone Joint Surg Am. 1981;63:1095–1108. doi: 10.2106/00004623-198163070-00006. [DOI] [PubMed] [Google Scholar]
- 5.Ganz R, Gill T, Gautier E, et al. Surgical dislocation of the adult hip. A technique with full access to the femoral head and acetabulum without the risk of avascular necrosis. J Bone Joint Surg Br. 2001;83:1119–1124. doi: 10.1302/0301-620X.83B8.0831119. [DOI] [PubMed] [Google Scholar]
- 6.Eijer H, Podeszwa D, Ganz R, et al. Evaluation treatment of femoro acetabular impingement secondary to Perthes’ disease. Hip Int. 2006;16:273–280. doi: 10.1177/112070000601600406. [DOI] [PubMed] [Google Scholar]
- 7.Nötzli HP, Siebenrock KA, Hempfing A, et al. Perfusion of the femoral heads during surgical dislocation of the hip. Monitoring by laser Doppler flowmetry. J Bone Joint Surg Br. 2002;84:300–304. doi: 10.1302/0301-620X.84B2.0840300. [DOI] [PubMed] [Google Scholar]
- 8.Ganz R, Huff TW, Leunig M. Extended retinacular soft tissue flap for intra articular hip surgery: surgical technique, indications, and results of its application. Instr Course Lect. 2009;58:241–255. [PubMed] [Google Scholar]
- 9.Leunig M, Slongo T, Kleinschmidt M, et al. Subcapital correction osteotomy in slipped capital femoral epiphysis by means of surgical hip dislocation. Oper Orthop Traumatol. 2007;19:389–410. doi: 10.1007/s00064-007-1213-7. [DOI] [PubMed] [Google Scholar]
- 10.Ziebarth K, Zilkens C, Spencer S, et al. Capital realignment for moderate and severe SCFE using a modified Dunn procedure. Clin Orthop Relatres. 2009;467:704–716. doi: 10.1007/s11999-008-0687-4. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 11.Leunig M, Ganz R. Relative neck lengthening and intra-capital osteotomy for severe Perthes and Perthes-like deformities. Bull NYU Hosp Jt Dis. 2011;69:S62–S67. [PubMed] [Google Scholar]
- 12.Stulberg SD, Cooperman DR, Wallensten R. The natural coures of Legg-Perthes disease and its relationship to degenerative arthritis of the hip. A long term follow-up study. Orthop Trans. 1977;1:105–106. [Google Scholar]
- 13.Sevitt S, Thompson RG. The distribution and anastomosis of the arteries supplying the head and neck of the femur. J Bone Joint Surg Br. 1965;47:560–573. doi: 10.1302/0301-620X.47B3.560. [DOI] [PubMed] [Google Scholar]
- 14.Kalhor M, Beck M, Huff TW, et al. Capsular contribution to the acetabular perfusion. Anatomical considerations and surgical implications. J Bone Joint Surg Am. 2009;91:409–418. doi: 10.2106/JBJS.G.01679. [DOI] [PubMed] [Google Scholar]
- 15.Fürnstahl P, Ganz R, Ackermann J. Leading Opinions. 2018. A new treatment approach for severe Legg-Calvé-Perthes deformity based on computer simulation and surgical navigation. [Google Scholar]
- 16.Ziebarth K, Slongo T, Siebenrock KA. Residual Perthes deformity and surgical reduction of the size of the femoral head. Oper Tech Orthop. 2013;23:134–139. doi: 10.1053/j.oto.2013.08.001. [DOI] [Google Scholar]
- 17.Siebenrock K, Anwander H, Zurmühle C, Tannast M, Slongo TH, Seppacher S. Head reduction osteotomy with additional containment surgery improves sphericity and containment and reduces pain in Legg-Calvé-Perthes disease. Clin Orthop Relat Res. 2015;473(4):1274–1283. doi: 10.1007/s11999-014-4048-1. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 18.Ganz R, Horowitz K, Leunig M. Algorithm for femoral and peri-acetabular osteotomies in complex hip deformities. Clin Orthop Relat Res. 2010;468:3168–3180. doi: 10.1007/s11999-010-1489-z. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 19.Joseph B. Morphological changes in the acetabulum in Perthes’ disease. J Bone Joint Surg Br. 1989;71:756–763. doi: 10.1302/0301-620X.71B5.2584244. [DOI] [PubMed] [Google Scholar]
- 20.Kalhor M, Horowitz K, Gharehdaghi J, Beck M, Ganz R. Anatomic variations in femoral head circulation. Hip Int. 2012;22:307–312. doi: 10.5301/HIP.2012.9242. [DOI] [PubMed] [Google Scholar]
- 21.Paley D. The treatment of femoral head deformity and coxa magna by the Ganz femoral head reduction osteotomy. Orthop Clin North Am. 2011;42:389–399. doi: 10.1016/j.ocl.2011.04.006. [DOI] [PubMed] [Google Scholar]
- 22.Quain S, Catterall A. Hinge abduction of the hip. Diagnosis and treatment. J Bone Joint Surg Br. 1986;68:61–64. doi: 10.1302/0301-620X.68B1.3941142. [DOI] [PubMed] [Google Scholar]
- 23.https://subtilis.ch/referenzen.html
Weiterführende Literatur
- 24.Beck M, Leunig M, Parvizi J, et al. Anterior femoro acetabular impingement. Midterm results of surgical dislocation. Clin Orthop Relat Res. 2004;418:74–80. doi: 10.1097/00003086-200401000-00012. [DOI] [PubMed] [Google Scholar]
- 25.Tannast M, Hanke M, Ecker TM, et al. LCPD: Reduced range of motion resulting from extra- and intra articular impingement. Clin Orthop Relat Res. 2012;470:2431–2440. doi: 10.1007/s11999-012-2344-1. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 26.Tannast M, Macintyre N, Steppacher SD, et al. A systematic approach to analyze the sequelae of LCPD. Hip Int. 2013 doi: 10.5301/hipint.5000071. [DOI] [PubMed] [Google Scholar]