Prezado Editor,
Lemos com grande interesse o artigo “Ablação septal com cateteres e radiofrequência guiada pela ecocardiografia para tratamento de pacientes com cardiomiopatia hipertrófica obstrutiva (CHO): Experiência inicial”, publicado recentemente por Valdigem et al. 1 nos Arquivos Brasileiros de Cardiologia.
Nesse estudo, os autores avaliaram os efeitos da ablação endocárdica por radiofrequência (RF) do septo interventricular com redução do gradiente ventrículo-arterial e melhora de classe funcional em 12 pacientes com CHO. Cateteres com pontas sólidas de 8 mm de comprimento foram utilizados para aplicação de RF termo controlada. A intensidade de energia foi de 80 Watts com temperatura máxima de 60 0 C. A região de maior gradiente na via de saída do ventrículo esquerdo foi o alvo para ablação e identificada pelo ecocardiograma transesofágico. Os autores observaram uma redução média dos gradientes obtidos de 96,8±34 mmHg para 36,1±23 mmHg (p=0,0001) no seguimento de 1 ano, com melhora clínica em todos os pacientes da série. Concluíram que a ablação septal com RF é uma estratégia eficaz, segura e uma nova opção para tratamento de pacientes com CHO com gradiente elevados e sintomáticos. Parabenizamos os autores pelos bons resultados ao utilizar tecnologia de fácil acessibilidade e ao trazer novas informações sobre um procedimento ainda em desenvolvimento.
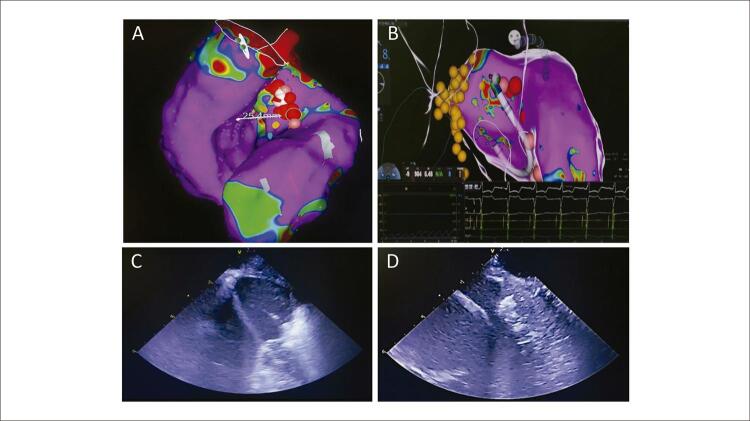
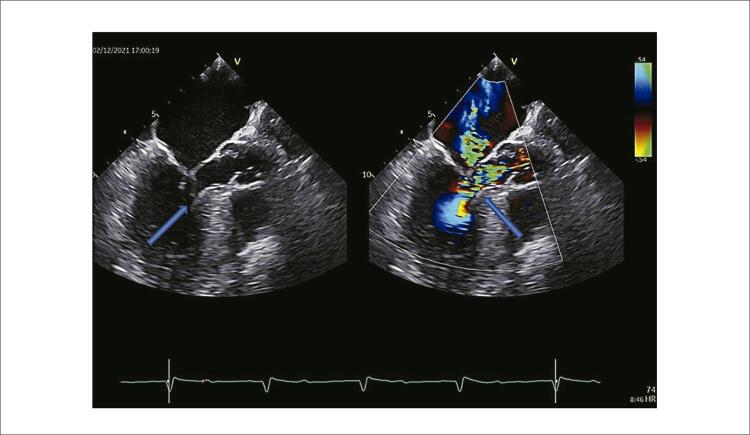
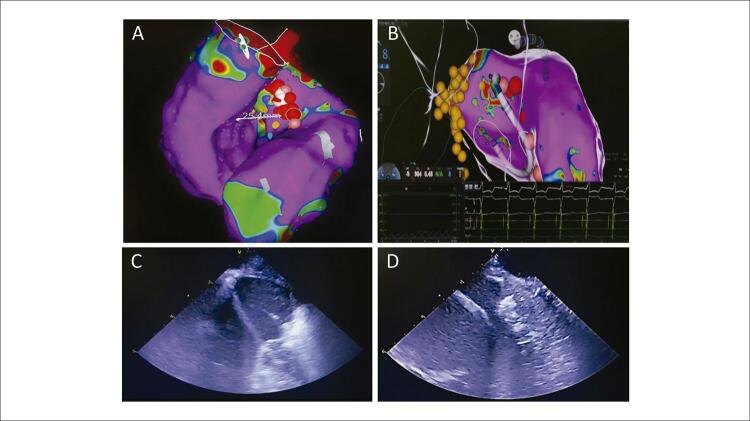
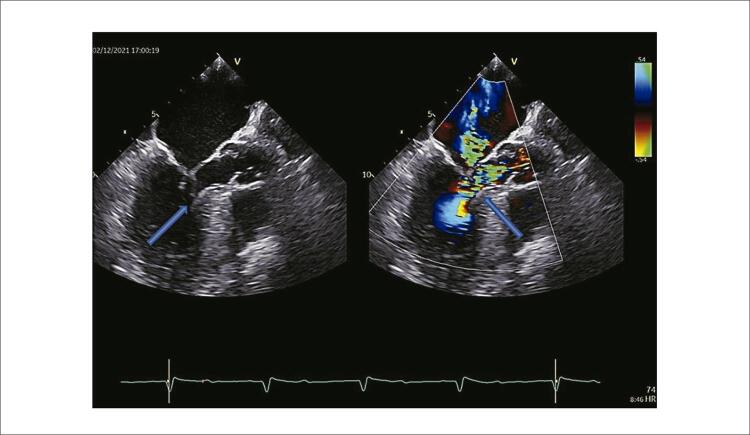
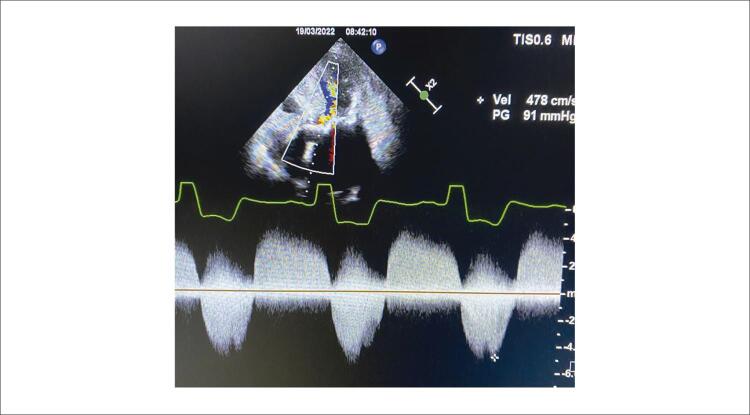
No período de agosto de 2020 a janeiro de 2021, realizamos ablação com RF do septo interventricular em dois pacientes (homem de 44 anos e mulher de 38 anos de idade) com CHO sintomática, refratários ao tratamento clínico, ambos com seguimento superior a 12 meses. Entretanto, diferentemente da técnica descrita por Valdigem et al., 1 utilizamos novas tecnologias de imagem, como mapeamento eletroanatômico (MEA) e o ecocardiograma intracardíaco ( Figura 1 ). O MEA permitiu delimitar a localização do sistema de condução intraventricular e conferiu maior segurança na aplicação de RF (evitar o bloqueio do ramo esquerdo ou atrioventricular total). A construção da geometria pelo MEA dos ventrículos esquerdo e direito também forneceu informação importante na delimitação da área a ser abordada. O ecocardiograma intracardíaco (ICE) permitiu acompanhar a produção das lesões de RF no septo interventricular e a evolução do edema próximo à via de saída do ventrículo esquerdo durante o procedimento, sem a necessidade de um ecocardiografista. Adicionalmente, a ablação com radiofrequência foi otimizada com a utilização de cateteres com ponta irrigada, e as lesões foram controladas pelo software VISITAG SURPOINT (J&J) 2 para uniformizar sua profundidade.
Figura 1. A) Mapa eletroanatômico Carto 3 do ventrículo direito e esquerdo. Pode-se observar o ponto de maior espessamento septal (25 mm). Os pontos em vermelho representam a região onde foi aplicada radiofrequência. B) Início da aplicação de radiofrequência. Os pontos amarelos representam as áreas a serem evitadas em que foi identificado sistema de condução. C) Hiperecogenicidade da região septal, avaliada continuamente com ecocardiografia intracardíaca durante a aplicação de radiofrequência. É possível identificar cateter em alça apoiado sobre a região septal. D) Ao término do procedimento, observado intenso edema na região septal, associado a hiperecogenicidade próximo a via de saída do ventrículo esquerdo.
O critério de interrupção do procedimento utilizado por Valdigem et al. 1 foi a queda aguda de 25% no gradiente ventrículo-arterial. No entanto, alguns autores sugerem que a ablação septal excessiva para atingir esses índices agudamente pode provocar aumento paradoxal e agudo do gradiente com risco de congestão pulmonar importante após a ablação. 3 Nossa impressão é que o uso de uma estratégia puramente anatômica, com aplicações septais logo acima do ramo esquerdo, tendo como alvo um Ablation Index entre 600 e 700, usando cateter irrigado de 3,5 mm (50 Watts e 43 0 C) e avaliação contínua do edema da via de saída do ventrículo esquerdo com o ICE, pode tornar o procedimento mais seguro.
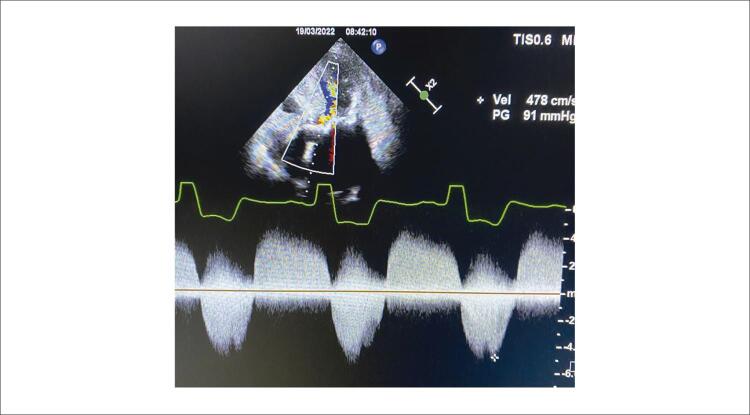
As diversas séries publicadas até o momento não valorizam o gradiente imediato sugerindo que o maior benefício na redução do gradiente ocorre entre 9 e 12 meses da ablação. 4 , 5 Nossos pacientes tiveram uma redução significativa do gradiente intraventricular, com redução média de 91±22 mmHg para 27±14 mmHg cerca de 12 meses após o procedimento índice, e redução no primeiro dia de pós-operatório de 22±6 mmHg, ambos com melhora significativa dos sintomas e atualmente em classe funcional II. A utilização de cateter irrigado, permite a realização de lesões mais previsíveis, mas pode contribuir com quadros de congestão pulmonar como descrito pelos autores. A utilização simultânea do ICE para acompanhar as aplicações de RF também pode evitar a ocorrência de “Stem Pops” , fato comum em aplicações prolongadas e com alta energia. Adicionalmente, o ecocardiograma intracardíaco auxilia na monitoração do risco de aplicações excessivas ao acompanhar a formação de edema septal. Apesar disso, um dos nossos pacientes apresentou quadro de congestão pulmonar imediatamente após a ablação, que foi resolvido com uso de diuréticos e ventilação não invasiva. Tanto a utilização de cateter irrigado como o edema importante na via de saída podem ter contribuído para o quadro apresentado pela paciente. Novos estudos são necessários a fim de comparar diferentes técnicas bem como padronizar qual seria a forma ideal de criar as lesões, que minimizem o risco de aumentos agudos de gradiente ventrículo-arterial após a ablação.
Referências
- 1.Valdigem BP, Correia EB, Moreira DAR, Bihan DL, Pinto IMF, Abizaid AAC, et al. Septal Ablation with Radiofrequency Catheters Guided by Echocardiography for Treatment of Patients with Obstructive Hypertrophic Cardiomyopathy: Initial Experience. 10.36660/abc.20200732.Arq Bras Cardiol. 2022;118(5):861–872. doi: 10.36660/abc.20200732. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 2.Okumura Y, Watanabe I, Iso K, Nagashima K, Sonoda K, Sasaki N, et al. Clinical Utility of Automated Ablation Lesion Tagging Based on Catheter Stability Information (VisiTag Module of the CARTO 3 System) with Contact Force-Time Integral During Pulmonary Vein Isolation for Atrial Fibrillation. 10.1007/s10840-016-0156-z.J Interv Card Electrophysiol. 2016;47(2):245–252. doi: 10.1007/s10840-016-0156-z. [DOI] [PubMed] [Google Scholar]
- 3.Lawrenz T, Lawin D, Radke K, Stellbrink C. Acute and Chronic Effects of Endocardial Radiofrequency Ablation of Septal Hypertrophy in HOCM. 10.1111/jce.15203.J Cardiovasc Electrophysiol. 2021;32(10):2617–2624. doi: 10.1111/jce.15203. [DOI] [PubMed] [Google Scholar]
- 4.Cooper RM, Shahzad A, Hasleton J, Digiovanni J, Hall MC, Todd DM, et al. Radiofrequency Ablation of the Interventricular Septum to Treat Outflow Tract Gradients in Hypertrophic Obstructive Cardiomyopathy: A Novel Use of CARTOSound® Technology to Guide Ablation. 10.1093/europace/euv302.Europace. 2016;18(1):113–120. doi: 10.1093/europace/euv302. [DOI] [PubMed] [Google Scholar]
- 5.Crossen K, Jones M, Erikson C. Radiofrequency Septal Reduction in Symptomatic Hypertrophic Obstructive Cardiomyopathy. 10.1016/j.hrthm.2016.04.018.Heart Rhythm. 2016;13(9):1885–1890. doi: 10.1016/j.hrthm.2016.04.018. [DOI] [PubMed] [Google Scholar]