Introdução
Os fenótipos da insuficiência cardíaca (IC) podem ser divididos em categorias de acordo com a fração de ejeção (FE) do ventrículo esquerdo – IC com FE preservada (ICFEp; FE ≥ 50%); IC com FE levemente reduzida (ICFElr; FE 41-49%) e IC com FE reduzida (ICFEr; FE≤40%). 1 No entanto, as diferenças entre os fenótipos da IC vão além da FE. Enquanto a ICFEp desenvolve-se a partir de uma interação de comorbidades que leva à doença cardíaca estrutural e sintomas da IC, a ICFEr geralmente desenvolve-se devido a um insulto cardíaco que reduz o débito cardíaco. 1 , 2 Além disso, embora múltiplas terapias possam melhorar o prognóstico da ICFEr, somente os inibidores do cotransportador de sódio-glicose-2 (SGLT2i) melhoraram os desfechos da ICFEp, demonstrado em um ensaio controlado randomizado (ECR). 3 Nesta carta científica, avaliamos evidências de terapias farmacológicas com potencial benefício na ICFEp.
Tratamento das etiologias da ICFEp e condições associadas
O manejo das etiologias da ICFEp e comorbidades (p.ex., hipertensão, diabetes, doença arterial coronariana, obesidade, anemia, doença renal crônica) é essencial para evitar a progressão da doença e reduzir hospitalização. 1 Pacientes com cardiomiopatia causada por amiloidose por transtirretina também se beneficiam de tafamidis, que reduziu em 30% e 32% o risco de mortalidade por todas as causas e internações por doenças cardiovasculares, respectivamente, em comparação a placebo. 4
Inibidores da enzima conversora de angiotensina (IECA), bloqueadores de receptor de angiotensina (BRAs), e inibidor da neprilisina e do receptor da angiotensina
ECRs anteriores, tais como o PEP-CHF, 5 o CHARM-Preserved 6 e o I-PRESERVE 7 não mostraram benefício significativo dos IECA ou BRAs em pacientes com ICFEp. Khan et al., 8 confirmaram esses achados, mas demonstraram, em uma análise agrupada dos ECRs, uma tendência de menor risco de hospitalização por IC. 8 Em seguida, sacubitril/valsartana surgiu como um medicamento promissor para melhorar desfechos na ICFEp, mas falhou em demonstrar benefício em seu desfecho primário de hospitalização por IC ou morte cardiovascular no ensaio PARAGON-HF. 9 No entanto, mulheres com ICFEp podem se beneficiar do sacubitril/valsartana, uma vez que o fármaco reduziu em 27% o desfecho primário em comparação ao placebo, em uma análise de subgrupo pré-especificada. 9 Evidências de uma meta-análise de ECRs mostrou que o sacubitril/valsartana levou à redução de níveis de NT-pro-BNP e melhora da qualidade de vida de pacientes com ICFEp. 10 Assim, pode-se preferir sacubitril/valsartana a BRAs ou IECA em pacientes com indicação para inibidores do sistema renina-angiotensina-aldosterona devido a comorbidades.
Antagonista dos receptores mineralocorticoides (ARMs)
No ensaio TOPCAT, a espironolactona não reduziu o desfecho primário de morte cardiovascular, parada cardíaca abortada ou hospitalização por IC em pacientes com ICFEp em comparação a placebo, embora tenha sido eficaz em pacientes como níveis elevados de peptídeos natriuréticos. 11 , 12 Enquanto pacientes nas Américas tiveram uma redução de 18% no risco do desfecho primário com a espironolactona, pacientes na Rússia e na Geórgia não tiveram melhora no prognóstico com a medicação. 11 Tal fato pode ser explicado por diferenças na randomização, pacientes que não tomaram a medicação, e taxas de eventos mais baixas na Rússia e na Geórgia. 11 , 13 Evidências de uma meta-análise mostraram que a espironolactona reduziu internações, melhorou a classe funcional da New York Heart Association (NYHA) e reduziu níveis do peptídeo natriurético tipo-B em pacientes com ICFEp. 14
Diuréticos
Devido a questões éticas em se realizar ECRs para o uso de diuréticos, seus efeitos sobre o prognóstico em longo prazo na ICFEp são desconhecidos. No entanto, uma análise pós-hoc do ensaio CHAMPION mostrou que ajustes na terapia com diuréticos e vasodilatadores de acordo com a pressão arterial pulmonar reduziu em 46% a razão de incidência de hospitalização por IC em pacientes com ICFEp classe III da NYHA. 15 Isso reforça a necessidade de se controlar edema pulmonar e periférico, e indica que diuréticos não só controlam sintomas como também reduzem internações por IC.
Inibidores do cotransportador de sódio-glicose-2 (SGLT2i)
Dados do ensaio EMPEROR-Preserved mostrou que a empagliflozina reduziu o risco de desfecho primário de morte cardiovascular ou hospitalização por IC em pacientes com ICEFp em comparação a placebo. 3 Em uma análise exploratória, a empagliflozina também reduziu internações por IC que requeriam cuidado intensivo, internações que requeriam droga vasopressora ou inotrópicos positivos, e a necessidade de se intensificar terapia com diuréticos em pacientes ambulatoriais. 16 Ainda, a probabilidade de melhora na classe funcional da NYHA foi maior nos pacientes que receberam empagliflozina. 16
Betabloqueadores e outras terapias
Em uma meta-análise de ECRs, os betabloqueadores não reduziram o risco de mortalidade por todas as causas ou morte cardiovascular em pacientes com ICFEp em ritmo sinusal ou com fibrilação atrial. 17 Tanto a digoxina como terapias cujo alvo era a via do óxido nítrico/monofosfato cíclico de guanosina não mostraram sucesso na melhora dos desfechos na ICFEp. 1 , 18 Detalhes de ECRs de fase III que investigaram tratamentos farmacológicos em pacientes com ICFEp estão descritos na Tabela 1 . Após rever as evidências aqui descritas, nós delineamos uma proposta de terapia tripla com o potencial de melhorar os desfechos de pacientes com ICFEp, ilustrada na Figura 1 .
Tabela 1. Ensaios controlados randomizados de fase III de terapias farmacológicas para insuficiência cardíaca com fração de ejeção preservada.
| Estudo | Droga | Critérios de inclusão | Mortalidade por todas as causas | Mortalidade cardiovascular | Mortalidade cardiovascular ou hospitalização por IC | Hospitalização por IC |
|---|---|---|---|---|---|---|
| PEP-CHF 5 | Perindopril | Índice de motilidade da parede do VE ≥ 1,4, IC sintomática tratada com diuréticos, disfunção diastólica, idade ≥ 70 anos | HR: 1,09 (0,75-1,58) | HR: 0,98 (0,63-1,53) | NR | HR: 0,86 (0,61-1,20) |
| CHARM-Preserved 6 | Candesartana | FEVE > 40%, NYHA II-IV, História de internação por doença cardiovascular | NR | HR: 0,99 (0,80-1,22) | HR: 0,89 (0,77-1,03) | HR: 0,85 (0,72-1,01) |
| I-PRESERVE 7 | Irbesartana | FEVE ≥ 45%, NYHA III-IV ou NYHA II com internação por IC nos últimos seis meses, idade ≥ 60 anos | HR: 1,00 (0,88-1,14) | HR: 1,01 (0,86-1,18) | HR: 0,96 (0,84-1,09) | HR: 0,95 (0,81-1,10) |
| PARAGON-HF 9 | Sacubitril-Valsartana | IC com FEVE ≥ 45%, NYHA II-IV, aumento do átrio esquerdo ou hipertrofia do VE e BNP ≥ 300 pg/mL ou NT-proBNP ≥ 900 pg/mL ou internação por IC nos últimos nove meses | HR: 0,97 (0,84-1,13) | HR: 0,95 (0,79-1,16) | RaR: 0,87 (0,75–1,01) | RaR: 0,85 (0,72-1,00) |
| TOPCAT 11 | Espironolactona | FEVE ≥ 45%, ≥ 1 sinal de IC e ≥ um sintoma de IC, internação por IC nos últimos nove meses, ou BNP ≥ 100 pg/mL, NT-proBNP ≥ 360 pg/mL, idade ≥ 50 anos | HR: 0,91 (0,77-1,08) | HR: 0,90 (0,73-1,12) | HR: 0,89 (0,77-1,04) | HR: 0,83 (0,69-0,99) |
| EMPEROR-Preserved 3 | Empagliflozina | IC com FEVE ≥ 40%, NYHA II-IV, idade ≥18 anos, NT-proBNP > 300 pg/mL ou NT-proBNP > 900 pg/mL para pacientes com IC e FA | HR: 1,00 (0,87-1,15) | HR: 0,91 (0,76-1,09) | HR: 0,79 (0,69-0,90) | HR: 0,73 (0,61-0,88) |
| DIG-PEF 18 | Digoxina | IC com FEVE > 45%, RS | RiR: 0,99 (0,76-1,28) | RiR: 1,00 (0,73-1,36) | RiR: 0,88 (0,70-1,11) | RiR: 0,79 (0,59-1,04) |
FA: fibrilação atrial; VE: ventrículo esquerdo; IC: insuficiência cardíaca; FEVE: fração de ejeção do ventrículo esquerdo; HR: hazard ratio; NT-proBNP: fragmento N-terminal do peptídeo natriurético tipo B; NYHA: New York Heart Association; RaR: rate ratio; RiR: risk ratio; RS: ritmo sinusal; NR: não reportado.
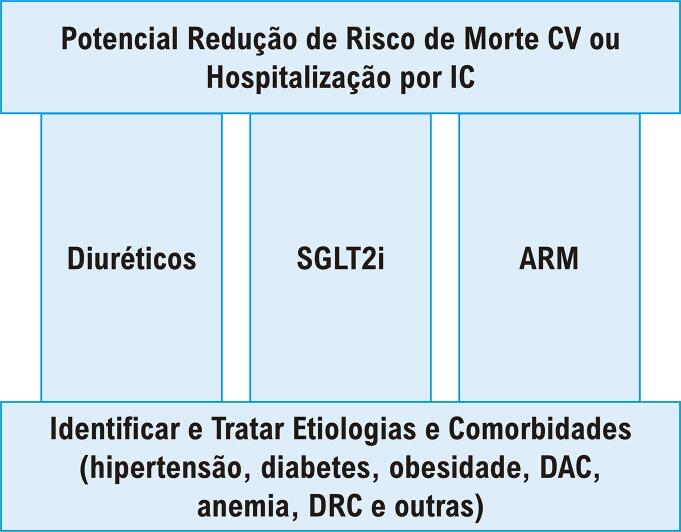
Figura 1. Proposta de terapia tripla para insuficiência cardíaca com fração de ejeção preservada. DAC: doença arterial coronariana; DRC: doença renal crônica; CV: cardiovascular; IC: insuficiência cardíaca; ARMs: antagonistas dos receptores mineralocorticoides; SGLT2i: inibidores do cotransportador de sódio-glicose-2; somente a empagliflozina tem evidências de um ensaio randomizado robusto. 3 Análises pós-hoc dos ensaios CHAMPION e TOPCAT podem corroborar o uso de diuréticos e ARMs. 11-13,15 .
Conclusões
Até o momento, a empagliflozina é a única terapia farmacológica com dados robustos de randomização que apoiem seus benefícios na ICFEp. Contudo, como discutido acima, uma combinação de diuréticos, ARMs e SGLT2i pode reduzir a mortalidade e a hospitalização em pacientes com ICFEp. Serão necessários outros ECRs investigando novas terapias para a ECFEp.
Vinculação acadêmica
Não há vinculação deste estudo a programas de pós-graduação.
Aprovação ética e consentimento informado
Este artigo não contém estudos com humanos ou animais realizados por nenhum dos autores.
Fontes de financiamento: O presente estudo não teve fontes de financiamento externas.
Referências
- 1.McDonagh TA, Metra M, Adamo M, Gardner RS, Baumbach A, Böhm M, et al. 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. Eur Heart J. 2021;42(36):3599–3726. doi: 10.1093/eurheartj/ehab368. [DOI] [PubMed] [Google Scholar]
- 2.Pfeffer MA, Shah AM, Borlaug BA. Heart Failure With Preserved Ejection Fraction In Perspective. 10.1161/CIRCRESAHA.119.313572Circ Res. 2019;124(11):1598–1617. doi: 10.1161/CIRCRESAHA.119.313572. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 3.Anker SD, Butler J, Filippatos G, Ferreira JP, Bocchi E, Böhm M, et al. Empagliflozin in Heart Failure with a Preserved Ejection Fraction. N Engl J Med. 2021;385(16):1451–1461. doi: 10.1056/NEJMoa2107038. [DOI] [PubMed] [Google Scholar]
- 4.Maurer MS, Schwartz JH, Gundapaneni B, Elliott PM, Merlini G, Waddington-Cruz M, et al. Tafamidis Treatment for Patients with Transthyretin Amyloid Cardiomyopathy. 10.1056/NEJMoa1805689N Engl J Med. 2018 Sep 13;379(11):1007–1016. doi: 10.1056/NEJMoa1805689. [DOI] [PubMed] [Google Scholar]
- 5.Cleland JGF, Tendera M, Adamus J, Freemantle N, Polonski L, Taylor J, et al. The perindopril in elderly people with chronic heart failure (PEP-CHF) study. 10.1093/eurheartj/ehl250Eur Heart J. 2006;27(19):2338–2345. doi: 10.1093/eurheartj/ehl250. [DOI] [PubMed] [Google Scholar]
- 6.Yusuf S, Pfeffer MA, Swedberg K, Granger CB, Held P, McMurray JJV, et al. Effects of candesartan in patients with chronic heart failure and preserved left-ventricular ejection fraction: the CHARM-Preserved Trial. 10.1016/S0140-6736(03)14285-7Lancet. 2003 Sep 6;362(9386):777–781. doi: 10.1016/S0140-6736(03)14285-7. [DOI] [PubMed] [Google Scholar]
- 7.Massie BM, Carson PE, McMurray JJ, Komajda M, McKelvie R, Zile MR, et al. Irbesartan in patients with heart failure and preserved ejection fraction. 10.1056/NEJMoa0805450N Engl J Med. 2008 Dec 4;359(23):2456–2467. doi: 10.1056/NEJMoa0805450. [DOI] [PubMed] [Google Scholar]
- 8.Khan MS, Fonarow GC, Khan H, Greene SJ, Anker SD, Gheorghiade M, et al. Renin-angiotensin blockade in heart failure with preserved ejection fraction: a systematic review and meta-analysis. 10.1002/ehf2.12204ESC Heart Fail. 2017 Nov;4(4):402–408. doi: 10.1002/ehf2.12204. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 9.Solomon SD, McMurray JJV, Anand IS, Ge J, Lam CSP, Maggioni AP, et al. Angiotensin-Neprilysin Inhibition in Heart Failure with Preserved Ejection Fraction. N Engl J Med. 2019 Oct 24;381(17):1609–1620. doi: 10.1056/NEJMoa1908655. [DOI] [PubMed] [Google Scholar]
- 10.Salah HM, Fudim M, Al’Aref SJ, Khan MS, Almarzooq ZI, Devabhaktuni SR, et al. Meta-Analysis of Efficacy of Sacubitril/Valsartan in Heart Failure With Preserved Ejection Fraction. 10.1016/j.amjcard.2021.01.013Am J Cardiol. 2021 Apr 15;145:165–168. doi: 10.1016/j.amjcard.2021.01.013. [DOI] [PubMed] [Google Scholar]
- 11.Pitt B, Pfeffer MA, Assmann SF, Boineau R, Anand IS, Claggett B, et al. Spironolactone for heart failure with preserved ejection fraction. 10.1056/NEJMoa1313731N Engl J Med. 2014 Apr 10;370(15):1383–1392. doi: 10.1056/NEJMoa1313731. [DOI] [PubMed] [Google Scholar]
- 12.Girerd N, Ferreira JP, Rossignol P, Zannad F. A tentative interpretation of the TOPCAT trial based on randomized evidence from the brain natriuretic peptide stratum analysis. 10.1002/ejhf.621Eur J Heart Fail. 2016 Dec;18(12):1411–1414. doi: 10.1002/ejhf.621. [DOI] [PubMed] [Google Scholar]
- 13.de Denus S, O’Meara E, Desai AS, Claggett B, Lewis EF, Leclair G, et al. Spironolactone Metabolites in TOPCAT - New Insights into Regional Variation. 10.1056/NEJMc1612601N Engl J Med. 2017 Apr 27;376(17):1690–1692. doi: 10.1056/NEJMc1612601. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 14.Xiang Y, Shi W, Li Z, Yang Y, Wang SY, Xiang R, et al. Efficacy and safety of spironolactone in the heart failure with mid-range ejection fraction and heart failure with preserved ejection fraction: A meta-analysis of randomized clinical trials. 10.1097/MD.0000000000014967Medicine. 2019 Mar;98(13):e14967. doi: 10.1097/MD.0000000000014967. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 15.Adamson PB, Abraham WT, Bourge RC, Costanzo MR, Hasan A, Yadav C, et al. Wireless pulmonary artery pressure monitoring guides management to reduce decompensation in heart failure with preserved ejection fraction. 10.1161/CIRCHEARTFAILURE.113.001229Circ Heart Fail. 2014 Nov;7(6):935–944. doi: 10.1161/CIRCHEARTFAILURE.113.001229. [DOI] [PubMed] [Google Scholar]
- 16.Packer M, Butler J, Zannad F, Filippatos G, Ferreira JP, Pocock SJ, et al. Effect of Empagliflozin on Worsening Heart Failure Events in Patients With Heart Failure and Preserved Ejection Fraction: EMPEROR-Preserved Trial. Circulation. 2021 Oct 19;144(16):1284–1294. doi: 10.1161/CIRCULATIONAHA.121.056824. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 17.Cleland JGF, Bunting KV, Flather MD, Altman DG, Holmes J, Coats AJS, et al. Beta-blockers for heart failure with reduced, mid-range, and preserved ejection fraction: an individual patient-level analysis of double-blind randomized trials. 10.1093/eurheartj/ehx564Eur Heart J. 2018 Jan 1;39(1):26–35. doi: 10.1093/eurheartj/ehx564. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 18.Ahmed A, Rich MW, Fleg JL, Zile MR, Young JB, Kitzman DW, et al. Effects of Digoxin on Morbidity and Mortality in Diastolic Heart Failure: The Ancillary Digitalis Investigation Group Trial. 10.1161/CIRCULATIONAHA.106.628347Circulation. 2006 Aug 1;114(5):397–403. doi: 10.1161/CIRCULATIONAHA.106.628347. [DOI] [PMC free article] [PubMed] [Google Scholar]