Malgré l’explosion de thérapies novatrices contre le cancer, la chimiothérapie demeure le pilier des traitements du cancer. Les médecins de famille apprennent peu sur la chimiothérapie durant leur formation, mais ils sont souvent appelés à prendre en charge les toxicités de ces traitements chez leurs patients1. Cet article d’ « Oncologie en bref » résume les éléments essentiels de la chimiothérapie à l’intention des médecins de famille.
Aperçu
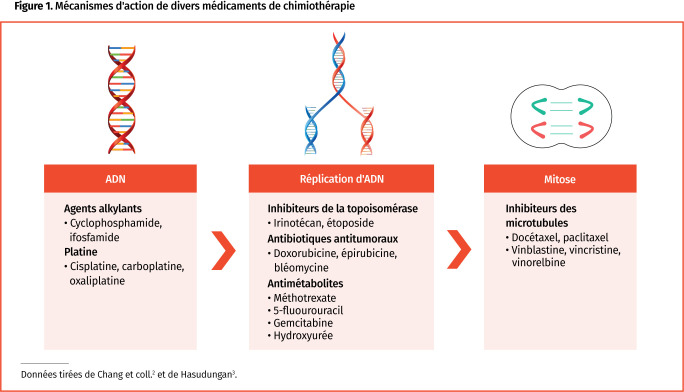
Tous les médicaments de chimiothérapie fonctionnent en réduisant la croissance et la prolifération des cellules. Les mécanismes d’action de ces médicaments varient, cependant, allant d’une inhibition concurrentielle des liaisons transversales des protéines de l’ADN au blocage des enzymes impliquées dans la réplication de l’ADN (p. ex. topoisomérase), en passant par l’entrave à la formation de fuseaux et de microtubules (Figure 1)2,3. Le manuel des médicaments contre le cancer de la Colombie-Britannique (en anglais) est une excellente source d’information sur les médicaments de chimiothérapie (http://www.bccancer.bc.ca/health-professionals/clinical-resources/cancer-drug-manual).
Figure 1.
Mécanismes d’action de divers médicaments de chimiothérapie
Intention de la chimiothérapie
Le mot adjuvant est utilisé couramment en oncologie et signifie un ajout au traitement définitif (p. ex. chirurgie, radiothérapie). Dans une perspective curative, un traitement néoadjuvant est utilisé pour baisser le stade (p. ex. réduire les cancers à un stade moins avancé et plus facilement traitable) ou rendre les cancers plus aisément opérables avant la thérapie définitive. Un traitement concurrent est administré pour améliorer la radiosensibilité durant la radiothérapie. Une thérapie adjuvante sert à éradiquer la maladie microscopique après le traitement définitif2.
La chimiothérapie palliative est un traitement non curatif qui vise à réduire le fardeau lié à la tumeur, et à améliorer la durée et la qualité de vie. La chimiothérapie palliative se distingue de la chimiothérapie curative en ce sens que le nombre de cycles n’est pas fixe4. L’efficacité d’une chimiothérapie palliative est évaluée à l’aide de la tomodensitométrie afin de restadifier périodiquement le cancer, de concert avec la surveillance de l’état clinique et des marqueurs biochimiques, le cas échéant. Un déclin inexpliqué dans l’état clinique devrait inciter à procéder à des investigations de restadification pour évaluer la progression. Les patients peuvent suivre la thérapie pendant des mois ou des années, et changer de régime lorsque la maladie progresse, puis arrêter lorsqu’ils se sentent trop mal ou ont décidé de ne plus suivre de traitement, ou encore, qu’il n’existe plus d’options thérapeutiques. La toxicité du traitement doit tenir compte des objectifs de la thérapie : par exemple, une plus grande toxicité avec une efficacité accrue peut être acceptable dans une perspective curative, mais inacceptable à des fins palliatives, lorsque la qualité de vie est d’une importance primordiale.
Considérations pratiques
L’efficacité de la chimiothérapie s’accroît proportionnellement à la dose; par ailleurs, étant donné que ces médicaments s’attaquent tous rapidement aux cellules qui se divisent, les doses sont limitées par la quantité de dommages causés aux tissus normaux, surtout les cellules hématologiques. En administrant la chimiothérapie par cycles, l’intensité de la dose peut être maintenue, en donnant à la moelle osseuse le temps de se rétablir entre les traitements. La durée des cycles varie habituellement entre 14 et 28 jours, et le nadir prévu dans les décomptes de neutrophiles se produit 7 à 14 jours après le traitement5. La combinaison de médicaments chimiothérapeutiques ayant différents mécanismes d’action a un effet synergique et peut permettre l’administration de doses plus faibles de médicaments, sans que les cellules cancéreuses développent une plus grande résistance (Tableau 1)6,7.
Tableau 1.
Régimes de chimiothérapie utilisés pour des cancers communs
| TYPE DE CANCER | MÉDICAMENTS DANS LE RÉGIME | ABRÉVIATION DU RÉGIME |
|---|---|---|
| Côlon |
|
FOLFOX |
| FOLFIRI | ||
| Sein |
|
FEC-D |
| FAC | ||
| AC/T | ||
| Cellules germinales |
|
BEP |
| Pancréas |
|
FOLFIRINOX |
| Lymphome non hodgkinien |
|
CHOP |
Bien que de nombreuses chimiothérapies soient administrées par perfusion de bolus intraveineux, le 5-fluorouracile (5-FU) peut aussi être administré par perfusion continue sur 48 heures. Divers agents chimiothérapeutiques, comme la capécitabine (qui est métabolisée en 5-FU) et l’étoposide, sont pris par voie orale7. Il y a lieu d’envisager d’utiliser un accès veineux central, comme un port ou un cathéter central inséré en périphérie, si la chimiothérapie est un vésicant (p. ex. doxorubicine, épirubicine, vinorelbine et vincristine)8.
Les résultats de l’analyse sanguine sont vérifiés avant chaque cycle de chimiothérapie, et on peut procéder au traitement si la numération globulaire est appropriée. Si les patients tolèrent mal le traitement ou si leur numération globulaire ne revient pas à la normale avant le prochain cycle de traitement, on peut envisager de réduire les doses ou de retarder le cycle, selon l’urgence de traiter avec des doses optimales. Dans une perspective curative, lorsqu’il est essentiel de maintenir l’intensité des doses et de respecter le calendrier, on peut administrer un facteur stimulant les colonies de granulocytes après chaque cycle pour stimuler la moelle osseuse afin d’augmenter la production de neutrophiles et de prévenir une neutropénie fébrile9. Les patients doivent avoir un état de rendement suffisant pour tolérer la chimiothérapie, ce qui signifie, en pratique, qu’ils sont assez bien pour ne pas être alités au moins 50 % du temps ou qu’ils sont au grade 2 de l’ECOG (Eastern Cooperative Oncology Group) (Tableau 2)10.
Tableau 2.
Échelle de performance ECOG
| GRADE | ÉTAT DU RENDEMENT SELON L’ECOG |
|---|---|
| 0 | Pleinement actif, capable d’effectuer sans restriction les mêmes activités qu’avant la maladie |
| 1 | Restreint dans les activités physiques vigoureuses, mais ambulatoire et capable d’accomplir du travail de nature plutôt sédentaire, comme des travaux ménagers légers, du travail de bureau |
| 2 | Ambulatoire et capable de ses soins personnels, mais incapable d’effectuer des activités liées au travail; debout et animé plus de 50 % du temps d’éveil |
| 3 | Capable seulement de soins personnels limités; confiné au lit ou au fauteuil plus de 50 % du temps d’éveil |
| 4 | Incapacité complète; n’effectue aucun de ses soins personnels; totalement confiné au lit ou au fauteuil |
| 5 | Mort |
ECOG—Eastern Cooperative Oncology Group.
Reproduit avec la permission d’Oken et coll.10.
Les soignants et les patients doivent traiter les liquides corporels comme étant cytotoxiques, et porter des gants s’ils manipulent des vomissements, des selles ou de l’urine durant les 48 premières heures suivant le traitement. Durant cette période, les patients devraient s’asseoir pour uriner et fermer le couvercle de la toilette avant de tirer la chasse d’eau pour éviter des éclaboussures de liquides corporels11. Il faut toujours utiliser des contraceptifs. Comme on ne sait trop si les médicaments chimiothérapeutiques peuvent passer dans le sperme, les sécrétions buccales ou vaginales durant des activités sexuelles, il est conseillé d’utiliser des méthodes de protection jusqu’à 7 jours après le dernier traitement de chimiothérapie12.
Prise en charge des toxicités aiguës
Une myélosuppression se produit avec la plupart des médicaments chimiothérapeutiques, et elle se manifeste cliniquement sous forme de fatigue, de dyspnée, de saignements et d’infections. D’autres toxicités aiguës sont spécifiques au médicament en cause (Tableau 3, Figure 2)2,13. Les toxicités des chimiothérapies sont classées sur une échelle de 1 (légère) à 5 (liée au décès)14. Les patients qui doivent être hospitalisés ont généralement des réactions de grade 3 ou 4.
Tableau 3.
Toxicités aiguës courantes de la chimiothérapie selon le médicament
| TOXICITÉ | MÉDICAMENTS COURAMMENT À L’ORIGINE |
|---|---|
| Alopécie | Doxorubicine, épirubicine, ifosfamide, cyclophosphamide, cisplatine |
| Nausée ou vomissements | Cisplatine, carboplatine, cyclophosphamide, doxorubicine, épirubicine |
| Diarrhée | 5-FU ou capécitabine, irinotécan |
| Mucosite | 5-FU ou capécitabine |
| Syndrome main-pied | 5-FU |
| Vasospasme coronarien | 5-FU |
| Neuropathie périphérique | Oxaliplatine, vincristine, paclitaxel |
| Néphrotoxicité | Cisplatine |
| Ototoxicité | Cisplatine |
| Cystite hémorragique | Ifosfamide, cyclophosphamide |
| Fibrose pulmonaire | Bléomycine |
5-FU—5-fluorouracil.
Données tirées de Chang et coll.2.
Figure 2.
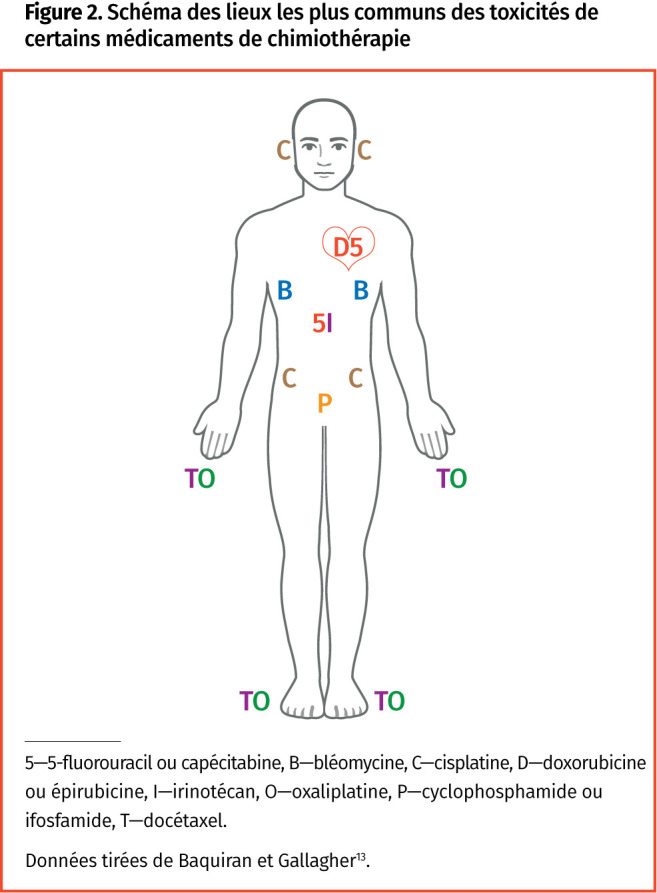
Schéma des lieux les plus communs des toxicités de certains médicaments de chimiothérapie
Les agents utilisés en chimiothérapie sont catégorisés comme ayant un potentiel émétisant d’élevé à faible, et il est démontré qu’ils causent de la nausée d’anticipation, aiguë ou à retardement (jour 2 à 5 après le traitement)15. Des antiémétiques ciblent les récepteurs neurotransmetteurs impliqués dans la provocation des vomissements. Un régime antiémétique efficace en prophylaxie combinant 4 médicaments est recommandé chez les patients qui reçoivent des médicaments fortement émétisants : un antagoniste des récepteurs des neurokinines-1 (p. ex. aprépitant), un antagoniste des récepteurs 5-HT3 (p. ex. ondansétron), un antagoniste de la dopamine (p. ex. olanzapine) et de la dexaméthasone16,17. Une hydratation par intraveineuse est un adjuvant utile pour les patients souffrant de nausée immédiate. La nausée à retardement peut être soulagée en prolongeant la durée de la dexaméthasone, et les anxiolytiques sont efficaces pour la nausée anticipée. Les professionnels doivent savoir que les antagonistes des récepteurs 5-HT3 causeront beaucoup de constipation.
Une neuropathie périphérique induite par la chimiothérapie (NPIC) se produit avec l’oxaliplatine, le docétaxel et le paclitaxel, qui sont des traitements courants pour le cancer du côlon et du sein18. La neuropathie périphérique induite par la chimiothérapie se manifeste sous la forme de symptômes sensoriels mains-pieds, et cause une déficience dans les tâches motrices fines et la stabilité de la démarche. Il importe de reconnaître rapidement une NPIC et d’ajuster la dose de la chimiothérapie, parce qu’une fois présente, cette neuropathie n’est que partiellement réversible. Le seul traitement dont les bienfaits sont étayés par des données probantes pour la NPIC est la duloxétine, bien qu’on puisse essayer les gabapentinoïdes et les antidépresseurs tricycliques19,20.
La capécitabine ou les 5-FU peuvent causer une inflammation et une ulcération dans tout le tractus gastro-intestinal. Dans la bouche, cette réaction se présente sous forme de mucosite, qui cause de la douleur et une réduction de l’apport alimentaire pouvant entraîner une déshydratation et un risque accru de batériémie21. L’entérite, ou l’inflammation du petit intestin, cause une diarrhée aqueuse, d’où un appauvrissement en liquides et en électrolytes. L’irinotécan cause aussi de la diarrhée en raison de dommages directs aux muqueuses. Lorsque d’autres causes, comme une infection, des laxatifs ou une obstruction intestinale partielle, ont été exclues, des thérapies pour les symptômes peuvent être utilisées. La prise en charge de la mucosite et de la diarrhée, fondée sur les lignes directrices d’organisations spécialisées en cancer, est présentée au Tableau 421-25.
Tableau 4.
Prise en charge de la mucosite et de la diarrhée liées à la chimiothérapie
| PRISE EN CHARGE NON PHARMACOLOGIQUE | PRISE EN CHARGE PHARMACOLOGIQUE |
|---|---|
| Mucosite | |
| Optimiser l’hygiène buccale de routine (brossage régulier, soie dentaire, nettoyage et ajustement de prothèses dentaires) | Surveiller la candidose, la xérostomie et le VHS dans la bouche. Traiter au besoin. |
| Éviter les aliments susceptibles d’irriter les muqueuses (durs, acides, épicés) | Agents de protection des muqueuses
|
| Utiliser des rince-bouche non médicamentés (solution au club soda ou au bicarbonate de soude dilué [1 c. à table de bicarbonate de soude dans 2 tasses d’eau]) | Agents lubrifiants solubles dans l’eau
|
| Utiliser du dentifrice à forte teneur en fluor (5000 ppm) | Anesthésiques topiques
|
| Changer pour un brossage à l’éponge si les brosses à dents causent de la douleur | Rince-bouche magique*
|
| Dans le cas d’une chimiothérapie par bolus de 5-FU, envisager une cryothérapie, soit des cubes de glace ou de l’eau froide dans la bouche durant l’administration de la chimiothérapie (en prévention) | Utiliser des analgésiques systémiques au besoin (par voie orale ou sous-cutanée) |
| Se procurer des suppléments alimentaires au besoin | |
| Diarrhée | |
| Utiliser des probiotiques (en prévention) | Envisager une investigation de causes infectieuses et s’assurer de l’absence d’une récente immunothérapie |
| Hydratation orale | Hydratation par voie intraveineuse |
| Des modifications alimentaires peuvent être nécessaires : utiliser un régime BRCT. Éviter les suppléments à forte osmolarité, les édulcorants et l’alcool | Administrer 2 mg de lopéramide par voie orale après chaque selle molle. Ne pas dépasser 16 mg en 24 h |
| Éviter le lactose (la chimiothérapie peut causer une carence temporaire en lactase) | En l’absence d’un contrôle adéquat, ajouter 2 comprimés de chlorhydrate de diphénoxylate–sulfate d’atropine par voie orale aux 6 h. S’il n’y a toujours pas de contrôle, ajouter de 50 à 600 μg/j d’ocréotide par voie sous-cutanée (administrée 2 ou 3 fois/j) |
5-FU—5-fluorouracil; BRCT—bananes, riz, compote de pommes, toast; VHS—virus de l’herpès simplex.
*Les données probantes de niveau 1 en faveur de l’utilisation de rince-bouche avec de multiples médicaments sont limitées en raison de l’hétérogénéité des solutions.
Conclusion
Ce bref aperçu de la chimiothérapie fournit aux médecins de famille des outils pour mieux comprendre les traitements contre le cancer de leurs patients et y participer. La compréhension des considérations pratiques de l’administration de la chimiothérapie et de la prise en charge des toxicités courantes qu’elle provoque permettra aux médecins de soins primaires de mieux soutenir leurs patients et de traiter efficacement les possibles effets secondaires des traitements contre le cancer.
Footnotes
Intérêts concurrents
Aucun déclaré
Cet article donne droit à des crédits d’autoapprentissage certifiés Mainpro+. Pour obtenir des crédits, allez à www.cfp.ca et cliquez sur le lien vers Mainpro+.
The English version of this article is available at www.cfp.ca on the table of contents for the January 2022 issue on page 30.
Références
- 1.Yip SM, Meyers DE, Sisler J, Wycliffe-Jones K, Kucharski E, Elser Cet al. Oncology education for family medicine residents: a national needs assessment survey. BMC Med Educ 2020;20(1):283. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 2.Chang AE, Ganz PA, Hayes DF, Kinsella T, Pass HI, Schiller JHet al., rédacteurs. Oncology: an evidence-based approach. New York, NY: Springer; 2006. [Google Scholar]
- 3.Hasudungan A. Oncology. Sydney, Aust: Armando Hasudungan Biology and Medicine Videos; 2021. Accessible à : https://armandoh.org/subjects/oncology/. Réf. du 24 nov. 2021. [Google Scholar]
- 4.Roeland EJ, LeBlanc TW.. Palliative chemotherapy: oxymoron or misunderstanding? BMC Palliat Care 2016;15:33. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 5.Hematology and associated laboratory tests. Dans : Clinical pharmacy guide: cancer drug treatment assessment and review 5th edition. Vancouver, CB: BC Cancer; 2020. Accessible à : http://www.bccancer.bc.ca/pharmacy-site/Documents/Clinical%20Pharmacy%20Guide/cpg3b-hematology-lab-tests.pdf. Réf. du 24 nov. 2021. [Google Scholar]
- 6.Kerr DJ, Haller DG, van de Velde CJ, Baumann M, rédacteurs. Oxford textbook of oncology. 3e éd. Oxford, RU: Oxford University Press; 2016. [Google Scholar]
- 7.Eguzo K, Jacobs C, Umezurike C, Eseigbe E, Ginsburg O, Hawley P.. Where there is no oncologist: manual of practical oncology in resource-limited settings. 2e éd. Nlagu, Nigeria: Marjorie Bash Foundation; 2017. Accessible à : https://www.researchgate.net/publication/318885762_Where_There_is_no_Oncologist_Manual_of_Practical_Oncology_in_Resource-Limited_Settings. Réf. du 24 nov. 2021. [Google Scholar]
- 8.BC Cancer extravasation hazard table. Vancouver, CB: BC Cancer; 2021. Accessible à : http://www.bccancer.bc.ca/drug-database-site/Documents/Extravasation%20Hazard%20Table.pdf. Réf. du 24 nov. 2021. [Google Scholar]
- 9.Aapro M, Boccia R, Leonard R, Camps C, Campone M, Choquet Set al. Refining the role of pegfilgrastim (a long-acting G-CSF) for prevention of chemotherapy-induced febrile neutropenia: consensus guidance recommendations. Support Care Cancer 2017;25(11):3295-304. Publ. en ligne du 25 août 2017. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 10.Oken MM, Creech RH, Tormey DC, Horton J, Davis TE, McFadden ETet al. Toxicity and response criteria of the Eastern Cooperative Oncology Group. Am J Clin Oncol 1982;5(6):649-55. [PubMed] [Google Scholar]
- 11.How to safely handle cancer medications and body fluids at home. Toronto, ON: Action Cancer Ontario. Accessible à : https://www.cancercareontario.ca/sites/ccocancercare/files/assets/HomeSafety.pdf. Réf. du 24 nov. 2021. [Google Scholar]
- 12.Intimacy and sex: for people with cancer and their partners. Toronto, ON: Cancer Care Ontario. Accessible à : https://www.cancercareontario.ca/sites/ccocancercare/files/IntimacyandSex.pdf. Réf. du 24 nov. 2021. [Google Scholar]
- 13.Baquiran DC, Gallagher J.. Lippincott’s cancer chemotherapy handbook. 2e éd. Alphen aan den Rijn, Pays-Bas: Wolters Kluwer; 2001. [Google Scholar]
- 14.Common terminology criteria for adverse events (CTCAE). Bethesda, MD: National Institutes of Health; 2020. Accessible à : https://ctep.cancer.gov/protocoldevelopment/electronic_applications/ctc.htm. Réf. du 24 nov. 2021. [Google Scholar]
- 15.Navari RM, Aapro M.. Antiemetic prophylaxis for chemotherapy-induced nausea and vomiting. N Engl J Med 2016;374(14):1356-67. [DOI] [PubMed] [Google Scholar]
- 16.2019 antiemetic recommendations for chemotherapy-induced nausea and vomiting: a clinical practice guideline. Toronto, ON: Action Cancer Ontario; 2019. Accessible à : https://www.cancercareontario.ca/sites/ccocancercare/files/guidelines/full/2019AntiemeticRecommendationsChemotherapyInducedNauseaVomiting.pdf. Réf. du 24 nov. 2021. [Google Scholar]
- 17.Antiemetic guidelines. Vancouver, CB: BC Cancer; 2017. Accessible à : http://www.bccancer.bc.ca/chemotherapy-protocols-site/Documents/Supportive%20Care/SCNAUSEA%20Appendix%20-%20Antiemetic%20Guidelines.pdf. Réf. du 24 nov. 2021. [Google Scholar]
- 18.Tofthagen C, McAllister RD, Visovsky C.. Peripheral neuropathy caused by paclitaxel and docetaxel: an evaluation and comparison of symptoms. J Adv Pract Oncol 2013;4(4):204-15. [PMC free article] [PubMed] [Google Scholar]
- 19.Chemotherapy induced peripheral neuropathy. Clinical practice guideline SUPP-010—version 1. Edmonton, AB: Alberta Health Services; 2019. Accessible à : https://www.albertahealthservices.ca/assets/info/hp/cancer/if-hp-cancer-guide-supp010-peripheral-neuropathy.pdf. Réf. du 24 nov. 2021. [Google Scholar]
- 20.Hershman DL, Lacchetti C, Dworkin RH, Lavoie Smith EM, Bleeker J, Cavaletti Get al. Prevention and management of chemotherapy-induced peripheral neuropathy in survivors of adult cancers: American Society of Clinical Oncology clinical practice guideline. J Clin Oncol 2014;32(18):1941-67. Publ. en ligne du du 14 avr. 2014. [DOI] [PubMed] [Google Scholar]
- 21.Elad S, Cheng KKF, Lalla RV, Yarom N, Hong C, Logan RMet al. MASCC/ISOO clinical practice guidelines for the management of mucositis secondary to cancer therapy. Cancer 2020;126(19):4423-31. Publ. en ligne du 28 juill. 2018. Erratum dans: Cancer 2021;127(19):3700.32786044 [Google Scholar]
- 22.Oral care management tips for healthcare professionals: mucositis, candidiasis, xerostomia. Edmonton, AB: Alberta Health Services; 2019. Accessible à : https://www.albertahealthservices.ca/assets/info/hp/cancer/if-hp-cancer-guide-symptom-summary-oral-care.pdf. Réf. du 24 nov. 2021. [Google Scholar]
- 23.Oral care (mouth care). Toronto, ON: Action Cancer Ontario. Accessible à : https://www.cancercareontario.ca/en/symptom-management/3156. Réf. du 24 nov. 2021. [Google Scholar]
- 24.Diarrhea. Toronto, ON: Action Cancer Ontario. Accessible à : https://www.cancercareontario.ca/en/symptom-management/3151. Réf. du 24 nov. 2021. [Google Scholar]
- 25.Symptom management guidelines: diarrhea. Vancouver, CB: BC Cancer; 2018. Accessible à : http://www.bccancer.bc.ca/nursing-site/Documents/4.%20Diarrhea.pdf. Réf. du 24 nov. 2021. [Google Scholar]