Abstract
Die perkutane hepatische Perfusion mit dem Chemotherapeutikum Melphalan (PHMP) ist eine Letztlinientherapie bei Patienten mit inoperablen primären oder sekundären Lebertumoren. Dabei wird die Leber transarteriell mit Melphalan perfundiert und aufgesättigt (Chemosaturation), mit dem Ziel, die Lebertumoren selektiv und ohne dessen systemische zytotoxische Eigenschaften zu behandeln. Über einen Extrakorporalkreislauf und eine Ballonokklusion der V. cava inferior wird das venöse hepatische Blut hämofiltriert und venös zurückgeleitet. Verfahrensbedingt kommt es dabei zu einer ausgeprägten Kreislaufdepression und einer Störung der plasmatischen Gerinnung. In diesem Artikel wird das anästhesiologische und postinterventionelle Management bei Patienten mit PHMP beschrieben und auf Fallstricke und Besonderheiten hingewiesen.
Schlüsselwörter: Lebertumoren, Melphalan, Angiographie, Chemosaturation, Extrakorporalkreislauf
Abstract
Percutaneous hepatic melphalan perfusion (PHMP) is a last-line treatment of inoperable primary or secondary liver tumors. Selective perfusion and saturation (chemosaturation) of the liver with the chemotherapeutic agent melphalan is performed via catheterization of the hepatic artery without affecting the rest of the body with its cytotoxic properties. Using an extracorporeal circulation and balloon occlusion of the inferior vena cava, the venous hepatic blood is filtered and returned using a bypass procedure. During the procedure, considerable circulatory depression and coagulopathy are frequent. The purpose of this article is to review the anesthesiological and postprocedural management of patients undergoing PHMP with consideration of the pitfalls and special circumstances.
Keywords: Liver tumors, Melphalan, Angiography, Chemosaturation, Extracorporeal circulation
Einleitung
Inoperable primäre oder sekundäre Lebertumoren sind Tumorerkrankungen mit insgesamt ungünstiger Prognose [28, 39, 44]. Das Aderhautmelanom weist dabei ein besonders aggressives hepatisches Metastasierungsverhalten auf [3, 54]. Obwohl die Einführung der Antikörpertherapie vielversprechende Ergebnisse insbesondere bei der Behandlung von metastasierenden kutanen Melanomen zeigt, können diese bei metastasierten Aderhautmelanomen nicht bestätigt werden [53]. Eine systemische Chemotherapie ist für hepatisch metastasierte Aderhautmelanome nicht etabliert.
Die selektive perkutane hepatische Perfusion mit dem Chemotherapeutikum Melphalan (Chemosaturation) ist ein Ansatz zur Tumorlastreduktion bzw. Tumorkontrolle, der insbesondere beim hepatisch metastasierten Aderhautmelanom mit einer guten Ansprechrate einhergeht [3, 7, 9, 14–16, 22, 23, 32, 35, 37, 39, 49]. Auch bei anderen Tumorentitäten, z. B. bei inoperablen hepatischen Metastasen von kutanen Melanomen, des kolorektalen Karzinoms, von neuroendokrinen Tumoren und bei Patienten mit hepatozellulärem Karzinom (HCC) oder intrahepatischem Cholangiokarzinom (ICC), kann häufig eine relevante Reduktion der Tumormasse erreicht werden [11, 14, 25, 30, 40, 46, 48, 50].
Bereits in den 1960er-Jahren wurden mit Untersuchungen zur Gefäßversorgung von Lebertumoren die Grundlage der selektiven Leberperfusion gelegt [8]. Dabei konnte erstmals gezeigt werden, dass die meisten primären und sekundären Lebertumoren hauptsächlich durch die hepatischen Arterien und deren Äste perfundiert werden, während gesunde Hepatozyten zu ca. 70 % durch die Pfortader versorgt werden [12, 45]. Diese Erkenntnis führte im weiteren Verlauf zu Therapiekonzepten von bis dato inoperablen Lebertumoren durch eine selektive isolierte hepatische Perfusion (IHP) mit hochdosierten Chemotherapeutika. Hierbei wurde offen chirurgisch eine komplexe Isolierung des Leberkreislaufs vom Körperkreislauf vorgenommen und anschließend das Chemotherapeutikum über eine Herz-Lungen-Maschine zugeführt [6]. Aufgrund des Komplikationspotenzials dieses Verfahrens [17] folgten in den 1990er-Jahren erste Schritte zu einer minimal-invasiven perkutanen hepatischen Melphalanperfusion (PHMP) [5]. Im Vergleich zur IHP zeigte die PHMP deutlich geringere Komplikationsraten und eine geringere 30-Tage-Sterblichkeit [7].
Es konnte mittlerweile in zahlreichen Studien gezeigt werden, dass die PHMP eine Behandlungsoption bei Patienten mit inoperablen, isolierten Lebermetastasen oder primären Lebertumoren darstellt [3, 9, 11, 14–17, 19, 22, 25, 29, 30, 33, 37, 38]. Allerdings ist die Auswahl geeigneter Patienten für eine PHMP entscheidend, um einen möglichst sicheren peri- und postoperativen Verlauf zu gewährleisten. Unerwünschte Wirkungen sind in diesem speziellen Setting durch die Interventionsschritte und die Toxizität des verwendeten Melphalans relativ häufig. Dabei spielen hauptsächlich vorübergehende Hypotension, Tachykardie und Koagulopathie eine Rolle; deren Management soll mit diesem Artikel etwas näher beleuchtet werden.
Verfahren/Methode
Derzeit steht mit dem Hepatic CHEMOSAT® Delivery System (Fa. Delcath Systems Inc., New York, NY, USA) ein minimal-invasives Verfahren zur Behandlung von Lebertumoren zur Verfügung. Seit 2011 besteht in der Europäischen Union eine CE-Zulassung [11].
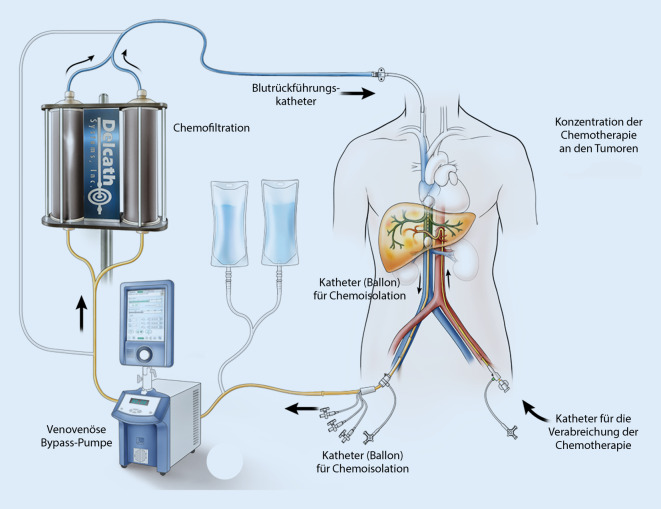
Dabei wird hochdosiertes Melphalan (3 mg/kg ideales Körpergewicht) durch ein interventionell eingebrachtes Kathetersystem direkt in die hepatischen Arterien injiziert. Dieses System wird über eine zuvor platzierte Schleuse in einer A. femoralis communis eingebracht. Dadurch werden die Tumorzellen in der Leber mit dem Chemotherapeutikum aufgesättigt. Um die systemische toxische Wirkung des Melphalans zu verhindern, wird über eine zweite Schleuse in der V. femoralis ein fenestrierter Doppelballonkatheter in der V. cava inferior positioniert (Abb. 1).
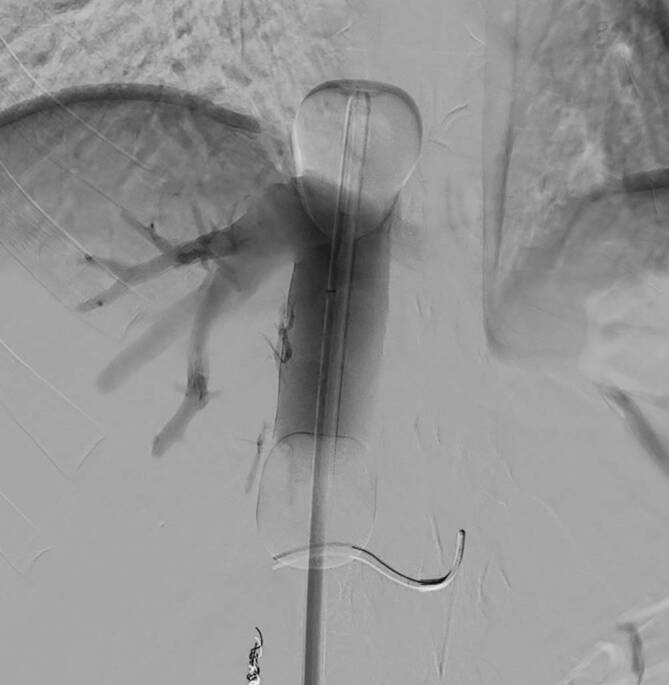
Auf diese Weise von der systemischen Zirkulation isoliert, kann das mit Melphalan aufgesättigte abfließende venöse Blut abgeleitet werden. Mittels einer extrakorporalen Zentrifugalpumpe wird das abfließende Blut durch spezielle Filter geführt und das Chemotherapeutikum zu ca. 95 % filtriert. Über eine weitere Schleuse in der rechten V. jugularis interna wird das gereinigte Blut in den Körperkreislauf zurückgeführt (Abb. 2). Der Einsatz dieses Pumpen‑/Filtersystems macht eine Vollheparinisierung des Patienten mit 300–400 IE Heparin/kgKG erforderlich, welche mittels Activated Clotting Time (ACT) gesteuert wird (Ziel: > 400 s). Die Steuerung und Überwachung der Extrakorporalpumpe werden durch einen Kardiotechniker durchgeführt. Die Heparinwirkung wird durch regelmäßige Bestimmungen der ACT überwacht. Nach der Beendigung der Melphalaninfusion wird eine halbstündige Auswaschphase durchgeführt, in der die Pumpe weiterläuft und schließlich abgekoppelt wird.
Dieses spezielle Verfahren mit chemotherapeutikumbindenden Filtern ermöglicht die Verabreichung höherer Wirkdosen von Melphalan, ohne schwere toxische Nebenwirkungen, die eine systemische Therapie mit sich bringen würde [27, 29, 30, 43]. Die Chemosaturation kann als Einzeleingriff oder wiederholt, abhängig vom klinischen Zustand und des Ansprechens des Tumors auf die Therapie, durchgeführt werden [3, 15, 47].
Komplikationen
Die Chemosaturation ist ein Verfahren mit einem relevanten Komplikationsrisiko. Die Klassifikation der unerwünschten Ereignisse erfolgt dabei anhand der Common Terminology Criteria for Adverse Events (CTCAE) [36]. In den Studien zu Wirkung und Nebenwirkungen der Chemosaturation waren die häufigsten Komplikationen den Graden I (mild) und II (moderat) zuzuordnen, und Komplikationen mit den Graden III (schwerwiegend) und IV (lebensbedrohlich) traten selten auf [23, 35, 40, 43, 47]. Frühkomplikationen waren dabei periinterventionelle hämodynamische Komplikationen, die sowohl ausgeprägte Hypotonien als auch hypertensive Entgleisungen (meist überschießende Effekte im Rahmen einer Vasopressortherapie) einschlossen [40, 43]. Einblutungen an den Punktionsstellen waren z. T. mit raumfordernden Hämatomen verbunden [23, 30, 33, 40, 43, 47–50]. Dabei wurden auch vereinzelte Fälle mit Atemwegsobstruktion, erforderlicher Reintubation und schwierigem Atemweg beschrieben [43]. Selten wurde über schwere thrombembolische Komplikationen (Apoplex, Myokardinfarkt und Lungenarterienembolie) berichtet, die auch im Zusammenhang mit postinterventionellen Protamingaben standen [13, 22, 23, 32, 35, 40]. Zu den häufigsten frühen Spätkomplikationen wurden hämatotoxische Nebenwirkungen (Thrombopenie, Anämie und Leukopenie) beschrieben, welche bei fast allen Patienten auftraten [3, 11, 13–17, 19, 23, 25, 35, 37, 40, 43, 47–50]. Ebenfalls häufig beschrieben wurden passagere Anstiege der Transaminasen sowie eine Bilirubinerhöhung. In Einzelfällen trat ein Leberversagen auf [40]. Weitere unerwünschte Ereignisse waren Übelkeit und Erbrechen, Fieber, Troponinerhöhungen, Nachblutungen, Störungen des Elektrolythaushalts und Nephrotoxizität mit passagerer Dialysepflichtigkeit [2, 35, 40, 43]. Todesfälle wurden bei Patienten mit einer sehr hohen Tumorlast im Zusammenhang mit der Chemosaturation beschrieben [30, 40].
Anästhesiologisches Management
Aufklärung und Vorbereitung
Der Eingriff wird unter Allgemeinanästhesie mit endotrachealer Intubation durchgeführt. Neben der Aufklärung für eine Allgemeinanästhesie mit invasiver Blutdrucküberwachung sind präoperative Überlegungen zu Ort und Durchführung der notwendigen arteriellen und venösen Kanülierungen notwendig. Intraoperativ muss aufgrund der Okklusion der V. cava inferior und der Nutzung eines venovenösen extrakorporalen Bypasses mit einer ausgeprägten hämodynamischen Instabilität gerechnet werden. Die Okklusion führt, ähnlich wie beim Ausklemmen der V. cava inferior bei Leberteilresektionen oder Lebertransplantationen, zu einer akuten Vorlastsenkung mit schwerer Hypotonie [34, 42]. Daher sollte im Rahmen der Patientenevaluation ein besonderes Augenmerk insbesondere auf die kardiale Belastbarkeit der Patienten gelegt werden. Diesbezüglich gibt es derzeit keine klaren Kontraindikationen, wobei die Durchführung einer transthorakalen Echokardiographie zur Abschätzung der Pumpfunktion und des Vorhandenseins von Vitien als sinnvoll eingeschätzt wird. Patienten mit fortgeschrittener Leberzirrhose, vorbestehenden ausgeprägten Blutgerinnungsstörungen, Kontrastmittelallergie oder Vorliegen von extrahepatischen Metastasen, v. a. zerebralen Metastasen und Läsionen, sind aufgrund ihres Risikoprofils nicht für eine PHMP geeignet (Tab. 1; [13]).
| Kontraindikationen für eine Chemosaturationsbehandlung |
|---|
| Leberinsuffizienz oder portale Hypertension |
| Intrazerebrale Metastasen und andere extrahepatische Tumormanifestationen, die die Gesamtprognose relevant beeinflussen |
| Intrazerebrale Läsionen mit Blutungsgefahr |
| Allergien gegen Kontrastmittel, Heparin, Latex oder Melphalan |
| Z. n. chirurgischer oder interventioneller Leberbehandlung in den letzten 4 Wochen |
| Z. n. Kausch-Whipple-Operation oder pyloruserhaltender Pankreaskopfresektion (relativ, Einzelfallentscheidung, bei stabilem Allgemeinzustand PHMP möglich) |
| Tumorlast der Leber > 50 % (relativ, Einzelfallentscheidung, häufig schlechtes Ansprechen auf PHMP) |
| Gerinnungsstörungen, die mit einer relevant erhöhten Blutungsneigung einhergehen oder allgemeine Kontraindikationen für eine Vollheparinisierung |
PHMP Perkutane hepatische Melphalanperfusion
Die Patienten sollten neben den bekannten Risiken einer Allgemeinanästhesie explizit auch über das Risiko schwerwiegender Komplikationen aufgeklärt werden. Dies sind insbesondere allergische Reaktionen auf Melphalan und weitere Pharmaka. Hinzu kommen das Risiko für Blutungskomplikationen im Rahmen der notwendigen Antikoagulation, aber auch thrombembolische Komplikationen (Apoplex, Myokardinfarkt und Lungenarterienembolie) als mögliche Folge der Protamingabe. Als weitere Risiken sind ein Herz-Kreislauf-Versagen, die Notwendigkeit einer Nachbeatmung oder erneuten Intubation, ein Nieren‑, Leber- oder Multiorganversagen mit der Notwendigkeit zum Einsatz von Organersatzverfahren (insbesondere Hämodialyse) sowie eine hierdurch verlängerte Intensivtherapie zu benennen. Präoperativ werden in unserem Zentrum jeweils 4 Erythrozytenkonzentrate und gefrorene Frischplasmakonzentrate sowie 2 Thrombozytenkonzentrate eingekreuzt.
Anästhesiologisches Management
Der Arbeitsplatz in der Angiographieeinheit ist häufig in einem Außenbereich lokalisiert, sodass die Ressourcen eines zentralen Operationsbereichs nicht oder nur eingeschränkt zur Verfügung stehen.
Die Allgemeinanästhesie kann sowohl als balancierte Anästhesie oder als totale intravenenöse Anästhesie (TIVA) mit kontinuierlicher oder diskontinuierlicher Applikation von Opioiden erfolgen [43]. Nach Präoxygenation, Laryngoskopie, Intubation und Lagekontrolle erfolgt die sorgfältige Fixierung des Tubus. Die Anästhesietiefe sollte adäquat sein, da intraoperativ eine Dislokation der platzierten Okklusionsballons vermieden werden muss. Dabei kann die Verwendung der Relaxometrie als neuromuskuläres Monitoring hilfreich sein. Leckagen an den beiden Okklusionsballons könnten zum Entweichen des Chemotherapeutikums in den systemischen Kreislauf und entsprechenden toxischen Wirkungen vom Melphalan führen (Übelkeit, Erbrechen, Diarrhö, Alopezie, Stomatitis, Infertilität, Niereninsuffizienz, Leberinsuffizienz, Knochenmarkdepression). Daher erfordert die sichere Platzierung der Ballons große Aufmerksamkeit [13, 35, 40].
Nach der 3‑ bis 4‑stündigen Interventionsdauer kann die Allgemeinanästhesie im Regelfall ohne Verzögerung ausgeleitet werden (Tab. 2).
| Anästhesieeinleitung und Katheterplatzierungen | Standardmonitoring, Anlage einer peripheren Venenverweilkanüle |
| Einleitung der Allgemeinanästhesie (Intubationsnarkose) | |
| Anlage des Harnblasenkatheters mit intravesikaler Temperaturmessung | |
| Anlage der arteriellen Blutdruckmessung (A. radialis) | |
| Sonographie, Übersicht, Hals (Halsgefäße bds., gemeinsam mit Radiologie) | |
| Anlage eines ZVK (mit mindestens einem großen Lumen) + venöse Schleuse des Extrakorporalsystems als Doppelpunktion, bevorzugt in die V. jugularis interna dextra (zwingend sonographiegestützt) | |
| Anlage der arteriellen und venösen Schleuse durch die Radiologie (A. und V. femoralis communis) | |
| Heparingabe nach Anlage aller venösen und arteriellen Zugänge mit 300 IE/kgKG, Ziel Activated Clotting Time (ACT) > 400 s | |
| Platzierung des Chemosaturationssystems (arterieller Katheter und venöser Doppelballonkatheter) durch Radiologie | |
| Anschluss des Extrakorporalsystems | Vor Anschluss des Extrakorporalsystems muss die ACT > 400 s sein, ggf. Heparinnachdosierung und erneute ACT-Kontrolle |
| Laufende Noradrenalinspritzenpumpe, mittlerer arterieller Druck (MAD) 80–90 mm Hg | |
| Start des Extrakorporalsystems durch Kardiotechnik | |
| Inflation der Ballons | Cave: Blutdruckabfall zu erwarten, Bypass noch offen |
| Lage- und Leckagekontrolle der Ballons durch Radiologie (bei Leckage Gefahr systemischer Wirkung des Chemotherapeutikums) | |
| Abklemmen des Bypass | Kontrolle ACT, ggf. erneute Heparingabe |
| Vor Abklemmen des Bypass Ziel-MAD 80–90 mm Hg | |
| Cave: deutlicher Blutdruckabfall (hohe Noradrenalindosis erforderlich) | |
| Mit dem Verschließen des Bypass Gabe von Volumenbolus (z. B. 500 ml balancierte Vollelektrolytlösung) | |
| Nach Stabilisierung MAD, Freigabe für Injektion der Chemotherapie in die Leberarterie durch Radiologie (Melphalan 3 mg/kgKG, max. 220 mg/Sitzung) | |
| Lokale Applikation des Chemotherapeutikums | Cave: Bypass muss vor Applikation des Chemotherapeutikums geschlossen sein |
| Ca. 30 min Applikationsdauer des Chemotherapeutikums | |
| Danach 30 min Auswaschphase mit Extrakorporalsystem | |
| Währenddessen ACT-Kontrolle | |
| Beendigung der Chemosaturation | Nach Beendigung des Extrakorporalsystems Anstieg des MAD mit deutlicher Reduzierung der Noradrenalindosis zu erwarten |
| Entfernung arterieller Katheter und venöser Doppelballonkatheter aus den Schleusen | |
| Alle Schleusen und ZVK werden in situ belassen | |
| Nach Auswaschphase im Konsens mit Radiologie Antagonisierung des Heparins durch Protamin (Protamindosis entsprechend der verabreichten Heparindosis) und danach Abschluss-ACT (angestrebt < 150 s) | |
| Sonographie, Übersicht, Hals (Ausschluss Blutungen/Ödeme, gemeinsam mit Radiologie) | |
| Beendigung der Anästhesie und Extubation (auf Normothermie achten) | |
| Verlegung auf die Intensivstation | |
| Postoperatives Management | Aufnahmelabor mit Blutbild, Elektrolyte, Leber- und Nierenwerte und Gerinnungsparameter. Regelmäßige Verlaufskontrollen |
| Entfernung aller zentralen Zugänge und arterielle Blutdruckmessung nach Normalisierung der Gerinnung (in der Regel am Folgetag). Ggf. Substitution. Druckverband auf Punktionsstelle der arteriellen Schleuse für 12 h | |
| Verlegung auf die Normalstation am Folgetag bei komplikationslosem Verlauf | |
| Gabe von Allopurinol zur Prophylaxe eines Tumorlysesyndroms |
ACT „Activated clotting time“, MAD mittlerer arterieller Druck
Gefäßzugänge
Nach Einleitung der Anästhesie, endotrachealer Intubation und Beginn der maschinellen Beatmung werden in unserem Zentrum 2 zentrale Venenkatheter (ZVK) in die V. jugularis interna dextra platziert. Ein ZVK sollte für die Gabe von erforderlichen Volumenboli mit einem High-Flow-Lumen (12 G) ausgestattet sein. Es können alternativ auch Dialysekatheter mit zusätzlichem kleinlumigen Schenkel für die Vasopressorinfusion verwendet werden, insbesondere, wenn absehbar ist, dass postinterventionell eine Nierenersatztherapie notwendig ist. Der zweite Zugang ist die im Hersteller-Set enthaltene venöse Schleuse zur Rückführung des filtrierten Blutes (10-F-Schleuse des Hepatic CHEMOSAT® Delivery System). Die arterielle Blutdruckmessung kann über einen separaten Zugang einer A. radialis etabliert werden oder über die Schleuse des Interventionssystems an der A. femoralis abgeleitet werden. Die Platzierungen der arteriellen und venösen Femoralschleusen für das Chemosaturationssystem werden durch den Interventionsradiologen durchgeführt.
Im Rahmen eigener Erfahrungen kam es in einigen Fällen zu mechanischen Komplikationen bei den Gefäßpunktionen, wobei diese meistens geringfügig waren (z. B. nichtvorschiebbarer Führungsdraht) [43]. Nach Mehrfachpunktionen kam es in einem Fall bereits vor der interventionsbedingten Heparinisierung zu einem ausgeprägten zervikalen Hämatom, sodass die Intervention aufgrund der Gefahr der Progression des Hämatoms bei Heparinisierung abgebrochen werden musste. Arterielle Blutungen im Bereich der Leistenregion und des Oberschenkels wurden nach Dislokation einer Schleuse beschrieben [43]. Um das Risiko von punktionsbedingten Blutungen insbesondere unter der intra-interventionell ausgeprägten Heparinisierung zu minimieren, sollten folgende Punkte beachtet werden:
Die Punktionen der zentralen Zugänge (ZVK und venöse Rückgabeschleuse) sollen primär unter ultraschallgeführter ständiger Nadelspitzenvisualisierung („real-time ultrasound guidance“) erfolgen, um die Fehlpunktionsrate bzw. die Mehrfachpunktionsrate zu verringern und das Blutungsrisiko bei der erforderlichen hochdosierten Heparingabe zu vermindern [2, 27]. Die primäre Punktionsstelle ist die rechte V. jugularis interna. Die Doppelpunktion der V. jugularis interna dextra ist erfahrungsgemäß problemlos möglich und bietet durch den anatomischen Gefäßverlauf Vorteile gegenüber der V. jugularis interna sinistra, bei deren Katheterisierung auf eine adäquate Einführtiefe und Spitzenposition im Bereich des kavoatrialen Überganges geachtet werden sollte [4, 42, 51, 52]. Bei Notwendigkeit einer Punktion der linken V. jugularis interna sollten der längere intravaskuläre Verlauf und das mögliche Risiko von Intimaläsionen bei zu kurzer Einführtiefe des ZVK berücksichtigt werden [20]. Grundsätzlich empfiehlt es sich, vor dem sterilen Abdecken der ausgewählten Punktionsstelle eine Übersichtssonographie von rechter und linker V. jugularis interna durchzuführen, um Kalibergrößen und benachbarte Arterien einzuschätzen [41]. Die Vermeidung der Punktion der V. subclavia ist angesichts des Risikos von Punktionsläsionen (Pneumothorax und intrathorakale Blutungen) empfehlenswert. Eine Lagekontrolle des ZVK kann neben dem endovaskulären EKG (bei Patienten ohne Vorhofflimmern) auch angiographisch unter Durchleuchtung stattfinden [18]. Zur Vermeidung von Dislokationen sind eine Annaht der Katheter und ein sorgfältiger Verband erforderlich. Die Punktionsstellen sollten während der Intervention regelmäßig auf eine Hämatomentwicklung und Blutungen kontrolliert werden [1, 2]. Nach der Auswaschphase, noch vor der Ausleitung der Anästhesie, ist eine erneute Übersichtssonographie des Halses sinnvoll, um Blutungen und Ödeme auszuschließen, die möglicherweise einer Extubation im Angiographiebereich entgegenstehen und eine spätere Extubation auf der Intensivstation erforderlich machen können.
Gerinnungsmanagement
Vor Etablierung des Extrakorporalkreislaufs werden 300–400 IE Heparin/kgKG i.v. appliziert (angestrebte ACT > 400 s), da es ohne Heparinisierung zu einer Gerinnselbildung im Chemosaturationsfiltersystem kommt [13, 14, 26]. Die Heparinwirkung wird während des gesamten Verfahrens überwacht und ggf. durch wiederholte Dosen an die angestrebte ACT angepasst. Nach dem Ende der Intervention empfiehlt der Hersteller des Filtersystems, die Heparinwirkung mittels Protamin zu antagonisieren, um Blutungskomplikationen zu verhindern [3, 13]. Nach vermehrten Berichten über schwere thrombembolische und allergische Komplikationen verzichtet man in einigen Zentren auf eine generelle Antagonisierung mittels Protamin [15, 22, 23]. Im Rahmen einer Risiko-Nutzen-Abwägung erscheint es empfehlenswert, anhand des individuellen Interventionsverlaufs über die Gabe von Protamin zu entscheiden. Hierzu sind die Bestimmung einer ACT nach Interventionsende und ein interdisziplinärer Konsens zur Gabe von Protamin bzw. zur Indikation von Nachbeatmung noch vor Beendigung der Anästhesie sinnvoll. Im Zentrum der Autoren wird eine ACT < 150 s vor der Verlegung auf die Intensivstation angestrebt.
Ein Großteil der Patienten entwickelt postinterventionell transitorische myeloproliferative Effekte, u. a. in Form einer Leukopenie, Anämie und Thrombopenie [15, 35]. Durch diese Effekte auf das Gerinnungssystem und bei zusätzlichem Heparineffekt können auch im Anschluss der Intervention Blutungskomplikationen auftreten. Daher ist der Kontrolle der Blutgerinnungsparameter und der klinischen Überwachung auf Blutungszeichen eine große Aufmerksamkeit zu schenken. Die Substitution von Blutkomponenten oder Plasmaderivaten sollte faktorenorientiert entsprechend den gültigen Empfehlung der Bundesärztekammer erfolgen [10].
Hämodynamisches Management
Das hämodynamische Management erfolgt mittels Vasopressorspritzenpumpe (z. B. Noradrenalin) und kristalloider Infusionslösung via Rapid Infusion System (RIS). Als Vasopressor wird vom Hersteller primär die kontinuierliche Infusion von im Vergleich zu Noradrenalin etwas weniger potentem Phenylephrin angegeben [13]. In unserem Zentrum haben wir gute Erfahrungen mit Noradrenalin und verwenden es als Standardvasopressor. Aufgrund des vorhersehbaren starken Abfalls des arteriellen Blutdrucks nach der Okklusion des Doppelballonkatheters sollte vor dem Ausklemmen des Bypass ein systolischer Blutdruck von 150–160 mm Hg angestrebt werden [11, 43]. Hier ist im Vorfeld eine besonders klare Kommunikation zwischen allen beteiligten Fachdisziplinen notwendig. Neben der Anpassung der Katecholamindosierung kann dabei auch ein präemptiver Volumenbolus erforderlich sein [3, 11, 43]. Durch den Einsatz großer Infusionsvolumina (ca. 15–30 ml/kgKG*h) kann es in Abhängigkeit vom Ausgangszustand zu einer Dilutionsanämie kommen, die angesichts des eingeschränkten Gerinnungsstatus das Risiko für relevante Blutungseffekte erhöht.
Prinzipiell ist es empfehlenswert, das hämodynamische Management überwiegend durch die Noradrenalindosierung zu steuern, um Überinfusionseffekte (Ödeme, Dilutionseffekte, Senkung der Transfusionsschwelle) zu vermeiden. Im Rahmen des Betriebes des Extrakorporalkreislaufs können als mechanische Komplikationen das temporäre Ansaugen oder die Dislokation des Doppelballonkatheters an der Venenwand auftreten (Absinken der Flussrate). Dabei kann die Volumengabe über die Pumpe und ggf. die Beendigung der Melphalaninfusion erforderlich sein. Daten zu Einsatz und Nutzen eines erweiterten hämodynamischen Monitorings bei PHMP existieren bislang nicht. Die während des Filtereinsatzes häufig beobachtete Notwendigkeit hoher Katecholamindosierungen wurde in der Vergangenheit auch einem Filtrationseffekt von endogenen und exogen zugeführten Katecholaminen zugeschrieben. Beweisende Untersuchungen diesbezüglich sind bislang jedoch nicht publiziert worden [11, 31]. Vor dem Ende der Intervention ist ggf. eine Anpassung der Katecholamindosierung zu empfehlen, um hypertone Entgleisungen und konsekutive Einblutungen bei noch ausgeprägter Antikoagulation zu vermeiden [43].
Postinterventionelle Phase
Nach einem komplikationslosen Eingriff kann die Allgemeinanästhesie beendet werden und der Patient noch im Angiographiebereich extubiert werden. Postinterventionell sollte routinemäßig eine Überwachung für mindestens einen Tag auf der Intensivstation gewährleistet werden. Bei entsprechenden Kontraindikationen für eine Extubation, wie z. B. ausgeprägten zervikalen Ödemen oder Einblutungen, sollte die Indikation für eine Nachbeatmung auf der Intensivstation großzügig gestellt werden. Unabhängig davon sollten alle erforderlichen Vorkehrungen für eine notfallmäßige Reintubation unter erschwerten Bedingungen sowohl im unmittelbaren Arbeitsbereich der Angiographie als auch auf der Intensivstation getroffen sein [21, 43]. Alle Gefäßkatheter (ZVK und Schleusen) sollten bis zur Normalisierung der Gerinnungsparameter in situ verbleiben. Dabei sollten regelmäßige Verlaufskontrollen der Basisgerinnungswerte, aktivierte partielle Thromboplastinzeit (aPTT), Prothrombinzeit (Quick-Wert oder International Normalized Ratio, INR) und Thrombozytenzahl, und arterieller Blutgasanalysen durchgeführt werden. Bei anhaltend eingeschränkter Gerinnungssituation sollte eine gezielte Substitution mit Faktoren bzw. Thrombozyten erwogen werden. Nach der Entfernung der arteriellen Schleuse sollte auf eine ausreichend lange manuelle Kompressionszeit geachtet werden und ein mehrstündiger Druckverband an der Punktionsstelle angelegt werden. Darüber hinaus sollte eine regelmäßige Inspektion der Punktionsstellen hinsichtlich Hämatomen durchgeführt werden. Angesichts häufig beobachteter postinterventioneller passagerer Knochenmarkdepression (Leukopenie, Anämie und Thrombopenie) sowie Leber- und Nierenfunktionseinschränkungen sollten regelmäßige Laborkontrollen erfolgen [43]. Bei insgesamt erhöhtem Risiko für eine postoperative Übelkeit (PONV) sollte eine prophylaktische antiemetische Therapie (z. B. mit Ondansetron) durchgeführt werden. Postinterventionell kann Fieber auftreten, welches symptomatisch mit Antipyretika (z. B. Metamizol oder Ibuprofen) behandelt werden kann. Zur Prophylaxe eines Tumorlysesyndroms wird Allopurinol p.o. für die ersten 3 postoperativen Tage empfohlen. Die Verlegung des Patienten von der Intensivstation kann bei unauffälligem Verlauf in der Regel am Folgetag erfolgen. Die Krankenhausentlassung ist häufig schon nach wenigen Tagen möglich [24, 34, 43].
Fazit für die Praxis
Die peri- und postinterventionelle Betreuung von Patienten mit Chemosaturation ist mit ausgeprägten interventionsbedingten hämodynamischen und hämostaseologischen Schwankungen verbunden.
Ein besonderes Augenmerk erfordert die präoperative Evaluation, um Patienten mit erhöhtem Risiko für Komplikationen zu identifizieren.
Aus Sicherheitsgründen erfolgt die Anlage der zentralen Venenkatheter ausschließlich ultraschallgestützt.
Nach Beendigung der Chemosaturation muss eine entsprechende Anpassung der Vasopressordosierung erfolgen, um eine Rebound-Hypertension zu vermeiden.
Eine klare Kommunikation zwischen Interventionsradiologen, Kardiotechnikern und Anästhesiologen zu den einzelnen Interventionsschritten und insbesondere vor den potenziell kritischen Phasen ist für einen sicheren peri- und postinterventionellen Verlauf essenziell.
Funding
Open Access funding enabled and organized by Projekt DEAL.
Einhaltung ethischer Richtlinien
Interessenkonflikt
P. Kliem, S. Ebel, R. Werdehausen, F. Girrbach, D. Bösemann, F. van Bömmel, T. Denecke, S. Stehr und M.F. Struck geben an, dass kein Interessenkonflikt besteht.
Für diesen Beitrag wurden von den Autor/-innen keine Studien an Menschen oder Tieren durchgeführt. Für die aufgeführten Studien gelten die jeweils dort angegebenen ethischen Richtlinien.
Footnotes

QR-Code scannen & Beitrag online lesen
Literatur
- 1.Abram J, Klocker J, Innerhofer-Pompernigg N, et al. Verletzungen herznaher Gefäße durch zentralvenöse Katheter. Anaesthesist. 2016;65(11):866–871. doi: 10.1007/s00101-016-0226-8. [DOI] [PubMed] [Google Scholar]
- 2.American Society of Anesthesiologists Practice guidelines for central venous access 2020: an updated report by the American society of anesthesiologists task force on central venous access. Anesthesiology. 2020;132(1):8–43. doi: 10.1097/ALN.0000000000002864. [DOI] [PubMed] [Google Scholar]
- 3.Artzner C, Mossakowski O, Hefferman G, et al. Chemosaturation with percutaneous hepatic perfusion of melphalan for liver-dominant metastatic uveal melanoma: a single center experience. Cancer Imaging. 2019;19(1):31. doi: 10.1186/s40644-019-0218-4. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 4.Aurshina A, Hingorani A, Alsheekh A, et al. Placement issues of hemodialysis catheters with pre-existing central lines and catheters. J Vasc Access. 2018;19(4):366–369. doi: 10.1177/1129729818757964. [DOI] [PubMed] [Google Scholar]
- 5.Beheshti MV, Denny DF, Glickman MG, et al. Percutaneous isolated liver perfusion for treatment of hepatic malignancy: preliminary report. J Vasc Interv Radiol. 1992;3(3):453–458. doi: 10.1016/s1051-0443(92)71988-5. [DOI] [PubMed] [Google Scholar]
- 6.Ben-Shabat I, Hansson C, Sternby Eilard M, et al. Isolated hepatic perfusion as a treatment for liver metastases of uveal melanoma. J Vis Exp. 2015;95:52490. doi: 10.3791/52490. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 7.Bethlehem MS, Katsarelias D, Olofsson Bagge R. Meta-analysis of isolated hepatic perfusion and percutaneous hepatic perfusion as a treatment for uveal melanoma liver metastases. Cancers. 2021 doi: 10.3390/cancers13184726. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 8.Breedis C, Young G. The blood supply of neoplasms in the liver. Am J Pathol. 1954;30(5):969–977. [PMC free article] [PubMed] [Google Scholar]
- 9.Brüning R, Tiede M, Schneider M, et al. Unresectable hepatic metastasis of uveal melanoma: hepatic chemosaturation with high-dose melphalan-long-term overall survival negatively correlates with tumor burden. Radiol Res Pract. 2020;2020:5672048. doi: 10.1155/2020/5672048. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 10.Bundesärztekammer (2020) Querschnitts-Leitlinien Querschnitts-Leitlinien zur Therapie mit Blutkomponenten und Plasmaderivaten, Gesamtnovelle 2020. https://www.bundesaerztekammer.de/fileadmin/user_upload/downloads/pdf-Ordner/MuE/Querschnitts-Leitlinien_BAEK_zur_Therapie_mit_Blutkomponenten_und_Plasmaderivaten-Gesamtnovelle_2020.pdf. Zugegriffen: 26. März 2022
- 11.Carr MJ, Sun J, Cohen JB, et al. Over 12 years single institutional experience performing percutaneous hepatic perfusion for unresectable liver metastases. Cancer Control. 2020;27(1):1073274820983019. doi: 10.1177/1073274820983019. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 12.Cazejust J, Bessoud B, Colignon N, et al. Hepatocellular carcinoma vascularization: from the most common to the lesser known arteries. Diagn Interv Imaging. 2014;95(1):27–36. doi: 10.1016/j.diii.2013.04.015. [DOI] [PubMed] [Google Scholar]
- 13.CHEMOSAT® . Hepatisches Applikationssystem für Melphalan-Hydrochlorid zur Injektion. Gebrauchsanweisung Version 120055 Rev D. 08.03.2021. Queensbury, NY: Delcath systems inc; 2021. [Google Scholar]
- 14.Dewald CLA, Becker LS, Maschke SK, et al. Percutaneous isolated hepatic perfusion (chemosaturation) with melphalan following right hemihepatectomy in patients with cholangiocarcinoma and metastatic uveal melanoma: peri- and post-interventional adverse events and therapy response compared to a matched group without prior liver surgery. Clin Exp Metastasis. 2020;37(6):683–692. doi: 10.1007/s10585-020-10057-9. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 15.Dewald CLA, Hinrichs JB, Becker LS, et al. Chemosaturation durch perkutane hepatische Perfusion mit Melphalan bei hepatisch metastasiertem Aderhautmelanom: eine Überlebens- und Sicherheitsanalyse. RoFo. 2021;193(8):928–936. doi: 10.1055/a-1348-1932. [DOI] [PubMed] [Google Scholar]
- 16.Dewald CLA, Warnke M-M, Brüning R, et al. Percutaneous hepatic perfusion (PHP) with melphalan in liver-dominant metastatic uveal melanoma: the German experience. Cancers. 2021 doi: 10.3390/cancers14010118. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 17.Forster MR, Rashid OM, Perez MC, et al. Chemosaturation with percutaneous hepatic perfusion for unresectable metastatic melanoma or sarcoma to the liver: a single institution experience. J Surg Oncol. 2014;109(5):434–439. doi: 10.1002/jso.23501. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 18.Gebhard RE, Szmuk P, Pivalizza EG, et al. The accuracy of electrocardiogram-controlled central line placement. Anesth Analg. 2007;104(1):65–70. doi: 10.1213/01.ane.0000250224.02440.fe. [DOI] [PubMed] [Google Scholar]
- 19.Glazer ES, Zager JS. Chemosaturation with percutaneous hepatic perfusion in unresectable hepatic metastases. Cancer Control. 2017;24(1):96–101. doi: 10.1177/107327481702400116. [DOI] [PubMed] [Google Scholar]
- 20.Gravenstein N, Blackshear RH. In vitro evaluation of relative perforating potential of central venous catheters: comparison of materials, selected models, number of lumens, and angles of incidence to simulated membrane. J Clin Monitor Comput. 1991;7(1):1–6. doi: 10.1007/BF01617891. [DOI] [PubMed] [Google Scholar]
- 21.Hansel J, Rogers AM, Lewis SR, et al. Videolaryngoscopy versus direct laryngoscopy for adults undergoing tracheal intubation. Cochrane Database Syst Rev. 2022;4:CD011136. doi: 10.1002/14651858.CD011136.pub3. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 22.Hughes MS, Zager J, Faries M, et al. Results of a randomized controlled multicenter phase III trial of percutaneous hepatic perfusion compared with best available care for patients with melanoma liver metastases. Ann Surg Oncol. 2016;23(4):1309–1319. doi: 10.1245/s10434-015-4968-3. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 23.Karydis I, Gangi A, Wheater MJ, et al. Percutaneous hepatic perfusion with melphalan in uveal melanoma: a safe and effective treatment modality in an orphan disease. J Surg Oncol. 2018;117(6):1170–1178. doi: 10.1002/jso.24956. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 24.Keller H, Lotz G, Zangos S, et al. Extrakorporale Perfusion mit dem Delcath-System: Methodik der intraarteriellen ultrahochdosierten Chemotherapie der isolierten Leber. Kardiotechnik. 2014;2:37–40. [Google Scholar]
- 25.Kirstein MM, Marquardt S, Jedicke N, et al. Safety and efficacy of chemosaturation in patients with primary and secondary liver tumors. J Cancer Res Clin Oncol. 2017;143(10):2113–2121. doi: 10.1007/s00432-017-2461-z. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 26.Kuhner M, Tan B, Fiedler MO, et al. Thrombotischer Verschluss der extrakorporalen Zirkulation während hepatischer Chemosaturation trotz zielgerechter Antikoagulation: Ein Fallbericht. Anästhesiologie. 2022 doi: 10.1007/s00101-022-01175-y. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 27.Lamperti M, Biasucci DG, Disma N, et al. European society of anaesthesiology guidelines on peri-operative use of ultrasound-guided for vascular access (PERSEUS vascular access) Eur J Anaesthesiol. 2020;37(5):344–376. doi: 10.1097/EJA.0000000000001180. [DOI] [PubMed] [Google Scholar]
- 28.Lane AM, Kim IK, Gragoudas ES. Survival rates in patients after treatment for metastasis from uveal melanoma. JAMA Ophthalmol. 2018;136(9):981–986. doi: 10.1001/jamaophthalmol.2018.2466. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 29.de Leede EM, Burgmans MC, Meijer TS, et al. Prospective clinical and pharmacological evaluation of the Delcath system’s second-generation (GEN2) hemofiltration system in patients undergoing percutaneous hepatic perfusion with melphalan. Cardiovasc Intervent Radiol. 2017;40(8):1196–1205. doi: 10.1007/s00270-017-1630-4. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 30.Marquardt S, Kirstein MM, Brüning R, et al. Percutaneous hepatic perfusion (chemosaturation) with melphalan in patients with intrahepatic cholangiocarcinoma: European multicentre study on safety, short-term effects and survival. Eur Radiol. 2019;29(4):1882–1892. doi: 10.1007/s00330-018-5729-z. [DOI] [PubMed] [Google Scholar]
- 31.McEwan PE, Bailey L, Trost D, et al. Percutaneous hepatic perfusion with filtered melphalan for localized treatment of metastatic hepatic disease: a risk assessment. Int J Toxicol. 2018;37(6):434–447. doi: 10.1177/1091581818811306. [DOI] [PubMed] [Google Scholar]
- 32.Meijer TS, Burgmans MC, Fiocco M, et al. Safety of percutaneous hepatic perfusion with melphalan in patients with unresectable liver metastases from ocular melanoma using the Delcath systems’ second-generation hemofiltration system: a prospective non-randomized phase II trial. Cardiovasc Intervent Radiol. 2019;42(6):841–852. doi: 10.1007/s00270-019-02177-x. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 33.Meijer TS, Burgmans MC, de Leede EM, et al. Percutaneous hepatic perfusion with melphalan in patients with unresectable ocular melanoma metastases confined to the liver: a prospective phase II study. Ann Surg Oncol. 2021;28(2):1130–1141. doi: 10.1245/s10434-020-08741-x. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 34.Miao N, Pingpank JF, Alexander HR, et al. Percutaneous hepatic perfusion in patients with metastatic liver cancer: anesthetic, hemodynamic, and metabolic considerations. Ann Surg Oncol. 2008;15(3):815–823. doi: 10.1245/s10434-007-9781-1. [DOI] [PubMed] [Google Scholar]
- 35.Modi S, Gibson T, Vigneswaran G, et al. Chemosaturation with percutaneous hepatic perfusion of melphalan for metastatic uveal melanoma. Melanoma Res. 2022;32(2):103–111. doi: 10.1097/CMR.0000000000000806. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 36.National Cancer Institute (2017) Common terminology criteria for adverse events (CTCAE). https://ctep.cancer.gov/protocoldevelopment/electronic_applications/ctc.htm. Zugegriffen: 26. März 2022
- 37.Pingpank JF, Hughes MS, Alexander HR, et al. A phase III random assignment trial comparing percutaneous hepatic perfusion with melphalan (PHP-mel) to standard of care for patients with hepatic metastases from metastatic ocular or cutaneous melanoma. J Clin Oncol. 2010;28(18):LBA8512-LBA8512. doi: 10.1200/jco.2010.28.18_suppl.lba8512. [DOI] [Google Scholar]
- 38.Pingpank JF, Libutti SK, Chang R, et al. Phase I study of hepatic arterial melphalan infusion and hepatic venous hemofiltration using percutaneously placed catheters in patients with unresectable hepatic malignancies. J Clin Oncol. 2005;23(15):3465–3474. doi: 10.1200/JCO.2005.00.927. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 39.Robert Koch-Institut . Krebs in Deutschland für 2017/2018. Berlin: Robert Koch-Institut; 2021. [Google Scholar]
- 40.Schönfeld L, Hinrichs JB, Marquardt S, et al. Chemosaturation with percutaneous hepatic perfusion is effective in patients with ocular melanoma and cholangiocarcinoma. J Cancer Res Clin Oncol. 2020;146(11):3003–3012. doi: 10.1007/s00432-020-03289-5. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 41.Schummer W, Köditz JA, Schelenz C, et al. Pre-procedure ultrasound increases the success and safety of central venous catheterization. Br J Anaesth. 2014;113(1):122–129. doi: 10.1093/bja/aeu049. [DOI] [PubMed] [Google Scholar]
- 42.Smith T, Kaufman C, Quencer K. Internal jugular central venous catheter tip migration: patient and procedural factors. Tomography. 2022;8(2):1033–1040. doi: 10.3390/tomography8020083. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 43.Struck MF, Kliem P, Ebel S, et al. Percutaneous hepatic melphalan perfusion: single center experience of procedural characteristics, hemodynamic response, complications, and postoperative recovery. PLoS ONE. 2021;16(7):e0254817. doi: 10.1371/journal.pone.0254817. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 44.Sung H, Ferlay J, Siegel RL, et al. Global cancer statistics 2020: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin. 2021;71(3):209–249. doi: 10.3322/caac.21660. [DOI] [PubMed] [Google Scholar]
- 45.Taylor I, Bennett R, Sherriff S. The blood supply of colorectal liver metastases. Br J Cancer. 1978;38(6):749–756. doi: 10.1038/bjc.1978.283. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 46.Vahrmeijer AL, van Dierendonck JH, Keizer HJ, et al. Increased local cytostatic drug exposure by isolated hepatic perfusion: a phase I clinical and pharmacologic evaluation of treatment with high dose melphalan in patients with colorectal cancer confined to the liver. Br J Cancer. 2000;82(9):1539–1546. doi: 10.1054/bjoc.2000.1175. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 47.Veelken R, Maiwald B, Strocka S, et al. Repeated percutaneous hepatic perfusion with melphalan can maintain long-term response in patients with liver cancers. Cardiovasc Intervent Radiol. 2022;45(2):218–222. doi: 10.1007/s00270-021-02983-2. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 48.Vogel A, Gupta S, Zeile M, et al. Chemosaturation percutaneous hepatic perfusion: a systematic review. Adv Ther. 2017;33(12):2122–2138. doi: 10.1007/s12325-016-0424-4. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 49.Vogl TJ, Koch SA, Lotz G, et al. Percutaneous isolated hepatic perfusion as a treatment for isolated hepatic metastases of uveal melanoma: patient outcome and safety in a multi-centre study. Cardiovasc Intervent Radiol. 2017;40(6):864–872. doi: 10.1007/s00270-017-1588-2. [DOI] [PubMed] [Google Scholar]
- 50.Vogl TJ, Zangos S, Scholtz JE, et al. Chemosaturation with percutaneous hepatic perfusions of melphalan for hepatic metastases: experience from two European centers. RoFo. 2014;186(10):937–944. doi: 10.1055/s-0034-1366081. [DOI] [PubMed] [Google Scholar]
- 51.Walshe C, Phelan D, Bourke J, et al. Vascular erosion by central venous catheters used for total parenteral nutrition. Intensive Care Med. 2007;33(3):534–347. doi: 10.1007/s00134-006-0507-9. [DOI] [PubMed] [Google Scholar]
- 52.Weber E, Liberek T, Wołyniec W, et al. Catheter tip malposition after percutaneous placement of tunneled hemodialysis catheters. Hemodial Int. 2015;19(4):509–513. doi: 10.1111/hdi.12303. [DOI] [PubMed] [Google Scholar]
- 53.Wessely A, Steeb T, Erdmann M, et al. The role of immune checkpoint blockade in uveal melanoma. Int J Mol Sci. 2020;21(3):879. doi: 10.3390/ijms21030879. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 54.Woodman SE. Metastatic uveal melanoma: biology and emerging treatments. Cancer J. 2012;18(2):148–152. doi: 10.1097/PPO.0b013e31824bd256. [DOI] [PMC free article] [PubMed] [Google Scholar]