Abstract
临床研究证实缓慢呼吸具有显著降低血压的疗效。本文基于此原理设计了一种便携式慢呼吸训练降压仪。降压仪采用微型变极距电容传感器采集呼吸信号,以 STM32 为主控芯片,用 WT588D 语音芯片实现语音、音乐引导慢呼吸训练,并在 3.5 寸彩屏上实现呼吸状态指引。针对患者难以适应慢呼吸训练的问题,提出了基于反馈调节的智能引导呼吸算法来训练患者慢呼吸。10 名高血压患者使用本仪器进行了累计 100 次慢呼吸训练,结果表明:随着训练次数增加,患者呼吸率从(15.16±0.92)次/分降低到(9.40±0.29)次/分,同时呼吸率低于 8 次/分的时间占总治疗时间的比例也从 0.079±0.017 升高到 0.392±0.019。因此,本研究设计的降压仪能有效引导高血压患者进行慢呼吸训练。
Keywords: 高血压, 慢呼吸训练, 降压仪, 便携式
Abstract
Clinical studies had demonstrated that slow breathing could lower blood pressure significantly. Based on this knowledge, a portable blood pressure depressor was designed in this study. The device used a miniature variable distance capacitive sensor to collect respiratory signal, an STM32 as the main control chip, a WT588D voice chip to generate voice and music and guide slow breathing, and a 3.5-inch color screen to display breathing state and provide guidance. For patients with difficulty in adapting themselves to the slow breathing training, an intelligent guiding breathing algorithm based on feedback regulation mechanism was proposed to train patients to breathe slowly. Ten volunteers with hypertension were recruited and then trained to breathe slowly, accumulating up to 100 times using this device. The results showed that breath rate of the volunteers decreased from 15.16±0.92 times per minute to 9.40±0.29 times per minute, and meanwhile, time length of breath rate less than 8 times per minute in the proportion of total treatment time increased from 0.079±0.017 to 0.392±0.019 as the training times increased. In a conclusion, the proposed blood pressure depressor worked effectively in guiding slow breathing training.
Keywords: hypertension, slow breathing training, blood pressure depressor, portable
引 言
高血压病是一种全世界患病人数最多、流行范围较广、难以彻底根治的心血管疾病,常常引起心、脑、肾及其它器官的并发症,如心力衰竭、心肌梗死、慢性肾脏病等高死亡率疾病,严重危害了人类的生命健康[1-2]。常规治疗高血压的方法为药物治疗,但因长期的药物治疗存在药物副作用明显、患者经济负担重等弊端,国内外研究人员一直在寻求有效的非药物降压治疗方法。
近年来,慢呼吸训练降低高血压的非药物治疗方法逐渐成为了研究热点,研究表明:通过缓慢呼吸训练降低高血压患者的呼吸率(breath per minute,BPM),可有效降低患者血压[3-8],特别是将 BPM 控制在低于 8 次/分的慢呼吸状态,具有显著降低血压的疗效[9-10]。以色列的 InterCure 公司根据慢呼吸训练降低血压的原理,研制了 RESPeRATE 降压仪[6, 10],该仪器是目前唯一获得美国食品和药品管理局认证的非药物高血压治疗仪;而国内相关仪器研究尚未见报道。本课题组前期设计了基于个人电脑的高血压治疗系统[11-12],但该系统不便于患者随身携带进行慢呼吸训练,且治疗过程中缺乏智能化的提醒机制,临床试验中志愿者在训练初始阶段难以适应慢呼吸节奏。
针对上述问题,本文基于慢呼吸训练降压原理,采用 UCOSII 操作系统,研制了一种便携式智能化的高血压降压仪,并提出了一种基于反馈调节的智能引导呼吸算法,通过多次反馈与迭代调节,自适应调整节律,减缓患者的呼吸,增加患者慢呼吸训练的适应性和舒适度。本文研究旨在提供一种自适应高血压患者进行慢呼吸训练的降压仪,为进一步临床试验研究降压疗效提供设备。
1. 便携式降压仪工作原理
本文设计的降压仪主要由降压仪主机、穿戴式呼吸传感器和耳机三部分组成。使用前需安装传感器和耳机接头,患者佩戴传感器于腹部并带上耳机。开启训练前,患者需坐卧放松身心 5~10 min[13-14]。慢呼吸训练引导信号由语音、音乐(听觉信号)和方向箭头(视觉信号)共同组成。启动慢呼吸训练后,患者跟随呼吸引导信号节奏呼吸,此时变极距电容传感器通过呼吸感应体积描记技术原理获取变频信号[15],经算法转换为 BPM 值,再将 BPM 值传递给本文设计的基于反馈调节的智能引导呼吸算法,通过多次反馈与迭代调节,自适应患者的呼吸。在训练过程中,患者不必故意屏气,只需按自己最舒适的节奏呼吸,智能反馈调节算法能逐渐引导患者向缓慢呼吸进行。
2. 便携式降压仪的硬件设计
2.1. 硬件总体结构
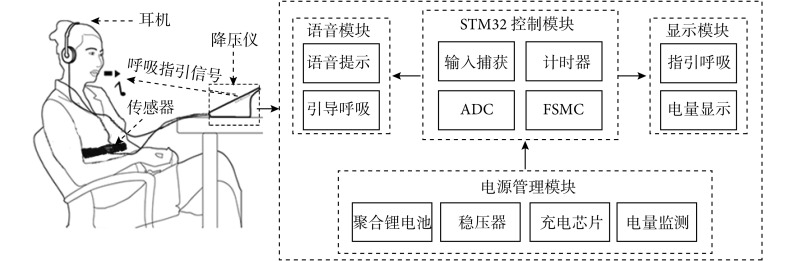
降压仪设计原理如图 1 所示,STM32 作为核心控制器,接收传感器所测数据,语音模块、显示模块均由其通过软件算法设计控制,电源管理模块为降压仪系统供电。
图 1.
Block diagram of the pressure normalizing apparatus ADC: analog to digital converter; FSMC: flexible static memory controller
降压仪结构框图 ADC:模数转换器;FSMC:可变静态存储控制器
2.2. STM32 控制模块
基于本文降压仪实时处理性能、外设和彩屏显示方面考虑,选择的主控芯片为 ST(意法半导体)公司的 STM32F103ZET6,其内核为 Cortex-M3 的 ARM 32 位 CPU,工作频率 72 MHz。其优异的性能表现在:超低的价格,超多的外设,丰富的存储空间,优异的实时性能,杰出的功耗控制和极低的开发成本等。
2.3. 传感器模块
传感器是实现 BPM 检测的核心模块,本文基于呼吸感应体积变化原理[16],在胸腹部横向具有最大的体积变化,可适应于不同胖瘦身形的患者进行 BPM 的检测。优化微型变极距电容传感器的设计,以呼吸感应体积变化的横向为极距变化方向,改进设计的微型变极距电容传感器具有更高的灵敏度,非常适合中老年高血压患者检测 BPM。微型变极距电容传感器主要由变极距敏感电容、NE555 芯片及其他部件组成。敏感电容 CX 的两极一端接地,另一端接 NE555 的第 2 管脚和第 6 管脚。传感器电路原理图如图 2 所示。
图 2.
Variable distance capacitance sensor circuit
变极距电容传感器电路
变极距电容传感器的工作原理:在电路上电时,由于 CX 电容两端的电压不能突变,则 2 脚为低电平,此时 NE555 被置位,3 脚输出高电平。随着时间的推移,高电平经过 R1 不断给 CX 充电,导致 CX 两端电压不断升高,此时等同于芯片 6 脚电压的升高。当 6 脚电压升到 2VCC/3 后,NE555 芯片复位,此时 3 脚输出低电平,使得储存于 CX 的电荷经过 R1 放电,等价于 2 脚电压值逐渐下降,直到降至 VCC/3 后,再次使得 NE555 置位,3 脚又可以向电容 CX 充电。如此循环往复,最终在芯片 3 脚端输出一系列频率随敏感电容极距变化而相应变化的幅值确定的波形。其中 R1 和 CX 的大小决定了传感器的振荡频率。
3 脚输出高电平,也即 CX(公式中的 C)的充电时间:
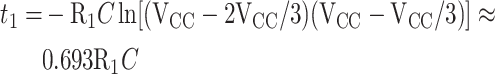 |
1 |
3 脚输出低电平,也即 CX 的放电时间:
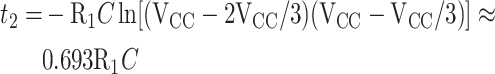 |
2 |
 |
3 |
 |
4 |
BPM 检测原理:当人吸气时,胸腹部向外凸起,传感器因受吸气的横向拉伸,使 Cx 电容极距增大,周期变小,频率变高;当人呼气时,胸腹部向里收缩,传感器的极距逐渐恢复正常,周期变大,频率变低。在此电路中,敏感电容的变化程度反映在输出信号频率的改变上,而敏感电容的变化是基于呼吸感应体积变化引起的,对输出波形频率特点的判定,经算法处理可获得 BPM 值。
2.4. 语音模块
语音模块的核心功能是通过语音或音乐引导高血压患者进行慢呼吸训练。本文语音模块采用 WT588D 语音芯片,此芯片集成可重复擦除和烧写的语音单片机芯片,且具有数模转化器(digital to analog converter,DAC),可输出高质量的语音。本文降压仪设计中,考虑到可程控、低功耗的需求,选择三线串口控制模式,其应用方框图如图 3 所示,首先通过录音设备将语音进行录制,再将录制的语音经过 Cool Edit PRO 软件进行去噪、组合等,然后将语音经过上位机 Voice Chip 软件加载、编译,最后通过 USB 下载入芯片。语音芯片通过 STM32 控制端的指令,完成相应地址中语音的输出或 BUSY 状态指示。
图 3.
Block diagram of the voice module application
语音模块应用方框图
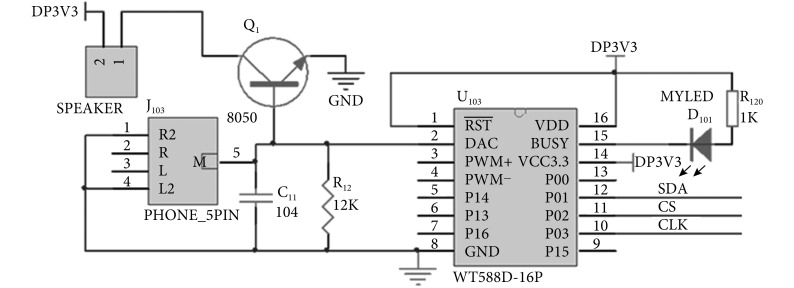
三线串口控制模式的 DAC 应用电路如图 4 所示,通信由片选信号 CS、数据信号 SDA 和时钟信号 CLK 组成,通信时序将在软件部分详述,降压仪通过三线串口控制模式实现语音芯片的命令控制和语音调控播放。
图 4.
DAC output circuit
DAC 输出电路
2.5. 显示模块
显示模块的突出功能在于通过屏幕显示呼吸方向指引,可引导高血压患者经过视觉进行慢呼吸训练。另外为了适应不同高血压患者的操作习惯,设置触摸和按键双模式交互操作,显示屏配置触摸功能可满足降压仪的设计。本文基于视觉图像质量和触摸操作性能考虑,选择了 3.5 寸的 TFT-LCD 显示屏。TFT-LCD 不同于无源的 TN-LCD 和 STN-LCD,在屏的每一个像素点上都设置了一个薄膜晶体管,有效克服了非选通时的信号串扰问题,使得屏的静态特性与扫描线数无关,大大提高了图像质量。其特点包括 320*480 的分辨率、自带触摸屏以及 16 位真彩色显示。
2.6. 电源模块
电源模块是降压仪工作的必要前提,考虑到仪器稳压、可便携充电等要求,设计降压仪的电源模块采用成熟的稳压电路、mini USB 接口电路和充电电路。用可充电锂电池,配备 3.7 V、1 400 mA 的锂电池。
稳压电路兼有稳压和电量检测功能,稳压由 CAT6219 稳压芯片实现,电量通过主控模块的 ADC 进行实时检测,并由彩屏显示当前电量状态。mini USB 接口部分使用电源适配器将 220 V 的电压转为 5 V,再连接 mini USB 接口,供系统充电。充电电路中,CN3068 芯片可以对单节锂电池进行恒压或恒流充电。CN3068 在应用时,只需很少的外围元件,同时也符合 USB 总线技术规范,在便携式的应用范围比较适合,此芯片固定的恒压充电电压值为 4.2 V,在充电时,可通过一个外部电阻进行调节。
3. 慢呼吸训练引导算法设计及实现
3.1. 获取呼吸率 BPM
微型变极距电容传感器跟随呼吸感应胸腹部的横向变化,可在传感器输出端检测出幅值相同、频率变化的波形。判定一次呼吸过程的示意图见图 5,分别为平常呼吸和缓慢呼吸状态下,变极距电容传感器输出波形频率变化与呼吸波形对应关系图。平常呼吸状态下,传感器输出最大频率 fmax 和最小频率 fmin 分别对应吸气的终点和呼气的终点;而缓慢呼吸状态下,有时因为心脏的搏动,导致检测出的 fmax 并非吸气的终点,这就要求呼吸率检测算法具备一定的抗干扰能力。本文设计的呼吸率检测算法如图 6所示,该算法利用 STM32 控制器捕获连续 10 个周期波形的时间,求其平均频率,基于变频信号求差分,再结合阈值增强算法抗干扰能力。该算法根据 fmin 的平稳周期性检测,而不再采用传统的 fmax 周期性计算 BPM,因此可有效地检测出平常呼吸状态和缓慢呼吸状态下的 BPM 值。
图 5.
Relationship between sensor frequency and respi-ratory waveform
传感器频率变化与呼吸波形的关系
图 6.
BPM detection algorithm
BPM 检测算法
3.2. 基于反馈调节的智能引导呼吸算法设计
本论文设计自适应患者慢呼吸的智能引导呼吸算法,通过呼吸传感器的呼吸感应体积描记技术获得变频信号,经 BPM 检测算法,每检测到 4 次有效呼吸时计算一次当前呼吸率(current breath per minute, CBPM),CBPM 值被逐级判定后获得当前反馈引导呼吸音乐的位置(Position)。若当前的位置不等于先前的位置(prePosition),则引导呼吸音乐按 Position 值对后续引导呼吸音乐的节律进行相应的改变,反之,引导呼吸音乐按原有减缓速率继续引导呼吸,通过多次反馈与迭代调节,从而自适应匹配患者的慢呼吸训练。开始阶段,引导呼吸音乐的节律是不断变慢的,达到慢呼吸训练效果时,又趋于平稳的音乐节律,从而实现了自适应的智能引导训练。其算法如图 7 所示,逐步引导患者将呼吸速率调整为 8 次/分的慢呼吸训练状态。用户在呼吸过程中不必故意屏气或者用力延长呼吸,如果用户觉得呼、吸速率太慢或者费力,只需按照最舒适的方式进行呼吸,算法会自适应调整乐律,再次根据患者的呼吸速率引导患者向缓慢呼吸进行。
图 7.
Algorithm of guide breathing based on feedback regulation
基于反馈调节的呼吸引导算法
3.3. 音乐引导控制设计
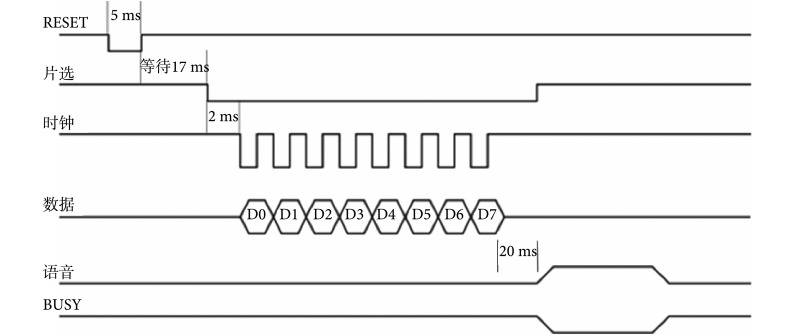
音乐引导控制的通信协议类似于串行外设接口(serial peripheral interface,SPI),由片选信号 CS、时钟信号 CLK 和数据信号 SDA 组成。复位信号 RESET 在发码前先置为低电平 5 ms 左右,再置为高电平 17 ms 左右。在通信过程中 RESET 信号要一直保持高电平状态。CS 则应置为低电平 2~10 ms 的时间,以唤醒 WT588D 语音芯片。接收数据时,低位在前,高位在后,并在时钟的上升沿开始接收数据。工作的时钟周期介于 200 μs~2 ms 之间,可选 300 μs 作为时钟周期。接收数据成功后,语音播放 BUSY 忙信号在 20 ms 后输出作为响应。发送数据时,也应先发低位,再发高位。发码完成后数据线、时钟线、片选线均需保持高电平。在发送数据时,可不用先发命令再发指令码。D0~D7 表示一个地址或者命令数据,音量调控指令为 E0H~E7H,地址指令为 00H~DBH,需要停止播放时可发 FEH,需要循环播放时可发 F2H,控制时序如图 8 所示。
图 8.
Diagram of the music guidance control timing
音乐引导控制时序图
4. 志愿者试验
基于上述硬件及软件算法设计,本文研制出便携式慢呼吸训练降压仪,并通过了药监局规定的医疗器械注册检验,能安全地进行志愿者试验研究。
2016 年 5 月开展了初步的志愿者试验,因慢呼吸训练降压效果的临床研究已经大量开展,故本试验研究目的重点在于验证本降压仪能否有效引导患者进行慢呼吸训练。
试验对象为 10 名高血压患者,所有志愿者在详细阅读完本研究的试验目的和流程后,均签署了知情同意书,同时试验遵守《赫尔辛基宣言》的伦理原则。志愿者的收缩压范围为 122~138 mm Hg,舒张压范围为 76~92 mm Hg,男女各 5 名,年龄为 42~68 岁。
试验为期 5 天,每天 9:00 和 18:00 时段进行慢呼吸训练,先让受试者静坐 5 min,然后进行慢呼吸训练 15 min,如图 9 所示,记录每次的 BPM 值,当次训练结束后,求 BPM 和 BPM 低于 8 次/分的时间占总治疗时间的比例(以下简称:归一化占比),结果如表 1 和表 2 所示。
图 9.
Slow breathing training for a hypertensive volunteer
高血压志愿者进行慢呼吸训练
表 1. Statistics results of BPM.
BPM 统计结果
| 第 N次训练 | 第 n名患者的 BPM/(次·分–1) | |||||||||
| N-001 | N-002 | N-003 | N-004 | N-005 | N-006 | N-007 | N-008 | N-009 | N-010 | |
| 1 | 16.3 | 15.6 | 16.0 | 14.3 | 15.1 | 14.2 | 13.6 | 15.5 | 14.8 | 16.2 |
| 2 | 14.8 | 14.4 | 14.2 | 13.4 | 13.8 | 13.1 | 12.5 | 14.1 | 13.6 | 14.3 |
| 3 | 13.6 | 13.3 | 13.4 | 12.3 | 12.7 | 12.1 | 11.8 | 13.1 | 12.6 | 13.1 |
| 4 | 12.5 | 12.5 | 12.1 | 11.2 | 12.0 | 11.2 | 10.9 | 12.2 | 11.8 | 12.2 |
| 5 | 11.2 | 11.5 | 11.3 | 10.4 | 10.8 | 10.5 | 10.3 | 11.4 | 10.6 | 11.0 |
| 6 | 10.3 | 10.1 | 10.5 | 10.1 | 10.4 | 10.2 | 9.6 | 10.6 | 9.9 | 10.1 |
| 7 | 9.8 | 9.5 | 10.1 | 9.6 | 9.7 | 9.6 | 9.2 | 10.0 | 9.5 | 9.5 |
| 8 | 9.5 | 9.4 | 9.6 | 9.3 | 9.5 | 9.6 | 9.0 | 9.6 | 9.5 | 9.0 |
| 9 | 9.2 | 9.2 | 9.5 | 9.5 | 9.6 | 9.2 | 8.8 | 9.5 | 9.8 | 8.9 |
| 10 | 9.0 | 9.3 | 9.6 | 9.5 | 9.8 | 9.5 | 8.9 | 9.7 | 9.5 | 9.2 |
表 2. Statistics results of normalized accounting with BPM less than 8.0 breath/min.
BPM<8.0 次/分的时间归一化占比统计结果
| 第 N次训练 | 第 n名患者 BPM<8.0 次/分的时间归一化占比 | |||||||||
| N-001 | N-002 | N-003 | N-004 | N-005 | N-006 | N-007 | N-008 | N-009 | N-010 | |
| 1 | 0.062 | 0.072 | 0.063 | 0.088 | 0.079 | 0.089 | 0.122 | 0.073 | 0.081 | 0.065 |
| 2 | 0.113 | 0.123 | 0.112 | 0.157 | 0.148 | 0.156 | 0.197 | 0.126 | 0.176 | 0.135 |
| 3 | 0.187 | 0.189 | 0.202 | 0.213 | 0.216 | 0.205 | 0.243 | 0.208 | 0.232 | 0.198 |
| 4 | 0.236 | 0.248 | 0.254 | 0.268 | 0.284 | 0.278 | 0.287 | 0.253 | 0.252 | 0.249 |
| 5 | 0.305 | 0.308 | 0.316 | 0.328 | 0.342 | 0.346 | 0.352 | 0.321 | 0.318 | 0.308 |
| 6 | 0.342 | 0.336 | 0.358 | 0.358 | 0.372 | 0.371 | 0.382 | 0.354 | 0.356 | 0.346 |
| 7 | 0.356 | 0.364 | 0.375 | 0.382 | 0.396 | 0.396 | 0.403 | 0.360 | 0.362 | 0.358 |
| 8 | 0.362 | 0.372 | 0.383 | 0.391 | 0.396 | 0.392 | 0.406 | 0.365 | 0.368 | 0.366 |
| 9 | 0.381 | 0.398 | 0.375 | 0.383 | 0.384 | 0.408 | 0.415 | 0.361 | 0.354 | 0.375 |
| 10 | 0.401 | 0.418 | 0.375 | 0.385 | 0.394 | 0.398 | 0.425 | 0.364 | 0.376 | 0.384 |
为了更直观地分析降压仪引导慢呼吸训练的有效性,本文采用 Origin 软件处理表 1 和表 2 中的数据,作图分析每次试验的 BPM 及 BPM 低于 8 次/分的时间归一化占比变化趋势,其结果如图 10 所示。由表 1、表 2 和图 10 可见,随着训练次数的增多,受试患者的 BPM 值从首次的(15.16±0.92)次/分降低到第 10 次的(9.40±0.29)次/分,并有达到平稳的趋势;而 BPM<8.0 次/分的时间归一化占比也从 0.079±0.017 增高到 0.392±0.019,并慢慢趋于稳定。
图 10.
Trends of BPM changes and normalized accounting with BPM less than 8.0 breath/min
BPM 变化与 BPM<8.0 次/分的归一化占比变化趋势
分析试验结果可知,BPM 值逐渐降低,表明患者随着训练次数的增加逐渐适应慢呼吸训练;BPM 低于 8 次/分的时间归一化占比值逐渐升高,表明 BPM 稳定在有效降压的呼吸率范围内的时间越来越长。试验结果验证了本文提出的基于反馈调节的智能引导呼吸算法的降压仪能够增强患者慢呼吸的适应性及舒适度,有效地引导高血压患者进行慢呼吸训练。
5. 结论
本文基于课题组前期对生物反馈高血压治疗系统的研究,对降压仪的便携性和智能化进行了优化设计,重点研究设计了基于反馈调节的智能引导呼吸算法,增强患者对慢呼吸训练的适应性。通过 STM32 采集变极距电容传感器的信号,经优化设计的 BPM 检测算法获取 BPM 值,再经基于反馈调节的智能引导呼吸算法,多次反馈与迭代调节,自适应患者进行慢呼吸训练。在完成试验样机的研制后,进行了初步的志愿者试验,结果表明:基于反馈调节的智能引导呼吸算法的降压仪能自适应患者进行慢性呼吸训练,增强患者慢呼吸的适应性及舒适度,有效地引导高血压患者进行慢呼吸训练。
Funding Statement
国家科技支撑计划项目(2015BAI01B14,2013BAI03B04)
References
- 1.Mahtani K R, Beinortas T, Bauza K, et al. Device-guided breathing for hypertension: a summary evidence review. Curr Hypertens Rep. 2016;18(4):33. doi: 10.1007/s11906-016-0631-z. [DOI] [PubMed] [Google Scholar]
- 2.高血压联盟. 中国高血压患者教育指南. 中华高血压杂志. 2013;6(12):1123–1149. [Google Scholar]
- 3.Mahtani K R, Nunan D, Heneghan C J. Device-guided breathing exercises in the control of human blood pressure: systematic review and meta-analysis. J Hypertens. 2012;30(5):852–860. doi: 10.1097/HJH.0b013e3283520077. [DOI] [PubMed] [Google Scholar]
- 4.Landman G W, van Hateren K J, van Dijk P R, et al. Efficacy of device-guided breathing for hypertension in blinded, randomized, active-controlled trials: a meta-analysis of individual patient data. JAMA Intern Med. 2014;174(11):1815–1821. doi: 10.1001/jamainternmed.2014.4336. [DOI] [PubMed] [Google Scholar]
- 5.Anderson D E, Mcneely J D, Windham B G. Regular slow-breathing exercise effects on blood pressure and breathing patterns at rest. J Hum Hypertens. 2010;24(12):807–813. doi: 10.1038/jhh.2010.18. [DOI] [PubMed] [Google Scholar]
- 6.Elliott W J, Izzo J L. Device-guided breathing to lower blood pressure: case report and clinical overview. MedGenMed. 2006;8(3):23. [PMC free article] [PubMed] [Google Scholar]
- 7.Joseph C N, Porta C, Casucci G, et al. Slow breathing improves arterial baroreflex sensitivity and decreases blood pressure in essential hypertension. Hypertension. 2005;46(4):714–718. doi: 10.1161/01.HYP.0000179581.68566.7d. [DOI] [PubMed] [Google Scholar]
- 8.Howorka K, Pumprla J, Tamm J, et al. Effects of guided breathing on blood pressure and heart rate variability in hypertensive diabetic patients. Auton Neurosci. 2013;179(1/2):131–137. doi: 10.1016/j.autneu.2013.08.065. [DOI] [PubMed] [Google Scholar]
- 9.Chang Qinghua, Liu Renguang, LI Changjun, et al. Effects of slow breathing rate on blood pressure and heart rate variabilities in essential hypertension. Int J Cardiol. 2015;185(1):52–54. doi: 10.1016/j.ijcard.2015.02.105. [DOI] [PubMed] [Google Scholar]
- 10.van Hateren K J, Landman G W, Logtenberg S J, et al. Device-guided breathing exercises for the treatment of hypertension: An overview. World J Cardiol. 2014;6(5):277–282. doi: 10.4330/wjc.v6.i5.277. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 11.Diao Ziji, Liu Hongying, Zhu Lan, et al. Therapeutic hypertension system based on a microbreathing pressure sensor system. Med Devices (Auckl) 2011;4:51–57. doi: 10.2147/MDER.S19971. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 12.黄戎, 何红梅, 皮喜田, 等. 基于生物反馈的便携式高血压治疗仪的研究. 生物医学工程学杂志. 2014;(3):586–589. [Google Scholar]
- 13.Landman G W, Drion I, van Hateren K J, et al. Device-guided breathing as treatment for hypertension in type 2 diabetes mellitus: a randomized, double-blind, sham-controlled trial. JAMA Intern Med. 2013;173(14):1346–1350. doi: 10.1001/jamainternmed.2013.6883. [DOI] [PubMed] [Google Scholar]
- 14.Hering D, Kucharska W, Kara T, et al. Effects of acute and long-term slow breathing exercise on muscle sympathetic nerve activity in untreated male patients with hypertension. J Hypertens. 2013;31(4):739–746. doi: 10.1097/HJH.0b013e32835eb2cf. [DOI] [PubMed] [Google Scholar]
- 15.Fiamma M N, Samara Z, Baconnier P, et al. Respiratory inductive plethysmography to assess respiratory variability and complexity in humans. Respir Physiol Neurobiol. 2007;156(2):234–239. doi: 10.1016/j.resp.2006.12.001. [DOI] [PubMed] [Google Scholar]
- 16.Robles-Rubio C, Bertolizio G, Brown K, et al. Scoring tools for the analysis of infant respiratory inductive plethysmography signals. PLoS One. 2015;10(7):e0134182. doi: 10.1371/journal.pone.0134182. [DOI] [PMC free article] [PubMed] [Google Scholar]