Impfungen sind auch für explizit dermatologische Indikationen wie Herpes zoster und HPV-Infektionen verfügbar. Der Einsatz von Systemtherapien kann mit erhöhten Risiken für Infektionskrankheiten vergesellschaftet sein, sodass bestimmte Vakzinierungen - wie die Zosterimpfung - besonders wichtig sind.
Impfungen erleben eine Renaissance, da uns die Corona-Pandemie vor Augen geführt hat, dass Infektionen durch Impfungen beherrschbar sind. Grund genug, Impfungen in dermatologischen Indikationen zu besprechen.
Herpes zoster
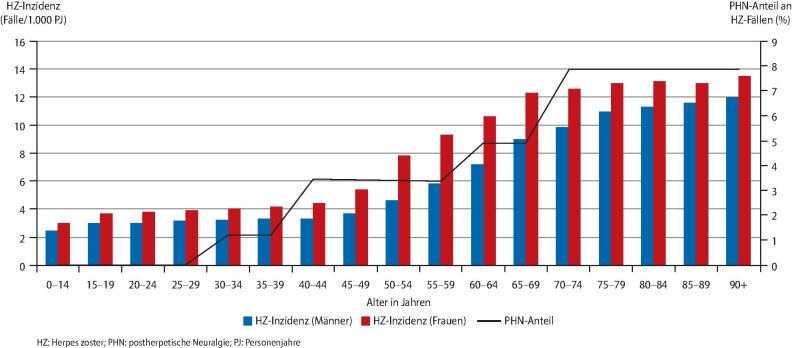
Etwa ein Drittel der in Deutschland lebenden Menschen erkrankt im Laufe ihres Lebens an Herpes zoster [1]. Die Zahl der Fälle von Herpes zoster wird auf 400.000 pro Jahr geschätzt [2]. 10-30 % der Erkrankten entwickeln eine Post-Zoster-Neuralgie (PZN) und 10-25 % weisen Sehstörungen oder Sehverlust bei Zoster ophthalmicus auf. Eine weitere mögliche Komplikation ist Hörverlust. Innerhalb der ersten zwölf Monate nach der Infektion bestehen erhöhte Risiken für Myokardinfarkt und Apoplex [3]. Die Inzidenz des Herpes zoster steigt mit zunehmendem Lebensalter deutlich an, insbesondere in der Altersgruppe der 50- bis 70-Jährigen. Die Inzidenz der PZN steigt insbesondere ab dem Alter von 70 Jahren an [2, 4], wie in Abb. 1 zu sehen ist.
Erwachsene mit Asthma, chronisch obstruktiver Lungenerkrankung, Depressionen und rheumatoider Arthritis zeigen ein durchschnittlich 30 % höheres Risiko für Herpes zoster. Chronisch-entzündliche und Autoimmunerkrankungen gehen mit einem erhöhten Risiko eines Herpes zoster einher [5], darunter auch Psoriasis, Pemphigus, bullöses Pemphigoid, Lupus erythematodes und Dermatomyositis (Abb. 2).
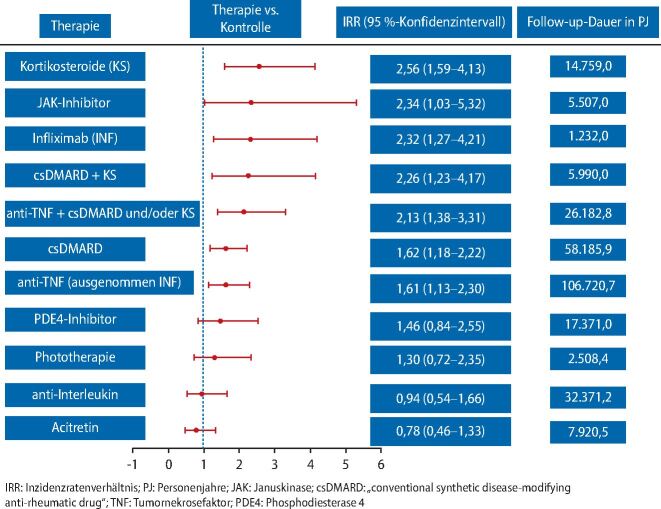
Darüber hinaus erhöhen immunsupprimierende und -modulierende Erkrankungen signifikant das Zosterrisiko. Forschende untersuchten in einer Metaanalyse [6] das Herpes-zoster-Risiko bei Psoriasis und Psoriasis-Arthritis unter Therapie. Dabei zeigten sich bei fast allen Therapien erhöhte Inzidenzraten für Herpes zoster, wobei Kortikosteroide, Januskinase(JAK)-Inhibitoren, Infliximab, krankheitsmodifizierende antirheumatische Medikamente ("disease-modifying anti-rheumatic drug", DMARD) plus Kortikosteroide und Anti-Tumornekrosefaktor (anti-TNF) plus DMARD oder Kortikosteroide besondere Treiber des Risikos für einen Herpes zoster sind (Abb. 3).
Registerdaten des RABBIT (deutsches Register zur Langzeitbeobachtung der Therapie mit Biologika, Biosimilars und JAK-Inhibitoren bei erwachsenen Patienten mit rheumatoider Arthritis) weisen leicht erhöhte Event-Rates für Herpes zoster unter verschiedenen der aufgeführten Medikamentenklassen aus [7], insbesondere wird jedoch eine deutliche Erhöhung unter JAK-Inhibitoren evident (Abb. 4).
Interessanterweise können auch Statine, also Medikamente ohne direkte immunsuppressive Wirkung, das Risiko für einen Herpes zoster erhöhen. In einer Analyse zeigte sich [8], dass sich mit der Einnahmezeit von Statinen über die Jahre das relative Risiko im Vergleich zu Nicht-Statin-Nutzern immer weiter erhöht und bei zehnjähriger Einnahme 4,2 % höher liegt.
Vor dem Hintergrund dieser Erkenntnisse ist die Impfrate von etwa 6 % bei über 60-Jährigen als sehr gering anzusehen und es besteht ein hohes Potenzial, durch die Steigerung der Impfraten die Inzidenz des Herpes zoster deutlich abzusenken. In der Dermatologie muss vor dem Hintergrund moderner immunsuppressiver oder immunmodulierender Therapien die iatrogen erhöhte Inzidenz des Herpes zoster bereits im Vorfeld geplanter Therapien berücksichtigt werden.
Impfstoffe und Nebenwirkungen
Es stehen zwei Herpes-zoster-Impfstoffe zur Verfügung. Der Lebendimpfstoff Zostavax® wird von der Ständigen Impfkommission (STIKO) aufgrund der eingeschränkten Wirksamkeit und seiner begrenzten Wirkdauer nicht für die Standardimpfung empfohlen. Darüber hinaus ist er nicht zur Impfung von immunsupprimierten Personen geeignet. Die nachfolgenden Erläuterungen beziehen sich deshalb auf den rekombinanten, adjuvantierten Zoster-Totimpfstoff Shingrix®. Dieser wird in zwei Impfdosen im Abstand von mindestens zwei und höchstens sechs Monaten in den Musculus deltoideus injiziert. Eine Koadministration mit dem Influenzaimpfstoff, dem 23-valenten Pneumokokken-Polysaccharid-Impfstoff und dem Tdap-Impfstoff (Tetanus-, Diphtherie-, azellulärer Pertussisimpfstoff) ist möglich.
Der Impfstoff ist für Personen ab 50 Jahren beziehungsweise ab 18 Jahren bei Personen mit erhöhtem Herpes-zoster-Risiko zugelassen. Die STIKO empfiehlt die Impfung als Standardimpfung für Menschen ab 60 Jahren, ferner als Indikationsimpfung für Personen ab 50 Jahren mit erhöhtem Risiko für Herpes zoster. Dazu gehören Patienten mit HIV-Infektion, mit chronisch-entzündlichen- und Autoimmunkrankheiten sowie Personen unter Immunsuppression. Auch Patienten mit chronisch-obstruktiven Lungenerkrankungen oder Asthma bronchiale, chronischer Niereninsuffizienz oder Diabetes mellitus werden in diesem Zusammenhang genannt.
Die Wirksamkeit der Impfung wurde in mehreren großen Studien (ZOE-50/ZOE-70) untersucht. Dabei zeigten sich in allen Altersklassen eine Wirksamkeit von über 90 % [9, 10, 11].
Nach der Impfung treten Lokalreaktionen in Form von Schmerzen, Rötung und Schwellung auf. Schmerzen wurden in Studien von gut 70-80 % der Probanden angegeben. Systemische Reaktionen waren Erschöpfung, Fieber, Kopfschmerzen, Myalgie und Schüttelfrost. Schwerwiegende unerwünschte Ereignisse oder Todesfälle in Studienkollektiven unterschieden sich nicht von Placebo. Langzeitnebenwirkungen wurden bislang nicht registriert.
Wissenswertes zur Impfung
Die Impfung gegen Herpes zoster ist eine der wichtigsten Impfungen in der Dermatologie wegen Immunseneszenz und damit erhöhtem Zosterrisiko älterer Menschen, der stark beeinträchtigenden Langzeiteffekte und wegen der zunehmenden Bedeutung immunologisch kompromittierender Systemtherapien. Unsicherheiten wie der Glaube, eine Impfung reiche aus, oder Ängste vor Impfkomplikationen bedingen die erschreckend niedrige Impfrate insbesondere bei der zweiten Impfung. Die Impfung nach durchgemachter Zostererkrankung ist bei einem Rezidivrisiko von fast 10 % für das erste Zosterrezidiv besonders wichtig - auch bei der Impfung nach Herpes zoster wird der Vollschutz erst nach zwei Impfungen erreicht.
Häufig gestellte Fragen zur Herpes-zoster-Impfung und Antworten darauf:
Wie lange hält der Impfschutz vor? Die bislang gemessene Immunantwort persistiert über zehn Jahre, nach mathematischer Modellierung bis 20 Jahre. Eine Auffrischimpfung (Einzelimpfung) kann nach zehn Jahren erfolgen; eine weitere Auffrischimpfung ist nicht erforderlich.
Muss eine Person nach durchgemachter Herpes-zoster-Infektion noch geimpft werden? Ja, eine durchgemachte Erkrankung schützt nicht davor, erneut zu erkranken.
Reicht nach durchgemachtem Herpes zoster eine Impfdosis? Nein, der Vollschutz besteht erst nach zwei Dosen.
Wann ist der optimale Zeitpunkt zur Impfung nach Herpes zoster? Nachdem die akute Erkrankung und die Zostersymptome abgeklungen sind. Die Datenlage zum günstigsten Zeitpunkt ist bislang begrenzt.
Humane Papillomviren
Humane Papillomviren (HPV) sind unbehüllte DNA-Viren [12]. Mittlerweile sind rund 200 HPV-Genotypen nachgewiesen worden, von denen mehr als 10 % onkogenes Potenzial aufweisen. HPV-infektionen sind die häufigsten sexuell übertragbaren Infektionen (STI) weltweit und werden für rund 5 % der Karzinome verantwortlich gemacht, zum Beispiel für Zervix- und oropharyngeale Karzinome.
Der deutsche Forscher Harald zur Hausen postulierte bereits 1976, dass HPV eine Bedeutung bei der Entstehung des Zervixkarzinoms zukommt [13]. Durch Isolation der HPV-Typen 16 und 18 aus Zervixtumoren in den 1980er Jahren wurde diese Hypothese untermauert und später durch entsprechende pathogenetische Untersuchungen bewiesen. Die Entwicklung eines Impfstoffs, die im Jahre 2006 beendet werden konnte, eröffnete damit nicht nur eine Möglichkeit, Infektionen zu verhindern, sondern auch die dadurch hervorgerufenen Tumoren. Das Zervixkarzinom war zu dieser Zeit der dritthäufigste maligne Tumor bei Frauen.
Für die Entstehung des Gebärmutterhalskrebses wurden inzwischen eine Reihe Hochrisikotypen identifiziert, unter anderem HPV 16, 18, 31 und 45 (Tab. 1). HPV 16 ist in 50-60 % und HPV 18 in 10-20 % der Zervixkarzinome nachweisbar. Die Bedeutung von Hochrisiko-HPV-Typen ist in Tab. 2 dargestellt.
| Lokalisation des Karzinoms | Von der IARC als karzinogen klassifizierte Hochrisiko-HPV-Typen | |
|---|---|---|
| Klassifikation mit ausreichender Evidenz | Klassifikation mit limitierter Evidenz | |
| Mundhöhle | HPV 16 | HPV 18 |
| Tonsillen | HPV 16 | - |
| Pharynx | HPV 16 | - |
| Larynx | - | HPV 16 |
| Anus | HPV 16 | HPV 18, 33 |
| Penis | HPV 16 | HPV 18 |
| Vulva | HPV 16 | HPV 18, 33 |
| Vagina | HPV 16 | - |
| Cervix uteri | HPV 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59 | HPV 26, 53, 66, 67, 68, 70, 73, 82 |
nach [21]
| Tumor | Häufigkeit in % |
|---|---|
| Zervixkarzinom | 100 |
| Analkarzinom | 95 |
| Oropharyngealkarzinom | 70 |
| Vaginalkarzinom | 65 |
| Vulvakarzinom | 50 |
| Peniskarzinom | 35 |
nach [22]
Die eigentlichen Wirtszellen von HPV sind Keratinozyten. Virale E6- und E7-Proteine blockieren in den Zellen die Auslösung der Apoptose, solange die Virusreplikation läuft. Ist die Replikation abgeschlossen, gehen die Wirtszellen in den programmierten Zelltod, Viren werden freigesetzt und können benachbarte Zellen infizieren. Diese Vorgänge können vom Immunsystem nur schlecht detektiert werden.
Das primäre Ziel der Impfung gegen HPV war bei Aussprechen der Impfempfehlung durch die STIKO im Jahre 2007 eine Reduktion der Krankheitslast durch den Gebärmutterhalskrebs. Die Impfempfehlung richtete sich damals an "alle Mädchen im Alter von zwölf bis 17 Jahren". Im Vordergrund stand damals die jährliche Erkrankungsrate von 6.500 erkrankten Frauen und 1.660 Todesfällen.
Mittlerweile wurden die Empfehlungen angepasst und auf Jungen ausgeweitet. Bei Männern zählen das Penis- und Analkarzinom sowie Plattenepithelkarzinome der Mundhöhle und des Rachens zu den HPV-assoziierten Krebsarten. Basierend auf Zahlen zu Krebsneuerkrankungen des Zentrums für Krebsregisterdaten am Robert-Koch-Institut (RKI) treten beim Mann pro Jahr etwa 600 Anal- und mindestens 250 Peniskarzinome sowie mindestens 750 Karzinome in der Mundhöhle und/oder im Rachen als Neuerkrankungen auf, die mit einer HPV-Infektion assoziiert sind. Die STIKO empfiehlt deshalb seit 2018 die Impfung gegen HPV für Mädchen und Jungen im Alter von neun bis 14 Jahren. Eine Immunisierung sollte vor dem ersten Sexualkontakt erfolgen [14].
Impfstoffe und Nebenwirkungen
Derzeit sind zwei HPV-Impfstoffe in Deutschland zugelassen [15], ein bivalenter Impfstoff (Cervarix® gegen HPV 16 und 18) und ein nonavalenter Impfstoff (Gardasil® 9, gegen HPV 6, 11, 16, 18, 31, 33, 45, 52 und 58).
Der nonavalente Impfstoff wird in den Musculus deltoideus oder den oberen anterolateralen Bereich des Oberschenkels injiziert. Im Alter von neun bis einschließlich 14 Jahren werden zwei Impfdosen im Abstand von mindestens sechs und maximal zwölf Monaten verabreicht, bei Personen ab 15 Jahren hingegen drei Dosen im Abstand von zwei sowie sechs Monaten zur Erstimpfung. Eine Koadministration mit dem Tdap-Impfstoff, dem Td-IPV-Impfstoff (Tetanus-, Diphtherie-, inaktivierter Polio-Viren-Impfstoff) und dem Tdap-IPV-Impfstoff ist möglich.
Lokale Nebenwirkungen sind sehr häufig Schmerzen, Schwellung und Erythem an der Injektionsstelle. Als systemische Nebenwirkungen kommen Kopfschmerzen (sehr häufig), Schwindel, Übelkeit, Fieber und Abgeschlagenheit (häufig) vor.
Für die Wirksamkeit des nonavalenten Impfstoffs liegen Daten über einen Zeitraum von über zehn Jahren für Mädchen und Jungen vor, die zum Zeitpunkt der Impfung zwischen neun und 15 Jahre alt waren. Abhängig vom HPV-Typ waren 81-98 % der Probanden seropositiv [16].
Niedrigeres Zervixkarzinomrisiko
Es stellt sich nunmehr die Frage, welche direkten Wirkungen die Impfung auf die Inzidenz des Zervixkarzinoms nimmt (Abb. 5). In diesem Zusammenhang wurden Registerdaten aus Schweden im Rahmen einer Kohortenstudie über einen Zeitraum von elf Jahren analysiert [17]. Die Mädchen und Frauen waren zwischen zehn und 30 Jahre alt und wurden auf Zervixkarzinome bis zu ihrem 31. Geburtstag evaluiert. Von 1.672.983 in die Studie einbezogenen Mädchen und Frauen erhielten 527.871 mindestens eine HPV-Impfdosis, davon 438.939 vor ihrem 17. Lebensjahr.
Unter den Frauen, die keine HPV-Impfung erhalten hatten, wurde in 538 Fällen ein Zervixkarzinom diagnostiziert (Inzidenzrate [IR]: 5,27/100.000 Personenjahre [PJ]). Bei geimpften Frauen erhielten 19 die Diagnose Zervixkarzinom (IR: 0,73/100.000 PJ). Unter diesen 19 Betroffenen befanden sich zwei Frauen, die vor ihrem 17. Lebensjahr geimpft worden waren (IR: 0,10/100.000 PJ).
Die Auswertung zeigte nach Bereinigung aller Kovariaten:
Das Risiko für ein Zervixkarzinom war bei Frauen, die bei der HPV-Impfung jünger als 17 Jahre alt waren, um 88 % niedriger als bei Frauen, die keine Impfung erhalten hatten, mit einem adjustierten Inzidenzratenverhältnis (IRR) von 0,12. (95 %-Konfidenzintervall [95 %-KI]: 0,00-0,34)
Bei Frauen, die im Alter von 17 bis 30 Jahren geimpft wurden, lag das adjustierte IRR bei 0,47 (95 %-KI: 0,27-0,75); die Risikoreduktion für ein Zervixkarzinom betrug demnach 53 %.
Wissenswertes zur Impfung
Trotz des großen Benefits der in vielen Ländern freiwilligen Impfung wird die angestrebte Impfquote von 90 % zum Aufbau einer Herdenimmunität deutlich verfehlt. Durch die Corona-Pandemie hat die Impfquote in verschiedenen Ländern in unterschiedlichem Maße abgenommen.
Eine Frage, die häufig gestellt wird, ist die, ob Personen über 17 Jahren noch von der Impfung profitieren können. Dies lässt sich ganz klar bejahen. Die Wirksamkeit der Impfung ist jedoch bei nicht HPV-naiven Personen reduziert. Außerdem muss die Kostenübernahme individuell geklärt werden.
Ob die HPV-Impfung auch gegen bereits bestehende HPV-Infektionen wirkt, lässt sich hingegen nicht mit Sicherheit beantworten. Während Impfstoffhersteller behaupten, die Impfung habe "keinen Effekt auf HPV-Infektionen oder bereits bestehende klinische Erkrankungen", zeigen Fallberichte und persönliche Erfahrungen bei Patienten mit hartnäckig therapierefraktären Hand- und Fußwarzen etwas anderes. Deutsche Forschende haben bereits 2015 Daten von sechs Kindern mit therapierefraktären palmaren und plantaren Warzen publiziert, die mit einem Dreier-Impfschema des damals verfügbaren quadrivalenten HPV-Impfstoffes geimpft wurden. Alle sechs behandelten Kinder waren nach der Impfung warzenfrei [18]. Weitere Arbeiten sprechen ebenfalls für eine Wirksamkeit, etwa eine unverblindete Studie mit 45 Patienten [19], bei der in etwa 70 % der Fälle eine komplette oder partielle Heilung durch die Impfung erzielt werden konnte, oder eine retrospektive Übersichtsstudie mit 26 Patienten [20], bei der es in rund zwei Dritteln der Fälle zu einer kompletten oder partiellen Heilung nach der HPC-Impfung kam.
Prof. Dr. med. Thomas Dirschka.
CentroDerm GmbH
Heinz-Fangman-Straße 57
42287 Wuppertal
t.dirschka@centroderm.de
SpringerMedizin.de.
Weitere interessante Artikel zum Thema Impfungen in der Dermatologie
...finden Sie auf SpringerMedizin.de bei Eingabe der Artikelnamen in die Suchleiste.
Warum Impfen Bestandteil Ihres Praxisalltags sein sollte
HPV und Krebsprävention
Bedeutung der prophylaktischen HPV-Vakzine für die Dermatologie und Venerologie
Zosterimpfung unter Biologikatherapie
Impfungen in der Dermatologie
Hautveränderungen bei COVID-19 und nach COVID-19-Impfung
Impfprävention HPV-assoziierter Neoplasien
Supplementary Information
Associated Data
This section collects any data citations, data availability statements, or supplementary materials included in this article.