Basierend auf den Arbeiten von Walter Dandy (1886-1946) zur Pneumoenzephalographie [1] entwickelte der portugiesische Neurologe Egaz Moniz (1874-1955) eine neue Technik zur indirekten Darstellung von Gehirntumoren mit Hilfe von Kontrastmitteln. Seine Überlegungen basierten auf der Annahme, dass eine einfache Lokalisation intrakranieller Läsionen durch die röntgenologische Darstellung der von ihnen hervorgerufenen Deformierungen der zentralen Gehirnstrukturen, wie etwa der Ventrikel oder der Blutgefäße, möglich sein sollte. Zur Darstellung feinster Strukturen auf Röntgenaufnahmen hatten sich ölige Jodverbindungen als besonders gut erwiesen. Das vom französischen Neurologen und Radiologen Jean-Athanase Sicard (1872-1929) erstmals 1921 zur Myelographie und Ventriculographie erfolgreich eingesetzte Kontrastmittel Lipiodol, ein 1901 von Marcel Guerbet (1861-1938) an der Pariser Hochschule für Pharmazie synthetisiertes ethiodiertes Mohnöl, konnte jedoch nicht für arterielle Anwendungen benutzt werden. Bei der Suche nach einem geeigneten Kontrastmittel für die Arteriographie erwiesen sich bald thoriumhaltige Suspensionen als besser verträgliche, ausgezeichnet schattengebende und weniger gefährliche Substanzen. 1929 setzte der portugiesische Chirurg Reynaldo Dos Santos (1880-1970) gemeinsam mit seinen Mitarbeitern Alfonso Lamas und J. Peireira Caldas diese Suspensionen erstmals erfolgreich zur abdominellen Aortographie ein [2].
Vor 90 Jahren, am 14. Oktober 1931 machte Moniz das erste zerebrale Arteriogramm unter Verwendung des neuen Kontrastmittels Thorotrast. „Seitdem es uns mit dem Thorotrast, das wir in die Technik der Enzephaloarteriographie eingesetzt haben, gelungen ist, auch das Venennetz des Gehirns, die großen Venen und die Sinus der Dura sichtbar zu machen und bildlich darzustellen, hat die arteriographische Erforschung des Gehirns an Bedeutung gewonnen“ [3]. Im Anschluss leistete Moniz Pionierarbeit bei der Anwendung und Einführung von Thorotrast für das neue Feld der Angiographie des Gehirns. Thorotrast erwies sich schnell als bestmögliches Kontrastmittel mit hervorragender Bildqualität für die zerebrale Angiographie. Sie bildete dabei vornehmlich die Grundlage für die Diagnose und Lokalisierung von Hirntumoren. Bis Mitte der 1950er Jahre wurde Thorotrast deshalb weltweit hauptsächlich für die Anwendung in der Arteriographie und Venographie eingesetzt.
Seit den frühen Anwendungen der Röntgenstrahlen in der Medizin wurde versucht, auch Gefäße, Hohlräume und Organe mit Hilfe von Kontrastmitteln im Röntgenbild sichtbar zu machen. Dabei wurden fast alle Elemente mit höherem Atomgewicht und deren Verbindungen auf ihren Nutzen hin überprüft. Nur wenige Substanzen haben Eingang in die radiologische Diagnostik gefunden. Hierzu zählten u.a. das für die Magen- und Darmdiagnostik 1904 von Hermann Rieder (1858-1932) in München verwendete in Grießbrei aufgelöste Wismutkarbonat oder die von C. Bachem und H. Günther 1910 verwendeten Bariumsalze der Schwefelsäure (Bariumsulfat). 1921 setzten die beiden französischen Ärzte Jacques Forestier (1890-1978) und Jean-Athanase Sicard (1872-1929) ein ethiodiertes Öl bestehend aus Jod in Verbindung mit Ethylestern von Fettsäuren des Mohnöls für die Myelographie ein. Dieses Öl wurde später unter dem Namen Lipiodol vermarktet.
Auf der Suche nach weiteren Kontrastmitteln mit besonderen physikalisch-chemischen Eigenschaften, die, bestehend aus negativ geladenen Teilchen, ein positiv geladenes kolloidales Kontrastmittel an der Wand des Schleimhautgewebes zum Ausflocken bringen können, um so eine bessere Reliefdarstellung zu ermöglichen, wurden unter Leitung von Karl Frik (1878-1944) am Werner Siemens Institut für Röntgenforschung im städtischen Krankenhaus Moabit einige der bei der Chemischen Fabrik Von Heyden in Radebeul, Sachsen entwickelten Kolloide für ihre Eignung als Röntgen-Kontrastmittel klinisch getestet. Heyden war führend auf dem Gebiet der industriellen kolloidchemischen Forschung und stellte Kolloide im technischen Maßstab her. Das Unternehmen leistete auf diesem Gebiet Pionierarbeit. Die bei von Heyden hergestellte kolloidale Form einer Reihe von chemischen Elementen (z.B. Silber, Gold, Eisen und Schwefel) und später auch chemischer Verbindungen (z. B. Silberchlorid und Kieselsäure) wurden unter anderem bereits auch im medizinischen Bereich eingesetzt. In den 1920er Jahren erweiterte von Heyden seine kolloidchemische Forschung auf Metalloxide wie Titanoxid, Eisenoxid, Chromoxid und Thoriumdioxid.
In Zusammenarbeit mit Herbert Freundlich (1880-1941), dem Leiter der kolloidchemischen Abteilung des Kaiser-Wilhelm-Instituts für Physikalische Chemie und Elektrochemie in Berlin-Dahlem, wurden am Werner Siemens Institut für Röntgenforschung weitere Elemente hoher Ordnungszahl, z.B. Silberjodid-Sol, Wismut oder Zirkoniumoxyd-Sol als mögliche neue röntgentaugliche Kontrastmittel experimentell, in Tierversuchen und auch klinisch untersucht. Das interdisziplinäre Forschungsprojekt wurde vom Magistrat der Stadt Berlin finanziell gefördert. 1928 konnte Karl Frik gemeinsam mit Theophil Blühbaum und Helmut Kalkbrenner nach eingehenden Untersuchungen Thoriumdioxydhydrosol als am besten geeignetes und alle Anforderungen erfüllendes neues Kontrastmittel identifizieren.
Thorium wird aus dem Monazit, einer Mischung von Phosphaten verschiedener Seltenerdmetalle, gewonnen. Das bei vorsichtigem Erwärmen von Thoriumoxalat auf ca. 500 °C erhaltene Oxyd wurde nach Anätzung mit Salzsäure zu einer kolloidalen Lösung. Vor Applikation des Hydrosols wurde zur Verringerung der schädlichen Wirkungen der Salzsäure die Lösung in destilliertem Wasser dialysiert. Nach erfolgreichen Tierversuchen auf Bildqualität und Toxizität wurde das neue Kontrastmittel auch an Patienten getestet. „Auf keinen Fall kann dem Thorium von dieser Seite eine schädigende Wirkung zugeschrieben werden, denn auch nach mehrmonatigem Verweilen an einer Stelle blieb das umgebende Gewebe unbeeinflußt. … Das Mittel wurde von uns monatelang bei Patienten, gelegentlich auch Schwerkranken mit peroraler, rektaler, intratrachealer und intravesikaler Einverleibung angewandt, ohne daß wir jemals unerwünschte Komplikationen zu verzeichnen hätten. Auch seitens der Klinik konnte nichts Beunruhigendes beobachtet werden. Die ersten Versuche am Menschen hatten die Aufgabe, uns über die optimale Konzentration des Mittels zu informieren.“ [4] In Ermangelung erforderlicher größerer Mengen des Kontrastmittels und des Fehlens des entsprechenden „klinischen Materials“ für umfangreiche Studien wurde beschlossen, zuerst ein Ersatzmittel für die damals zur Bronchographie verwandten Jodölpräparate zu finden. Weitere, orientierende experimentelle Versuche wurden am Magen-Darmkanal und den Nieren im Rahmen des Forschungsprojektes vorgenommen.
Nach diesen ersten, doch erfolgreich erschienenen Anwendungsversuchen begann die Geschichte der breiten weltweiten Nutzung von Thoriumdioxyden in der radiologischen Diagnostik mit ihrem Einsatz bei der direkten Darstellung von Leber und Milz. Nachdem bereits ab 1914 die indirekte Darstellung durch intraperitoneale Injektion von Luft in Magen und Dickdarm möglich war, schlugen 1929 der Internist Paul Radt (1902-1971) vom Pathologischen Institut des Krankenhauses Moabit in Berlin und Mitsutomo Oka von der Medizinischen Klinik der Kaiserlichen Universität Tokyo in Japan vor, eine kolloidale Lösung aus Thoriumdioxiden zur direkten röntgenologischen Darstellung von Leber und Milz zu verwenden [5], [6].
Unter dem Namen “Umbrathor” wurde das neue Kontrastmittel erstmals 1928 von Heyden vermarktet. Umbrathor war ein nicht stabilisiertes Thoriumdioxid-Sol mit einer positiven Ladung. Es bestand aus 25% Thoriumdioxid und hatte einen pH-Wert von 2,8 - 3. Es flockte Proteine aus, auch die des menschlichen Körpers. Die orale Verabreichung lieferte ausgezeichnete Kontrastbilder der Magenschleimhaut und des oberen Teils des Darms. Die rektale Verabreichung lieferte ein kontrastreiches, konsistentes Bild des Dickdarms. Umbrathor hatte gegenüber den bereits verwendeten bariumhaltigen Kontrastmitteln den Vorteil, dass es in einer wässrigen Lösung blieb. Zudem kam es weniger oft zu den ansonsten aufgetretenen Verstopfungen. Umbrathor konnte jedoch nicht in den Blutkreislauf injiziert werden, da es sehr säurehaltig war und empfindlich auf Proteine reagierte. Die Entwicklung und Herstellung einer alkalistabilen Form, die nicht mit Körperflüssigkeiten ausflockte, wurde Ende der 1920er Jahre im Rahmen der Auswertung der Ergebnisse und klinischen Anforderungen des Berliner Forschungsprojektes vorgeschlagen. Heyden konnte daraufhin durch Verwendung von Schutzkolloiden, wie z. B. halbkolloidale Abbauprodukte von Stärke, die erforderliche stabilisierte Form herstellen [7].
Dieses neue Produkt wurde dann ab 1931 unter dem Handelsnamen Thorotrast vermarktet. Zwischen 1928 und 1950 wurden nach Zahlen der damaligen ostdeutschen Staatlichen Zentrale für Strahlenschutz (SZS) ca. 10,07 Tonnen Thoriumdioxyd hergestellt und vertrieben [8].
„Schließlich seien noch die vor einigen Jahren geschaffenen Röntgenkontrastmittel, d. h. Mittel zur Sichtbarmachung von Körperhohlräumen mit Hilfe von Röntgenstrahlen, Umbrathor und Thorotrast, genannt. Während das erstere Präparat vorzugsweise für die Untersuchung des Verdauungskanals Verwendung findet, ist das Thorotrast für eine sehr große Zahl der verschiedensten diagnostischen Fragestellungen herangezogen worden. Die außerordentlich große Zahl von wissenschaftlichen Abhandlungen gerade über dieses Präparat hat gezeigt, daß noch zahlreiche röntgendiagnostische Probleme der Lösung harren und daß die Mithilfe des Chemikers hier besonders notwendig ist. Es sei nur nebenbei die interessante Tatsache bemerkt, daß mit Thorotrast sogar das Gefäßsystem des Gehirns dargestellt werden kann, woraus Schlüsse auf Lageveränderungen, das Vorhandensein von Geschwülsten usw. ermöglicht werden.“[9]
Von Heyden wurde 1873 als “Salicylsäurefabrik Dr. von Heyden“ als erste Fabrik zur synthetischen Herstellung der Salicylsäure nach dem Verfahren von Hermann Kolbe (1859) gegründet und erlangte auch durch die Herstellung völlig neuer Arzneistoffe und Spezialpräparate Weltruf. Vor dem Ersten Weltkrieg wurde die Herstellung von Durchleuchtungsschirmen mit hoher Leuchtkraft für Röntgenapparate und von Verstärkerfolien für Röntgenaufnahmen entwickelt [10].
In den 1930er Jahren begann die Heyden Chemical Company in New York mit der Produktion von Thorotrast. Im Jahr 1953 verkaufte Heyden seine Antibiotika-Sparte an American Cyanamid, einschließlich aller Warenzeichen, Patente, des Firmenwerts und der Geschäfte im Zusammenhang mit Thorotrast. Nach dem Verkauf führte Heyden sein Geschäft weiter, stellte aber kein Thorotrast mehr her und verkaufte es auch nicht mehr. Im Jahr 1954 verkaufte American Cyanamid seine Thorotrast-Produktlinie an Testagar and Company. (Abb. 1) 1962 wurde Testagar Teil der Fellows Medical Manufacturing Company (FMM). 1971 wurde Fellows mit FMM, Inc. verschmolzen, einer hundertprozentigen Tochtergesellschaft der Chromalloy American Corporation. Später im selben Jahr änderte FMM seinen Firmennamen in Fellows Medical Manufacturing Corporation, Inc., eine Delaware Corporation. Die Thorotrast-Produktlinie wurde nacheinander an jedes neue Unternehmen weitergegeben, das seinerseits das Medikament herstellte und vertrieb [11]. In Radebeul wurde von Heyden 1951 als VEB Arzneimittelwerk Dresden weitergeführt. 2000 ging das Unternehmen an Degussa und 2004 an Hexal Syntech und produziert seit 2007 unter Arevipharma GmbH weiterhin pharmazeutische Wirkstoffe [12].
Abbildung 1.
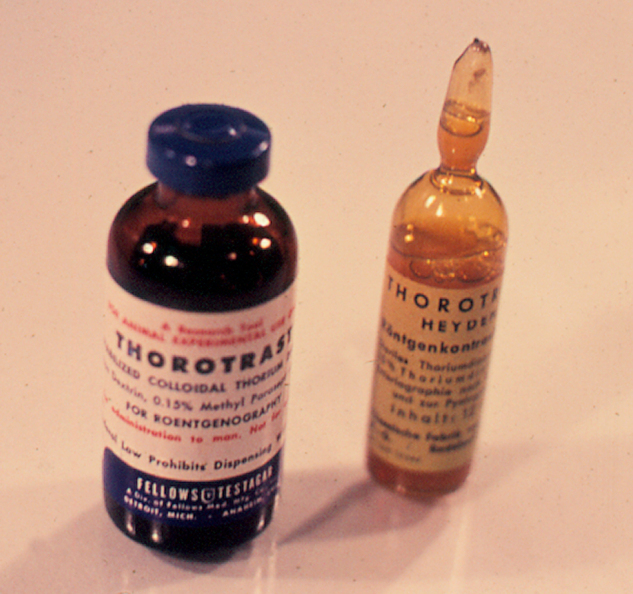
Thorotrast-Ampullen der Firmen von Heyden Radebeul (re) und Testagar & Co., Inc., Detroit, Michigan, USA (li).
Für Umbrathor und Thorotrast wurde ausschließlich das natürlich vorkommende Radioisotop Thorium-232 verwendet. Die Radioaktivität von Thorium wurde 1898 von Marie Curie (1867-1934) und dem deutschen Chemiker Gerhard Schmidt (1865-1949) zeitgleich entdeckt. Das langlebige Radioisotop mit einer Halbwertszeit von 1,4×1010 Jahren trägt durch die Energiebilanz bei seinem Zerfall hauptsächlich zur Erdwärme bei. Es zerfällt unter vornehmlicher Aussendung von Alpha-Strahlung (zu ca. 95%) in mehreren Schritten in stabiles Blei-208. Zwischenprodukte sind u.a. Radium-228 (Halbwertszeit 5,75 a), Actinium-228 (6,15 h), Radon-220 (55,6 s), Polonium-216 (0,145 s), Blei-212 (10,6 h) und Wismut-212 (60,55 min).
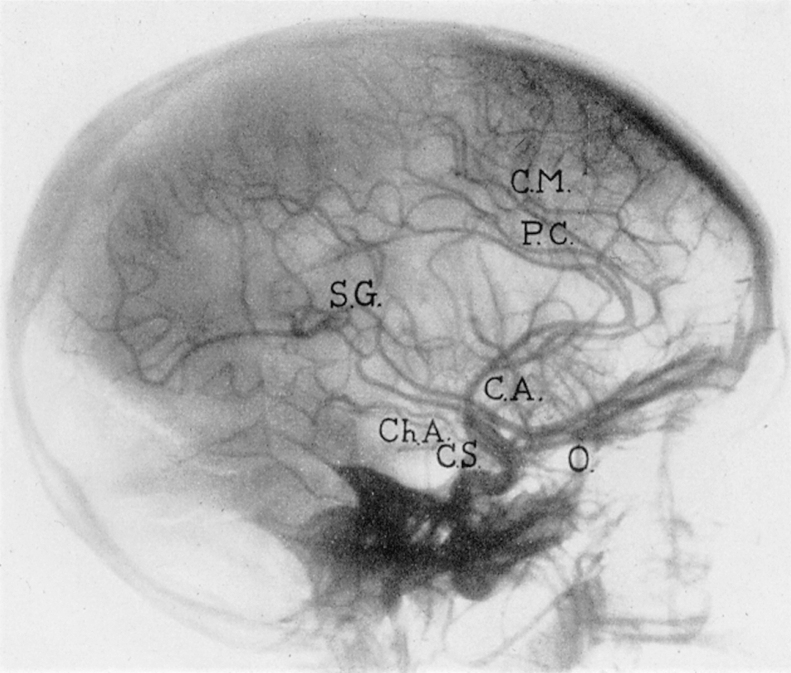
Die wässrige Suspension von 25% kolloidalem Thoriumdioxid (ThO2) erzeugt aufgrund der hohen Ordnungszahl (Z = 90) und des hohen Absorptions-Wirkungsquerschnitts eine große Opazität für Röntgenstrahlen und damit sehr kontrastreiche Bilder. Das Kontrastmittel zeigte im Vergleich zu den damals verfügbaren Alternativen praktisch keine unmittelbaren Nebenwirkungen. Thorotrast erwies sich somit als ideales, für die Zeit alternativloses Röntgenkontrastmittel für Darstellungen von Hohlräumen und engen Gefäßen. Es konnte sowohl intravenös als auch intraarteriell appliziert werden. Die Applikation von Thorotrast erfolgte bei etwa 70% der Patienten und Patientinnen als Injektion in die Halsschlagader und bei 30% in die Arterien der Beine oder der Arme. Nach der Injektion von durchschnittlich 25 ml Thorotrast, das 5 g Thorium mit einer Aktivität von 0,5 μCi bzw. 18,5 kBq 232-Th und additiv weiterer Zerfallsprodukte enthielt [13], in die Arteria carotis konnten besonders kontrastreiche Bilder des Gehirns (arterielle Enzephalographie) gewonnen werden.(Abb. 2) Bei der Aortographie der Extremitäten wurden herkömmlich 20 ml in die entsprechenden Gefäße injiziert.
Abbildung 2.
Normale zerebrale Angiographie mit Thorotrast.
Nach intravaskulärer Injektion wird der größte Teil des Thorotrasts von Makrophagen aufgenommen und in Körpergewebe transportiert. Dort verbleibt es in aggregierter, unaufgelöster Form. Die Ausscheidungsquote ist sehr gering und wird auf 0,09-0,16% pro Jahr geschätzt, was einer biologischen Halbwertszeit, in der 50 Prozent des verabreichten Thoriumdioxids durch biologische Prozesse abgebaut bzw. aus dem Körper ausgeschieden werden, von 430-770 Jahren entspricht. Die Anreicherung im Körper findet vornehmlich in der Leber (59%), in der Milz (29%), dem roten Knochenmark (9%), im kalzifizierten Knochen (2,4%), in der Lunge (0,7%) und in den Nieren (0,1%) statt [14].
Bei dem durchschnittlich intravaskulär injizierten Thorotrast-Volumen von 25 ml ergeben sich bei einer 70 kg schweren Person Energiedosisleistungen von 25 cGy/Jahr in der Leber; 70 cGy/Jahr in der Milz; 9 cGy/Jahr im Knochenmark; 0,6 cGy/Jahr in der Endothelschicht im Knochen; 0,4 cGy/Jahr in den Nieren. Die Strahlendosis im Lungengewebe wird hauptsächlich durch das Tochterprodukt Radon-220 verursacht, das mit der Atemluft ausgeatmet wird. Für die Strahlenexposition der Leber ergibt sich bei einer über 40jährigen Kumulation eine mittlere Dosis von 9,8 Gy [15].
Seit der Einführung von Thorotrast 1931 wurden bis Mitte der 1950er Jahre weltweit etwa 2 bis 10 Millionen Patienten und Patientinnen Thorotrast injiziert. Das Haupteinsatzgebiet war die Angiographie, insbesondere die Carotisangiographie, d.h. ca. 90% der betroffenen Patienten und Patientinnen erhielten Thorotrast mit dieser Indikationsstellung.
Da Thorium-232 und seine Folgeprodukte aufgrund der langen physikalischen und biologischen Halbwertszeiten lebenslang im menschlichen Körper deponiert werden, zeigten sich nach einer Latenzzeit von mehr als 15 Jahren zunehmend eine Reihe von vorwiegend stochastischen Spätschäden. Die Symptomatik wird allgemein pauschalisierend als „Thorotrastose“ bezeichnet. Bei der selektiven Anreicherung von Thorium-232 im Parenchym des retikuloendothelialen Systems, d.h. vor allem in Leber, Milz und Lymphknoten, waren Auswirkungen vor allem in diesen Organbereichen zu erwarten [16]. Abbildung 3, Abbildung 4
Abbildung 3.
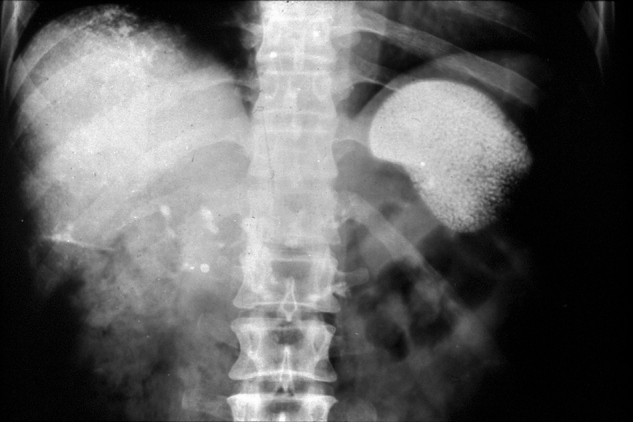
Abdomenübersichtsaufnahme mit Thorotrast-Ablagerungen in Leber, Milz und abdominalen Lymphknoten.
Abbildung 4.
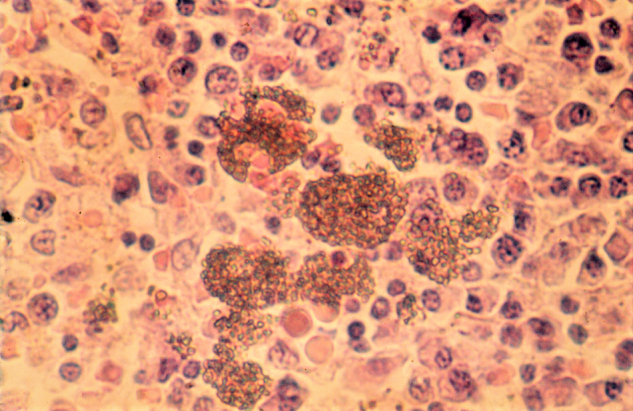
Thorotrast-Partikel im histologischen Schnitt.
Zur Untersuchung der Spätfolgen wurden mehre Studien unternommen. Die zwischen 1968 und 2016 durchgeführte, größte retrospektive deutsche Langzeit-Kohortenstudie umfasste 2326 Thorotrast-Patienten und -Patientinnen und 1890 Patienten und Patientinnen einer angepassten Kontrollgruppe. Mithilfe epidemiologischer Erhebungen sowie klinischer, radiologischer und biophysikalischer Untersuchungen wurden die Spätfolgen insbesondere in Bezug auf die Krebsentstehung untersucht. (Abbildung 1, Abbildung 2, Abbildung 3, Abbildung 4, Abbildung 5, Abbildung 6)
Abbildung 5.

Oberbauch-CT bei einem Thorotrastpatienten. Deutlich hyperdense Milz durch diffuse ThO2-Ablagerungen. In der Leber sieht man an einigen Stellen unscharfe Verdichtungen durch Thorotrastanreicherungen. Der wichtigste Befund ist der hypodense Herd im dorsalen Teil des rechten Leberlappens als Ausdruck eines neoplastischen Prozesses.
Abbildung 6.

Zustand nach Carotisangiographie mit Thorotrastparavasat entlang der Arteria carotis 30 Jahre nach der Injektion.
Es zeigte sich, dass das hepatische Angiosarkom trotz seines normalerweise eher seltenen Vorkommens das auffälligste Thorotrast-bedingte Neoplasma war. Zahlenmäßig häufiger waren jedoch das cholangiozelluläre und hepatozelluläre Karzinom der Leber. Für die Neoplasien der Leber ergab sich – jedenfalls in der deutschen Thorotraststudie – eine Korrelation zwischen Häufigkeit und mittlerer Organdosisleistung. (Abb. 5)
Auch die Zahl der Lebercirrhosen war im Vergleich zur Normalbevölkerung deutlich erhöht. In der Milz zeigten sich erstaunlicherweise keine neoplastischen Veränderungen, obwohl die Thorostrastdichte hier deutlich höher ist als in der Leber. Das Gleiche gilt auch für die dicht anreichernden abdominalen Lymphknoten. Eine deutliche Excessrate wurde für verschiedene Formen von Leukämien beobachtet. Sie lässt sich sehr wahrscheinlich auf die ThO2-Ablagerungen im Knochenmark zurückführen. Die Thorotrast-Patient*innen atmen kontinuierlich das aus den ThO2-Depots stammende radioaktive Gas Radon-220 aus. Obwohl daraus eine regelmäßige radioaktive Belastung des Lungengewebes resultiert, konnte keine Excessrate bei den betroffenen Patienten nachgewiesen werden. Die dichtesten Anreicherungen von ThO2 ergeben sich bei sogenannten „Thorotrast Paravasaten“, d.h. wenn das Kontrastmittel teils oder gänzlich bei der Injektion paravasal appliziert wurde. (Abb. 6)
Erstaunlicherweise wurde z.B. in der deutschen Studie, die am intensivsten mit klinischen Nachuntersuchungen verbunden war, bei ca. 120 Paravasaten mit sehr verschiedener Ausdehnung nur in weniger als 5 Fällen ein Zusammenhang mit einem lokalen Tumorgeschehen vermutet. Wahrscheinlich wird das lokale Gewebe durch die dichten Thorotrast-Ablagerungen weitgehend zerstört. Abschließende epidemiologische Untersuchungen zeigten, dass die Gesamtsterblichkeit in der Thorotrastgruppe um das 2,9-fache im Vergleich zur Allgemeinbevölkerung erhöht ist. Dabei wurde deutlich, dass die bösartigen Neubildungen in der Thorotrast-exponierten Kohorte die häufigste Todesursache darstellten. Während in der Allgemeinbevölkerung Lungenkrebs die bei weitem häufigste Krebstodesursache darstellt, ist in der Thorotrast-exponierten Patientengruppe Leberkrebs die häufigste Todesursache. Das Mortalitätsrisiko ist hier gegenüber der Allgemeinbevölkerung um das 167-fache (für Männer) und 127-fache (für Frauen) sowie das 164-fache für beide Geschlechter erhöht. In diesem Kontext wurden signifikante Erhöhungen der Sterblichkeitsraten auch für maligne Neubildungen der Knochen (7,1-fach), der Lunge (1,2-fach) und für das Lymph- und Knochenmark-System (5,4-fach) beobachtet. Es traten vermehrt das myeloische Syndrom und akute myeloische Leukämien (AML) auf. Dabei ist von Interesse, dass die AML hier eine lange Latenzzeit hat, während die Latenzzeit nach externer Strahlenexposition wesentlich kürzer ist (z.B. nach den Atombombenabwürfen in Hiroshima und Nagasaki) [17], [18], [19].
Bei einem kritischen Rückblick auf die Geschichte der Thorotrastanwendung ergeben sich bemerkenswerte Feststellungen. In allen Ländern, in denen damals die Angiographie etabliert war, wurde das neue Kontrastmittel als gut verträglich und mit ausgezeichnetem Gefäßkontrast gefeiert. Man darf nicht vergessen, dass damals andere Kontrastmittel schwere Nebenwirkungen hervorriefen und wesentlich schlechtere radiologische Aufnahmen lieferten. Es erforderte damit schon ein besonderes Engagement und auch Mut, gegen diese allgemeine Begeisterung kritisch anzugehen. Bemerkenswerterweise hat sich die US-amerikanische Food and Drug Administration (FDA) schon um 1933 warnend zu Thorotrast geäußert; gleichzeitig muss man aber feststellen, dass das Präparat in größeren amerikanischen Kliniken bis weit über die 1950er Jahre im Einsatz war. In Deutschland war es der Heidelberger Chirurg Professor Karl Heinrich Bauer (1890-1978), der bereits 1939 auf dem deutschen Chirurgenkongress vor Thorotrast gewarnt hat und schließlich 1943 den wegweisenden Artikel über „Thorotrast und Krebsgefahr” schrieb [20].
Die FDA entzog schließlich 1964 die Genehmigung zur klinischen Nutzung von Thorotrast. Testagar vermarktete das Mittel allerdings noch bis 1967 und ließ seinen Einsatz z.B. in Forschungsprojekten zur Verfolgung der Wirkung von Chemotherapeutika bei bösartigen Erkrankungen der Leber und bösartigen Zysten des Gehirns erproben [21].
Der zeitweise weltweite Erfolg des Röntgenkontrastmittels Thorotrast wurde letztendlich beflügelt durch den dringenden Bedarf nach geeigneten Kontrastmittel zur Organ- und Gefäßdiagnostik in den 1920er Jahren, durch die hervorragende diagnostische Qualität der radiologischen Bilder und das Fehlen von direkten Kontraindikationen. Die euphorische weltweite Anwendung und die damit verbundenen deutlich unterschätzten Risiken durch epidemiologisch nachgewiesene karzinogene Wirkungen machte Forschenden nach Abschluss der Studien direkt bewusst, dass insbesondere die Dosimetrie für inkorporierte Alpha-Strahler nur sehr ungenau war. Sie musste deutlich verbessert werden, um die Mechanismen der durch Inkorporation von Alphastrahlern hervorgerufen Strahlenwirkungen, die daraus resultierenden deterministischen und vor allem die stochastischen Gesundheitseffekte und das allgemeine biokinetische Verhalten von Radionukliden im menschlichen Körper besser zu verstehen.
Anders als bei der zellulären Strahlenbiophysik nach Röntgen- und Gammastrahlenbestrahlung, bei der alle Zellen ähnlich exponiert werden, sind bei Exposition durch inkorporierte Alpha-Strahler mit einer geringen Reichweite von etwa 50 μm nur wenige (typischerweise 1%) der Zellen exponiert. Diese wenigen Zellen sind dann aber viel stärker von einer Strahleneinwirkung betroffen. Deshalb müssen hier unterschiedliche Formen der Dosiswirkung angenommen und auch entsprechend in Strahlenschutzverordnungen berücksichtigt werden [22].
Die Geschichte des Röntgenkontrastmittels Thorotrast hat aber auch gezeigt, dass man die zuerst euphorisch positiven und im späteren Verlauf negativen Erfahrungen durchaus für neue Forschungsansätze nutzen kann. So fand u.a. das Konzept des linearen Energietransfers (LET) bzw. der linearen Dosiswirkung ohne Schwellendosis (LNT) Anwendung in der Alphastrahlen-Dosimetrie und -Wirkung [23]. In der Krebstherapie wurden neue klinische Behandlungsansätze in der radiopharmazeutischen Therapie mit Alphateilchen emittierenden Radionukliden entwickelt, bei der die Strahlung direkt auf die Zieltumorzellen oder deren Mikroumgebung abgegeben wird. Um hier von vornherein die sichere klinische Anwendung und die Mechanismen strahlenbiologischer Wirkungen der neu entwickelten alphastrahlenden Radiopharmaka, wie z.B. Actinium-225-antibody oder Radium-223-dichlorid, in kleinsten Zielvolumen besser zu verstehen und vorhersagen zu können, wurde eine neue Dosimetrie auf mikro- oder multizellulärer Ebene entwickelt. Da hier die mikroskopische Verteilung der Alphastrahlung bei einzelnen Patienten und Patientinnen in der Regel nicht messbar ist, wurden für die Übertragung der aus Tierversuchen stammenden Dosisberechnungen pharmakokinetische Modelle entwickelt, die die Pharmakokinetik auf der Makro- und Mikroebene miteinander verbinden und so die Extrapolation der Kinetik auf der Mikroebene aus makroskopischen Messungen beim Menschen ermöglichten [24], [25], [26].
Danksagung
Ich bedanke mich herzlich bei Herrn Professor Dr. Gerhard van Kaick, Heidelberg und Herrn Prof. Dr. Dr. Christian Streffer, Essen für ihre Anregungen und die kritische Durchsicht des Manuskripts.
Bildnachweis Abbildung 1, Abbildung 2, Abbildung 3, Abbildung 4, Abbildung 5, Abbildung 6: G. van Kaick, DKFZ, Heidelberg.
Literatur
- 1.Dandy W.E. Ventriculography following the injection of air into the cerebral ventricles. Ann Surg. 1918;68(1):5–11. doi: 10.1097/00000658-191807000-00002. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 2.dos Santos R., Lamas A.C., Pereira-Caldas J. Arteriografia da aorta e dos vasos abdominais. Bull Mem Soc Natl Chir. 1929;47:93. [Google Scholar]
- 3.Moniz E. Physio-Röntgenologie des Blutkreislaufes im Gehirn, in den Meningen und in den übrigen Geweben des Kopfes. Fortschr Röntgenstr. 1933;48(4):398–405. [Google Scholar]
- 4.Blühbaum T., Frik K., Kalkbrenner H. Eine neue Anwendungsart der Kolloide in der Röntgendiagnostik. Fortschr Röntgenstr. 1928;37:18. [Google Scholar]
- 5.Radt P. Eine Methode zur Röntgenstrahlung-Kontrastdarstellung von Milz und Leber. Klin WSchr. 1929;8:2128. [Google Scholar]
- 6.Oka M. Eine neue Methode zur röntgenologischen Darstellung der Milz (Lienographie) Fortschr Röntgenstr. 1929;40:497. [Google Scholar]
- 7.IAEA. The Dosimetry and Toxicity of Thorotrast. A scientific meeting organized by the International Atomic Energy Agency and the World Health Organization Vienna, 4-7 October, 1965. (https://www-pub.iaea.org/MTCD/Publications/PDF/te_106_web.pdf, aufgerufen 30.11.2021).
- 8.Abbatt J.D. History of the use and toxicity of Thorotrast. Environ Res. 1979;18(1):6–12. doi: 10.1016/0013-9351(79)90131-2. [DOI] [PubMed] [Google Scholar]
- 9.Chemische Fabrik von Heyden Aktiengesellschaft, Radebeul-Dresden 1874-1934 - Memorabilia from 6 decades, compiled by Dr. O. Schlenk, Radebeul. Publisher: Kupky & Dietze (Inh. C. and R. Müller), Radebeul. (http://www.arevipharma.com/geschichte_chemische_fabrik_von_heyden_kapitel15.html) Albert Gieseler - Chemische Fabrik von Heyden Aktiengesellschaft (albert-gieseler.de). http://www.albert-gieseler.de/dampf_de/firmen4/firmadet49279.shtml
- 10.Sammlung von Produktschriften im Archiv Deutsches Röntgen-Museum.
- 11.https://law.justia.com/cases/pennsylvania/supreme-court/1990/394-pa-super-464-1.html (aufgerufen am 30.11.2021).
- 12.http://www.arevipharma.com/geschichte_chemische_fabrik_von_heyden_kapitel1.html.
- 13.Krasninskas A.M., Minda J., Saul S.H., Shaked A., Furth E.E. Redistribution of thorotrast into a liver allograft several years following tranplantation: a case report. Mod Pathol. 2004;17:117–120. doi: 10.1038/modpathol.3800008. https://www.nature.com/articles/3800008. [DOI] [PubMed] [Google Scholar]
- 14.Jakobi W., Roth P., Noske D. Mögliches Risiko und Verursachungs-Wahrscheinlichkeit von Knochen- und Leberkrebs durch die berufliche Alphastrahlen-Exposition von Beschäftigten der ehemaligen WISMUT AG. Bundesamt für Strahlenschutz. GSF-Bericht 1/98, GSF-Forschungszentrum. Neuherberg. 1998:27–37. (abrufbar unter: https://www.osti.gov/etdeweb/servlets/purl/631543) [Google Scholar]
- 15.Kaul A, Noffz W (1978). Tissue Dose in Thorotrast Patients. Paper held at the Int. Symposium on Biological Effects of injected 224Ra (ThX) and Thorotrast. Alta, Utah/USA, Jul. 21-23, 1974. Health Physics, 35(1), 113-121. doi:10.1097/00004032-197807000. [DOI] [PubMed]
- 16.Wenz W., van Kaick G. Strahlenspätwirkungen bei Thorotrast-Ablagerungen. In: Langenbecks Archiv für Chirurgie. Springer, Berlin. Heidelberg. 1969 doi: 10.1007/978-3-662-41130-8_169. [DOI] [PubMed] [Google Scholar]
- 17.van Kaick G., Dalheimer A., Hornik S., Kaul A., et al. The German Thorotrast Study: recent results and assessment of risks. Radiat Res. 1999;152(6 Suppl):S64–S71. [PubMed] [Google Scholar]
- 18.Becker N, Liebermann D, Wesch H, van Kaick G. Epidemiologische Auswertung der Mortalität in der Thorotrast-exponierten Gruppe und der Kontrollgruppe im Vergleich zur Mortalität in der Allgemeinbevölkerung. Deutsches Krebsforschungszentrum Heidelberg. BMU – 2006-682. (abrufbar unter: https://www.bmu.de/fileadmin/bmu-import/files/strahlenschutz/schriftenreihe_reaktorsicherheit_strahlenschutz/application/pdf/schriftenreihe_rs682.pdf).
- 19.Grosche B., Birschwilks M., Wesch H., Kaul A., van Kaick G. The German Thorotrast Cohort Study: a review and how to get access to the data. Radiat Environ Biophys. 2016;55(3):281–289. doi: 10.1007/s00411-016-0651-8. [DOI] [PubMed] [Google Scholar]
- 20.Bauer K.-H. Thorotrast und Krebsgefahr. Chirurg. 1943;15:104. [Google Scholar]
- 21.Granger G.A. Use of thorotrast. Br Med J. 1967;4(5571):112. [Google Scholar]
- 22.van den Heuvel M. Den Mechanismen der Strahlenwirkung auf der Spur. (https://idw-online.de/de/news92846, aufgerufen am 23.11.2021).
- 23.Bundesamt für Strahlenschutz (Hrsg). Die Empfehlungen der Internationalen Strahlenschutzkommission (ICRP) von 2007. ICRP Veröffentlichung 102. Verabschiedet im März 2007. (abrufbar unter: https://www.icrp.org/docs/P103_German.pdf).
- 24.Sgouros G., Hobbs R.F., Song H. Modelling and Dosimetry for Alpha-Particle Therapy. Curr Radiopharm. 2011;4(3):261–265. doi: 10.2174/1874471011104030261. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 25.Sgouros G., Hobbs R.F., Josefsson A. Dosimetry and Radiobiology of Alpha-Particle Emitting Radionuclides. Curr Radiopharm. 2018;11(3):209–214. doi: 10.2174/1874471011666180426130058. [DOI] [PubMed] [Google Scholar]
- 26.Xu T., Liu T., Li G., Dugal C., Aydemir N.A., Liu Y., Roeske J.C. Technical Note: The development of a multi-physics simulation tool to estimate the background dose by systemic targeted alpha therapy. Med Phys. 2020;47(6):2550–2557. doi: 10.1002/mp.14111. [DOI] [PMC free article] [PubMed] [Google Scholar]